
Laktata acido
kemia kombinaĵo / From Wikipedia, the free encyclopedia
Laktata acido (aŭ laktacido; kemia formulo: C3H6O3) estas acida kemia kombinaĵo kiu rolas en multaj biokemiaj procezoj. Ĝi estas uzata en pluraj manĝaĵoj por konservi kaj reguli aliajn acidojn.
| Laktata acido | |||
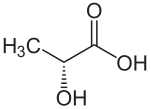 | |||
| Plata kemia strukturo de la Laktata acido | |||
 | |||
| Tridimensia kemia strukturo de la Laktata acido | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 50-21-5 | ||
| ChemSpider kodo | 96860 | ||
| PubChem-kodo | 612 | ||
| Merck Index | 15,5385 | ||
| Fizikaj proprecoj | |||
| Aspekto | solidaĵo | ||
| Molmaso | 90,078 g·mol−1 | ||
| Denseco | 1,2485g cm−3 | ||
| Fandpunkto | 53 °C | ||
| Bolpunkto | 122 °C | ||
| Refrakta indico |  1,4392 1,4392 | ||
| Ekflama temperaturo | 110 °C | ||
| Acideco (pKa) | 3,86 | ||
| Mortiga dozo (LD50) | 3543 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R38 R41 | ||
| Sekureco | S26 S39 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H315, H318 | ||
| GHS Deklaroj pri antaŭgardoj | P264, P280, P302+352, P305+351+338, P310, P321, P332+313, P362[1] | ||
(25 °C kaj 100 kPa) | |||
En solvaĵo, ĝi povas perdi protonon el la acida grupo. Tiel estiĝas la laktata jono CH3CH(OH)COO−, kiu miksiĝas kun akvo aŭ etanolo kaj estas higroskopa.


