
Ácido fluoroantimónico
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre Ácido fluoroantimónico?
Resumir este artículo para un niño de 10 años
El ácido fluoroantimónico (HSbF6) es una mezcla de fluoruro de hidrógeno y pentafluoruro de antimonio en diversas proporciones.[2] La proporción 1:1 conduce al superácido más fuerte conocido, el cual se ha demostrado que protona incluso a los hidrocarburos para producir carbocationes e H2. El ácido fluoroantimónico es el más corrosivo de los llamados super ácidos.[3]
 | ||
 | ||
| Nombre IUPAC | ||
| Hexafluoroantimonato (VI) de hidrógeno | ||
| General | ||
| Fórmula semidesarrollada | HF-SbF5 | |
| Fórmula estructural |
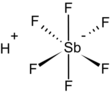 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | [16950-06-4][1] | |
| ChemSpider | 21241496 | |
| PubChem | 6337100 | |
| Propiedades físicas | ||
| Apariencia | jarabe incoloro | |
| Masa molar | 236,808 g/mol | |
| Propiedades químicas | ||
| Acidez | -31 pKa | |
| Solubilidad en agua | Se descompone, generando una explosión química | |
| Peligrosidad | ||
| Frases R | R39/23/24/25-35 | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La reacción de fluoruro de hidrógeno (HF) y SbF5 es exotérmica. HF libera el catión (H+), y su base conjugada (F−) es secuestrada por una o más moléculas de SbF5 para producir SbF6− octaédrico. Este anión se clasifica como no coordinante, porque es tanto un nucleófilo débil y una base muy débil. El catión H+ permanece efectivamente «desnudo», lo que trae como consecuencia la extrema acidez del sistema. El ácido fluoroantimónico es 2×1019 veces más fuerte que el ácido sulfúrico. La reacción del fluoruro de hidrógeno y pentafluoruro de antimonio procede como sigue:
