Toriumfluoridi
kemiallinen yhdiste From Wikipedia, the free encyclopedia
Remove ads
Toriumfluoridi tai torium(IV)fluoridi (ThF4) on torium- ja fluoridi-ionien muodostama epäorgaaninen ioniyhdiste. Toriumfluoridia ei esiinny vapaana luonnossa, vaan sitä saadaan monatsiitista ja muista toriummineraaleista.
Remove ads
Ominaisuudet
Toriumfluoridi on normaalioloissa kiinteää valkoista ainetta. Toisin kuin toriumkloridi, kidevedetön toriumfluoridi on huoneenlämpötilassa vain vähän hygroskooppista.[1] Siitä tunnetaan kidevedettömän muodon lisäksi muutama hydraatti, mutta näiden tarkka rakenne ei poikkeuksellisesti ole selvillä. Muodostuvan kidevedellisen fluoridin arvellaan olevan oktahydraattia, joka kuivuessaan muuttuu ensin tetrahydraatiksi ja sitten dihydraatiksi.[4] Toriumfluoridi liukenee vähäisissä määrin veteen; sen liukoisuus on paljon pienempi kuin harvinaisten maametallien fluoridien, jotka nekin ovat niukkaliukoisia.[1]
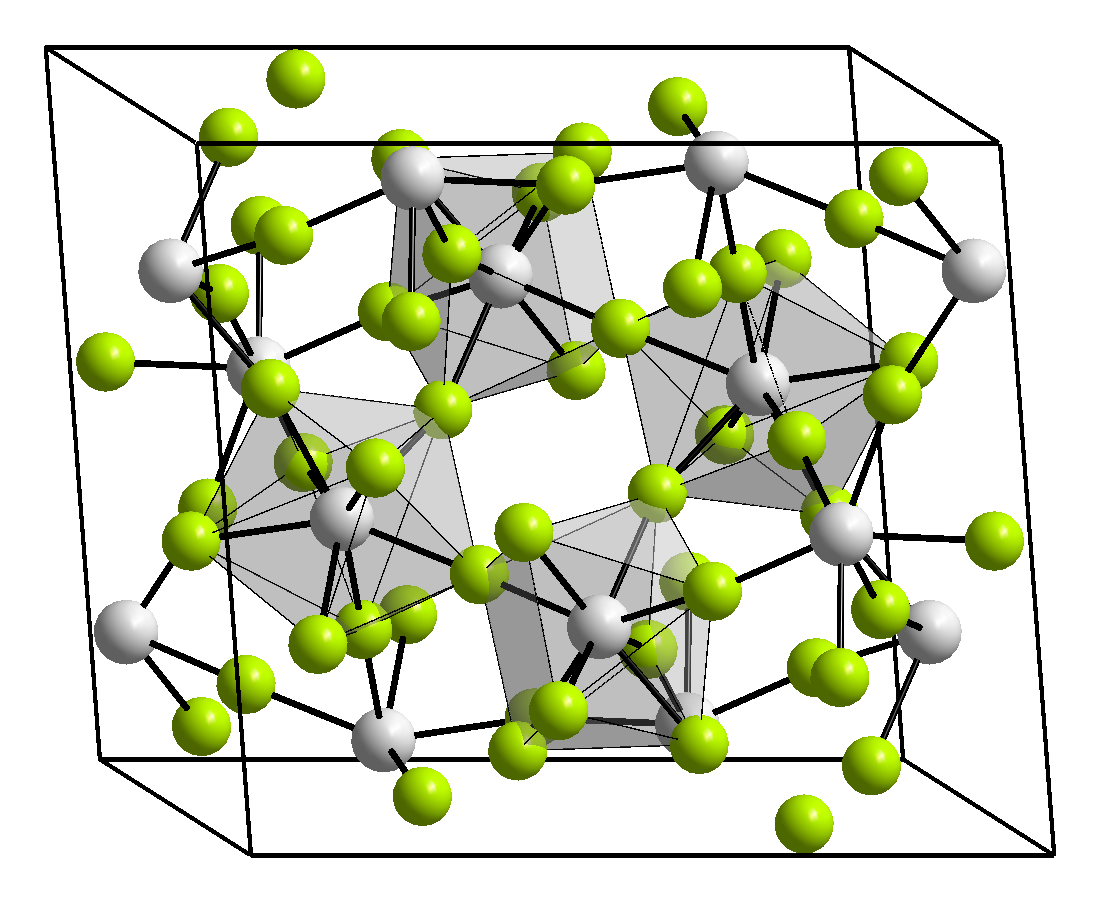
Toriumfluoridin monokliininen kiderakenne on samanlainen kuin zirkoniumfluoridilla ja hafniumfluoridilla ja sen avaruusryhmä on C2/c (hilavakiot a=1 304,9 pm, b=1 112,0 pm, c=853,8 pm).[4] Toriumfluoridi reagoi ilman kosteuden kanssa yli 500 °C lämpötilassa muodostaen ThOF2-yhdisteen.[3] Se reagoi alkalimetallien fluoridien kanssa muodostaen kompleksisia fluoridisuoloja, kuten KThF5 ja K2ThF6.[1]
Toriumin tavoin myös toriumfluoridi on radioaktiivista. Se on heikko alfasäteilijä.
Remove ads
Valmistus ja käyttö
Toriumfluoridia voidaan valmistaa antamalla toriummetallin tai toriumkarbidin reagoida suoraan fluorin kanssa, tai sitten vetyfluoridin reaktiolla muiden toriumin halidien, toriumin oksidien tai hydroksidien, tai toriumoksalaatin kanssa.[4]
Yhdistettä käytetään valmistettaessa puhdasta toriummetallia sekä korkean lämpötilan keraameissa ja joissakin optisissa pinnoitteissa.[3]
Toriumfluoridi on mahdollinen torium-ydinpolttoainekiertoa käyttävän sulasuolareaktorin polttoaine.[5][6]
Remove ads
Lähteet
Aiheesta muualla
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads