Top Qs
Chronologie
Chat
Contexte
Glycine (acide aminé)
composé chimique De Wikipédia, l'encyclopédie libre
Remove ads
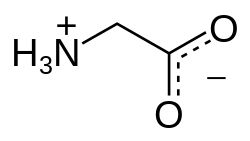
La glycine (abréviations UICPA-UIBBM : Gly et G) est un acide α-aminé et l'un des vingt-deux acides aminés protéinogènes. Elle est encodée sur les ARN messagers par les codons GGU, GGC, GGA et GGG. C'est le plus simple des acides α-aminés, et elle ne possède aucun atome de carbone asymétrique. Ainsi, c'est le seul acide aminé protéinogène achiral. Son rayon de van der Waals est égal à 48 Å. Grâce à sa chaîne latérale minimale d'un seul atome d'hydrogène, il peut s'adapter à des environnements hydrophiles ou hydrophobes.
Jadis appelée glycocolle ou acide aminoacétique, la glycine possède un goût sucré et peut être utilisée pour améliorer le goût d'édulcorants ou comme exhausteur de goût (E640). Le terme glycocolle, traditionnel en français, présentait l'avantage de ne pas risquer la confusion avec un nom de plante, mais l'appellation anglaise glycine a prévalu.
Remove ads
Métabolisme
Résumé
Contexte
Biosynthèse
La glycine peut être synthétisée dans le corps humain de plusieurs façons. Ce n’est donc techniquement pas un acide aminé essentiel. Toutefois, les quantités synthétisables sont limitées, ce qui en fait un acide aminé semi-essentiel[5],[6].
La voie principale de biosynthèse de la glycine découle d’un autre acide aminé, la sérine. Cette synthèse peut être catalysée soit par la sérine hydroxyméthyltransférase (SHMT), une transférase dépendant du phosphate de pyridoxal, une coenzyme dérivée de la vitamine B6, soit par un système enzymatique du nom de glycine synthase agissant dans le foie des vertébrés et dépendant de la coenzyme nicotinamide adénine dinucléotide (NAD). Ces deux réactions sont réversibles.
La glycine peut également être synthétisée à partir de la thréonine, de la choline ou de l’hydroxyproline. Ces voies métaboliques ont principalement lieu dans le foie et les reins[6].
Dégradation
Les deux réactions réversibles listées ci-dessus peuvent être utilisées pour convertir la glycine en sérine, la principale chez les animaux étant le système de clivage de la glycine (GCS).
Une troisième voie est sa conversion en glyoxylate, qui peut être catalysée soit par l’enzyme D-Aminoacide oxydase[6], soit par la glycine déshydrogénase. Le glyoxylate est ensuite oxydé en oxalate dans le foie par l’enzyme lactate déshydrogénase avec l’aide du NAD.
La glycine est également utilisée comme précurseur de nombreuses autres molécules dans le corps (voir Fonctions biologiques ci-dessous).
La demi-vie de la glycine dans le corps varie linéairement suivant sa dose, pouvant aller d’une demi-heure à 4 heures[7].
Remove ads
Fonctions biologiques
- La molécule de glycine joue un rôle de neurotransmetteur inhibiteur au niveau de la moelle épinière et de modulateur allostérique positif des récepteurs NMDA au glutamate dans l'ensemble du système nerveux central.
- Ce n'est pas une molécule chirale (c'est une exception pour les acides aminés).
- La glycine est un précurseur des porphyrines, mais aussi de la créatine (dans le foie), de l'acide urique (forme d'excrétion de l'azote chez les espèces uricotélique comme les oiseaux), du glutathion (composé qui participe à la réduction des radicaux libres), de l'acétylcholine (neurotransmetteur).
- La synthèse du collagène nécessite de la glycine.
- Elle entre dans la composition des acides biliaires primaires : elle se conjugue aux sels biliaires, les rendant plus solubles.
- Ajoutée au succinyl-CoA, elle forme l'hème, de l'hémoglobine par exemple.
Remove ads
Présence dans l'espace
De la glycine avait été trouvée dans de nombreuses météorites. Et depuis 2004, elle a été identifiée dans la traînée de comètes : d'abord par la sonde américaine Stardust dans le panache de la comète Wild 2[8], puis dans la queue de la comète 67P/Tchourioumov-Guérassimenko par l'instrument ROSINA (Rosetta Orbiter Spectrometer for Ion and Neutral Analysis) installé sur la sonde Rosetta[9],[8].
Ceci conforte l'hypothèse des exobiologistes d'une introduction d'acides aminés d'origine non terrestre dans l'atmosphère primitive de la Terre[8],[10]. La glycine n'étant pas volatile, sa présence dans la queue de comètes laisse penser qu'elle serait présente en plus grande quantité dans la glace cométaire. Cette découverte renforce l'hypothèse selon laquelle la vie pourrait s'être formée sur Terre grâce à l'apport de molécules d'origine extraterrestre dans la « soupe prébiotique », d'autant que les capteurs de la sonde Rosetta ont aussi détecté du phosphore, élément constitutif de l'ATP, moteur énergétique cellulaire essentiel pour le vivant sur Terre[8].
Analogue structurel
Un analogue structurel de la glycine est le glyphosate, molécule utilisée comme matière active de la plupart des pesticides désherbants totaux foliaires utilisés dans le monde.
Notes et références
Liens externes
Articles connexes
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads