
Hydrogénopersulfate de potassium
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
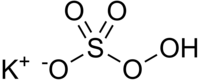
L'hydrogénopersulfate de potassium ou peroxymonosulfate de potassium [aussi connu sous l'abréviation MPS (pour monopersulfate) et les noms de marque Caroat et Oxone] est le sel de potassium de l'acide persulfurique. Il est largement utilisé comme agent oxydant en chimie organique[3].
| Hydrogénopersulfate de potassium | |||
| |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | hydrogénopersulfate de potassium | ||
| Synonymes |
peroxymonosulfate de potassium |
||
| No CAS | 10361-76-9 37222-66-5 (sel triple - voir le texte) |
||
| No ECHA | 100.030.158 | ||
| PubChem | 23712892 | ||
| SMILES | |||
| InChI | |||
| Propriétés chimiques | |||
| Formule | HKO5SKHSO5 | ||
| Masse molaire[1] | 152,168 ± 0,007 g/mol H 0,66 %, K 25,69 %, O 52,57 %, S 21,07 %, |
||
| Précautions | |||
| Directive 67/548/EEC[2] | |||
Symboles : C : Corrosif O : Comburant Phrases R : R8 : Favorise l’inflammation des matières combustibles. R34 : Provoque des brûlures. R37 : Irritant pour les voies respiratoires. Phrases S : S17 : Tenir à l’écart des matières combustibles. S36/37/39 : Porter un vêtement de protection approprié, des gants et un appareil de protection des yeux/du visage. |
|||
| Transport | |||
Numéro ONU : 3260 : SOLIDE INORGANIQUE CORROSIF, ACIDE, N.S.A. Classe : 8 Étiquette :  8 : Matières corrosives Emballage : Groupe d'emballage II : matières moyennement dangereuses ; |
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Ce sel est commercialisé par quatre compagnies : Arch Pool Chemicals (une filiale de Lonza Pharma Group), Evonik (auparavant Degussa) sous le nom de marque Caroat, DuPont sous le nom de marque Oxone (qui maintenant est devenu un mot commun dans le vocabulaire de la chimie) et Hangzhou Focus Chemical Co., Ltd. C'est le composant actif du sel triple du monopersulfate de potassium, de formule 2KHSO5•KHSO4•K2SO4[4]. Le potentiel standard (E0) de KHSO5 vaut 1,85 V[4] pour la demi-réaction qui génère l'ion hydrogénosulfate :
- HSO5− + 2 H+ + 2 e− → HSO4− + H2O E0 = 1,85 V

