Top Qs
Chronologie
Chat
Contexte
Fluorure de potassium
composé chimique De Wikipédia, l'encyclopédie libre
Remove ads
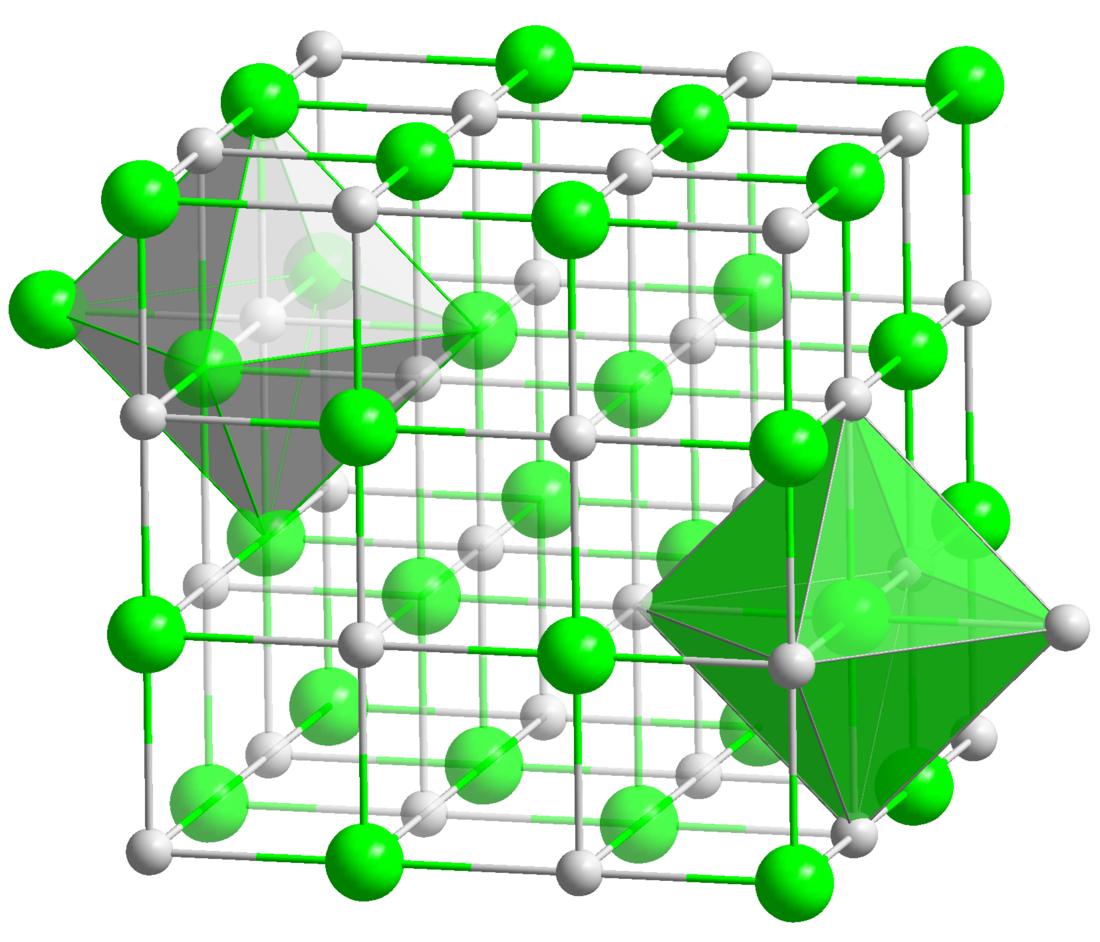
Le fluorure de potassium est un composé inorganique de formule KF. Après le fluorure d'hydrogène, il est la principale source d'ion fluorure utilisée dans l'industrie et en chimie. C'est un halogénure de métal alcalin présent naturellement sous la forme d'un minéral rare, la carobbiite. Les solutions de KF peuvent attaquer le verre, du fait de la formation de fluorosilicates solubles, même si l'acide fluorhydrique est plus efficace pour cette tâche.
Remove ads
Propriétés
Le fluorure de potassium se présente sous la forme d'une poudre blanche hygroscopique, généralement sous sa forme dihydrate. Le dihydrate fond à 46 °C dans son eau de cristallisation. On peut dissoudre 485 g de fluorure de potassium dans un litre d'eau à 20 °C.
Le fluorure de potassium a une enthalpie standard de formation de ΔHf°= -569 kJ/mol[8]
Du fait que le potassium naturel contient 0,0118 % du radioisotope 40K, la radioactivité de KF est de 20 979 Bq kg−1, à 89,28 % du rayonnement bêta et à et 10,72 % rayonnement gamma de 1,460 83 MeV.
Remove ads
Synthèse
Le fluorure de potassium peut être préparé par dissolution carbonate de potassium en excès dans l'acide fluorhydrique. Lors de l'évaporation de la solution, il se forme des cristaux de bifluorure de potassium. En chauffant ce bifluorure on obtient le fluorure de potassium :
Ce sel ne peut évidemment pas être préparé dans un récipient en verre ou en porcelaine car il serait attaqué par l'acide fluorhydrique. Un récipient en plastique (PTFE) résistant à la chaleur ou en platine doit être utilisé.
Remove ads
Applications
Chimie
En chimie organique, le fluorure de potassium peut être utilisé pour la conversion de composés organochlorés en composés organofluorés, via la réaction de Finkelstein[9]. Pour de telles réactions on utilise en général un solvant polaire tel que le diméthylformamide (DMF), l'éthylène glycol ou le diméthylsulfoxyde (DMSO)[10].
Autres
Le fluorure de potassium est utilisé dans la production d'émail, comme additif pour ciment, comme oxydant dans la poudre de soudure d'aluminium. Il est aussi utilisé comme agent de conservation du bois et pour la gravure sur verre. Il peut aussi être utilisé comme source d'ions fluorures dans les produits d'hygiène buccale (dentifrice, bain de bouche, etc.) et pour des aliments fluorés (sel alimentaire, eau).
Précautions
Comme d'autres sources d'ions fluorures, KF est toxique, même si les doses létales sont du niveau du gramme pour l'homme. Il est dangereux par inhalation et ingestion. Il est hautement corrosif, tout contact avec la peau pouvant entraîner de sévères brûlures.
Notes et références
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads