Bioloxía dos sistemas, bioloxía de sistemas ou bioloxía sistémica é o termo empregado para describir un conxunto de correntes na investigación das biociencias e un movemento orixinario destas correntes. Os seus propoñentes describen a bioloxía dos sistemas como un campo de investigación interdisciplinar baseado na bioloxía, que se centra nas interaccións complexas dos sistemas biolóxicos. Segundo os seus propoñentes, a bioloxía dos sistemas utiliza unha perspectiva holística, en contrapunto a unha perspectiva reducionista. En particular, a partir do ano 2000 o termo foi moi utilizado nas biociencias e nunha variedade de contextos. A bioloxía dos sistemas pretrende a modelaxe e descuberta de propiedades emerxentes, propiedades dun sistema cuxa descrición teórica só se fai posíbel grazas a técnicas usadas case exclusivamente na bioloxía dos sistemas.
A bioloxía dos sistemas pode considerarse a partir dunha variedade de aspectos:
- Como un campo de estudo, particularmente o estudo das interaccións entre os compoñentes de sistemas biolóxicos, e como estas interaccións orixinan a función e comportamento dese sistema (por exemplo, os enzimas e os metabolitos nunha vía metabólica).[1][2]
- Como paradigma, xeralmente definido en antítese ao chamado paradigma reducionista (organización biolóxica), aínda que fiel e coherente co método científico. A distinción entre os dous paradigmas é ilustrada polas seguintes citacións:
- "A abordaxe reducionista identificou con éxito a maioría dos compoñentes e moitas interaccións mais, desafortunadamente, non ofrece ningún concepto ou método convincente para entender como emerxen as propiedades de determinado sistema (...) a multiplicidade de causas e efectos nos conxuntos de redes biolóxicas trátase mellor por medio da observación simultánea, por métodos cuantitativos, dos múltiplos compoñentes e por unha integración rigorosa dos datos científicos cos modelos matemáticos" Science[3]
- "A bioloxía dos sistemas(...) trata de xuntar e non de descompor, da integración e non da redución. Require que desenvolvamos maneiras de pensar acerca da integración que sexan tan rigorosas coma os nosos programas reducionistas, só que diferentes(...) Iso significa mudar a nosa filosofía, en todo o sentido do termo"'Denis Noble[4]
- Como unha serie de protocolos operacionais usados para a realización de investigacións (incluíndo a compoñente práctica de laboratorio). Estes protocolos inclúen un ciclo composto de teoría, modelaxe analítica ou computacional para propor hipóteses específicas testábeis, validación experimental e utilización da recentemente adquirida descrición cuantitativa para refinar a teoría ou modelo computacionais.[5][6] Dado que o obxectivo é un modelo das interaccións dun sistema, as técnicas experimentais que mellor serven á Bioloxía dos Sistemas son aqueles que se estenden aos sistemas e tentan ser tan completos como sexa posíbel. Deste modo, empréganse a transcritómica, metabolómica e proteómica e técnicas con elevada capacidade procesiva para recoller datos cuantitativos para a construción e validación dos modelos.
- Como aplicación da teoría dos sistemas dinámicos á bioloxía molecular.
- Como fenómeno socio-científico definido pola estratexia de integrar datos complexos de interaccións en sistemas biolóxicos a partir de varias fontes experimentais, utilizando para tal ferramentas e persoal interdisciplinares.
Esta variedade de puntos de vista ilustra o feito de que a Bioloxía dos Sistemas se refire a un agregado de conceptos marxinalmente sobrepoñíbeis e non a un único campo claramente explicitado. Con todo, o termo adquiriu gran popularidade a partir de 2007, co desenvolvemento de cátedras e institutos de Bioloxía dos Sistemas por todo o mundo.
A bioloxía dos sistemas ten raíces nos seguintes campos:
- modelaxe cuantitativa da cinética enzimática, unha disciplina que floreceu entre 1900 e 1970;
- modelaxe matemática do crecemento de poboación;
- simulacións desenvolvidas para o estudo da neurofisioloxía;
- teoría do control e cibernética.
Un dos teóricos precursores da bioloxía dos sistemas foi Ludwig von Bertalanffy coa teoría xeral dos sistemas [7]. Unha das primeiras simulacións numéricas en bioloxía publicouse en 1952 polos neurofisiólogos británicos Alan Lloyd Hodgkin e Andrew Fielding Huxley, que construíran un modelo matemático que describía e xustificaba o potencial de acción que se propaga ao longo do axón dunha célula neuronal.[8] O seu modelo describía unha función celular que emerxía da interacción entre dous compoñentes moleculares distintos, canles de sodio e de potasio, e pode ser vista como o comezo da Bioloxía de Sistemas computacional.[9] In 1960, Denis Noble developed the first computer model of the heart pacemaker.[10]
O estudo formal da bioloxía dos sistemas como disciplina distinta foi lanzado polo teórico de sistemas Mihajlo Mesarovic en 1966 durante un simposio internacional no Case Institute of Technology en Cleveland, Ohio intitulado "Systems Theory and Biology."[11][12]
As décadas de 1960 e 1970 viran o desenvolvemento de varias abordaxes para estudar sistemas moleculares complexos, tales como a Análise de Control Metabólico e a teoría de sistemas bioquímicos. Os éxitos da bioloxía molecular ao longo da década de 1980, conxuntamente co escepticismo en relación á bioloxía teórica que frecuentemente presentaba fallas nas súas previsións, levou a que a modelaxe cuantitativa de procesos biolóxicos fose vista con desconfianza e se tornase nun campo limitado de investigación.
Porén, o nacemento da xenómica funcional nos anos 1990 posibilitou a xeración de enormes cantidades de datos fiábeis, acoplados ao poder crecente e xigantesco da computación. En consecuencia, fíxose finalmente posíbel traballar con modelos realistas de sistemas biolóxicos. En 1997, o grupo de Masaru Tomita publicou o primeiro modelo cuantitativo do metabolismo de toda unha célula hipotética.
A redor do ano 2000, despois de que os Institutos de Bioloxía dos Sistemas se tivesen establecido en Seattle e Toquio, a bioloxía dos sistemas xurdiu como ramo independente, impulsado pola finalización de varios proxectos xenómicos, polo aumento exponencial de datos ómicos (por exemplo da xenómica e proteómica) e polo éxito paralelo de técnicas de elevada procesividade e de bioinformática. Dende entón, xurdiron varios institutos de investigación dedicados á Bioloxía dos Sistemas. Dende o verán de 2006, debido á escaseza de persoal competente na área da Bioloxía dos Sistemas[13] estableceranse diversos centros formadores en Bioloxía dos Sistemas en varias partes do mundo.
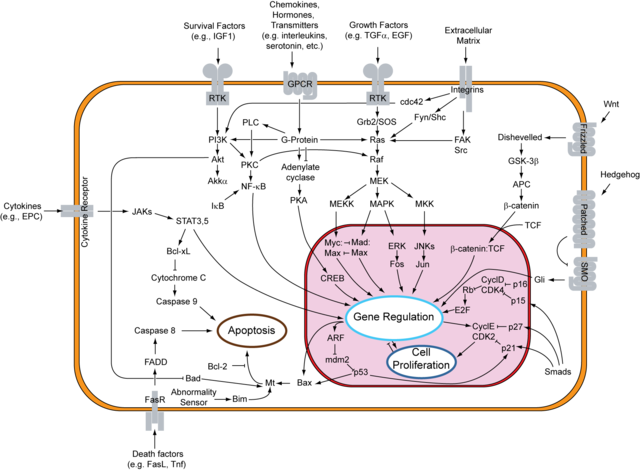
Podemos ver a bioloxía dos sistemas como a capacidade para obter, integrar e analizar datos complexos a partir de diversas fontes experimentais usando para tal ferramentas interdisciplinares. Algunhas plataformas tecnolóxicas comúns inclúen:
- Fenómica: analiza o conxunto de variacións fenotípicas que o organismo exhibe durante o seu tempo de vida.
- Xenómica: analiza toda a secuencia de ácido desoxirribonucleico (DNA) dun organismo, a disposición e evolución de xenes, incluíndo as variacións xenéticas entre células do mesmo organismo, por exemplo: variacións na lonxitude dos telómeros.
- Epixenómica / Epixenética: analiza os factores que regulan a transcrición xénica que non están codificados polo xenoma, por exemplo: metilación do DNA, acetilación de histonas.
- Transcritómica: analiza os niveis de expresión xénica dun organismo, tecido ou célula a través de técnicas como micromatrices de DNA ou análise seriada de expresión xénica.
- Interferómica: analiza os factores que corrixen ou interfiren coa expresión xénica despois da produción de RNA, por exemplo: Ribointerferencia, tamén coñecida como RNAi (do inglés RNA interference ou interferencia de RNA).
- "Tradutómica" / Proteómica: analiza os niveis de proteínas nun organismo, tecido ou célula por medio de electroforese en xel bidimensional, espectrometría de masa ou técnicas multidimensionais de identificación de proteínas (sistemas de HPLC avanzados, acoplados a espectrometría de masas). Son exemplo de subdisciplinas a fosfoproteómica, a glicoproteómica e outros métodos para detectar proteínas quimicamente modificadas.
- Metabolómica: analiza os niveis de todas as moléculas coñecidas como metabolitos.
- Glicómica: analiza todos os carbohidratos dun organismo, tecido ou célula.
- Lipidómica: analiza todos os lípidos dun organismo, tecido ou célula.
Alén da identificación e cuantificación das moléculas mencionadas anteriormente, existen outras técnicas que permiten a análise do dinamismo celular e das interaccións que ocorren dentro da célula. Estas técnicas inclúen:
- Interactómica: o estudo das interaccións entre moléculas. Neste momento o campo de investigación oficial denominase estudo das interaccións proteína-proteína (inglés: protein-protein interactions, PPI). O estudo das PPI pode incluír aspectos doutras disciplinas moleculares, tales como:
- Fluxómica: a medición das alteracións moleculares dinámicas ao longo do tempo.
- Biómica: análise sistémica do bioma.
As investigacións combínanse frecuentemente con métodos de perturbación a grande escala, incluíndo abordaxes do tipo químico ou xenético (por exemplo: RNAi, expresión anormal de xenes salvaxes ou mutantes) por medio de bibliotecas (coleccións) de substancias. Robots e sensores automáticos posibilitan a experimentación e adquisición de datos a tan larga escala. Estas tecnoloxías son aínda emerxentes e debátense cos problemas xerados pola enorme cantidade de datos producidos e unha relativa baixa calidade. Un número razoabelmente elevado de científicos cuantitativos (por exemplo: científicos e biólogos computacionais, estatísticos, matemáticos, enxeñeiros e físicos) procuran mellorar a calidade destas abordaxes e crear, refinar e retestar os modelos que reflicten máis rigorosamente determinadas observacións.
A abordaxe da bioloxía dos sistemas envolve frecuentemente o desenvolvemento de modelos mecanísticos, tales como a reconstrución de sistemas dinámicos a partir das propiedades cuantitativas dos seus elementos básicos.[14][15]
Por exemplo, unha rede celular pode ser modelada matematicamente por métodos do foro da cinética química e da teoría do control. Debido ao gran número de parámetros, variábeis e factores limitantes presentes en redes celulares, utilízanse moitas veces técnicas numéricas e computacionais. Ademais disto, utilízanse aínda outros aspectos da ciencia dos computadores e da informática na Bioloxía dos Sistemas, tales como:
- cálculos de proceso para crear modelos de procesos biolóxicos
- integración da información existente na literatura científica
- uso de técnicas de extracción de información e minaría de textos
- desenvolvemento da bases de datos online e repositorios para partillar dados e modelos
- abordaxes para integración de bases de datos e integración de interoperabilidade de programas de computador
- desenvolvemento de modos sintáctica e semanticamente racionais de representar un determinado modelo biolóxico
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.