Loading AI tools
אברון התא מוויקיפדיה, האנציקלופדיה החופשית
הריבוזום (Ribosome; מקור השם מחומצה ריבונוקלאית ומהמילה soma מיוונית שמשמעותה "גוף") הוא מבנה תוך-תאי המצוי בתאי כלל היצורים החיים ואחראי ליצירת החלבונים בתא. מאחר שכל החיים המוכרים לנו מבוססים על פעולת חלבונים, לריבוזום יש חשיבות מכרעת על חיי התא והאורגניזם כולו. בכל אחד מתאי גוף האדם כמיליון ריבוזומים, ובתאי הכבד – כחמישה מיליון.

מהות פעולת הריבוזום היא עבודת הרכבה על פי תוכנית מוכנה מראש (היא החומר התורשתי) של מרכיבי החלבון – חומצות אמינו - למולקולת חלבון חדשה. התהליך כולו מראשיתו עד סופו קרוי "תרגום" (Translation), מאחר שהריבוזום מתרגם את התוכנית המצויה בחומר התורשתי משפת הנוקלאוטידים לשפת חומצות האמינו והחלבונים.
ראשית תהליך התרגום הוא ביחידה זמנית של חומר גנטי מסוג RNA, שתפקידו להעביר את התוכנית לריבוזום – RNA זה נקרא RNA-שליח או mRNA. מולקולת ה-mRNA עוברת דרך הריבוזום, אשר קורא את המידע התורשתי ביחידות מידע בנות 3 נוקלאוטידים כל אחת, המכונות "קודונים" (Codons). כל קודון כולל אינפורמציה לזהות של חומצת אמינו אחת בחלבון הנוצר, על פי חוקיות המתוארת בקוד הגנטי. הריבוזום אוסף חומצת אמינו מתאימה לפי הקודון בעזרת מולקולות tRNA ומחבר אותה לקודמתה בתור, ואז ממשיך לקודון הבא. כך, קודון אחרי קודון, מורכב חלבון שלם. בקצה ה mRNA מצוי קודון מיוחד, "קודון סיום" (Stop codon), כשהריבוזום מגיע לקודון זה, הוא משחרר את מולקולת החלבון החדשה לחלל התא, משחרר את מולקולת ה-mRNA, ובכך תהליך התרגום מגיע לסופו. קריאה שגויה (misreading) מתקבלת כאשר אין התאמה בין הקוד המוטבע בRNA לחלבון המתקבל בסוף התהליך. שגיאה כזאת יכולה להיות ספונטנית או מושרית על-ידי תרכובות כמו אמינו-גליקוזידים כמו סטרפטומיצין בריכוזים נמוכים.[1]
ריבוזומים נמצאים בכל סוגי התאים ובכל יצור חי, וקיימים בשתי תצורות בסיסיות: המבנה הקיים ביצורים פרוקריוטים כגון חיידקים אמיתיים וחיידקים קדומים והמבנה הקיים ביצורים איקריוטיים. בתאים איקריוטיים, חלק מהריבוזומים צמודים לקרום אברוני הרשתית התוך-פלזמית. יחידה המכילה מספר ריבוזומים המתרגמים במקביל את אותו ה-mRNA (ומייצרים את אותו סוג של חלבון) נקראת "פוליזום".
הריבוזומים התגלו לראשונה באמצע שנות ה-50 של המאה ה-20 על ידי הביולוג הרומני ג'ורג'ה אמיל פאלאדה באמצעות מיקרוסקופ אלקטרוני, ונצפו כגרגירים או כחלקיקים צפופים. על גילוי זה זכה פאלאדה בפרס נובל. פרופ' עדה יונת זכתה בפרס נובל (2009) על חקר מבנה הריבוזום.

קוטרם של הריבוזומים כ-20 ננומטר, והם מורכבים מ-65% RNA-ריבוזומלי (rRNA) ומ-35% חלבונים ריבוזומליים (אנ').
הריבוזום מורכב משתי תת-יחידות (ראו תמונה), הקרויות לרוב "תת-היחידה הקטנה" ו"תת-היחידה הגדולה". כל יחידה מכילה רצועות ארוכות של rRNA. מחקרים שפגעו בחלקים החלבוניים של הריבוזום הראו שפעילותו הקטליטית, כלומר יצירת הקשר הפפטידי, יכולה להתקיים בנוכחות תת-היחידה הגדולה בלבד וללא צורך בפקטורים נוספים למעט סובסטרטים מתאימים, אולם בקצב איטי בהרבה. לפי ממצאים אלו, ולפי עדויות גנטיות ומבניות נוספות, ניתן להסיק שהחלקים החלבוניים של הריבוזום מהווים תוספת אבולוציונית מאוחרת ומשמשים כמעין פיגום המסייע ליעילות תהליך התרגום ולהאצתו.
מנגנון הפעילות והמבנה של הריבוזומים שמור עבור כל האורגניזמים, אך קיימים מספר הבדלים קטנים בין המחלקות של הפרוקריוטיים והאיקריוטיים, המתבטאים בין השאר בגודלי התת-יחידות של הריבוזום. יחידת סוודרברג (על שם החוקר תאודור סוודברג) המשמשת ביוכימאים (המסומנת בסימול S), משמשת להגדרת גודלן של תת-היחידות של הריבוזום. יחידה זו מבטאת את קצב השיקוע של החומר בצנטריפוגה. בעוד שבפרוקריוטיים גודל הריבוזום כולו הוא 70S, המתחלק ל-30S שהיא תת-יחידה הקטנה ו-50S שהיא תת-יחידה הגדולה, באיקריוטיים הריבוזום כולו בגודל 80S המתחלק ל-60S ו-40S.
בפרוקריוטיים תת-היחידה הגדולה (50S) מורכבת מתת-יחידה 5S rRNA (אנ') (מורכב מ-120 נוקלאוטידים), תת-יחידה של 23S rRNA (אנ') (2,900 נוקלאוטידים) ו-34 חלבונים. תת-היחידה הקטנה (30S) מורכבת מתת-יחידה של rRNA בן 1,540 נוקלאוטידים (16S) הקשור ל-21 חלבונים. באיקריוטיים תת-היחידה הגדולה (60S) מורכבת מתת-יחידה 5S RNA (מורכב מ-120 נוקלאוטידים), 28S rRNA (אנ') (4,700 נוקלאוטידים), 5.8S rRNA (160 נוקלאוטידים) וכ-49 חלבונים. תת-היחידה הקטנה (40S) מורכבת תת-יחידה של 18S rRNA (אנ') (בן 1,900 נוקלאוטידים) וכ-33 חלבונים.
באאוקריוטים, בעוד שהריבוזומים בחלל התא הם מסוג 80S, הרי שהריבוזומים המצויים בכלורופלסטים ובמיטוכונדריה הם מן הדגם הפרוקריוטי של 70S. עובדה זו מחזקת את ההשערה שאברונים אלו מקורם מחיידקים קדמונים (על פי תאוריית האנדוסימביוזה) אשר חברו לתא האאוקריוטי והפכו לחלק ממנו.
ההבדלים במבני הריבוזומים בין איקריוטיים לפרוקריוטים מאפשרים פיתוח אנטיביוטיקות היכולות לפגוע בחיידקים ללא פגיעה בתאים של האדם החולה. בשל ההבדלים במבנים, הריבוזומים של החיידקים (70S) פגיעים לאנטיביוטיקות אלו, בעוד הריבוזומים של האיקריוטיים (80S) אינם פגיעים. אף על פי שבמיטוכונדריה יש ריבוזומים הדומים לאלו של חיידקים, המיטוכונדריה אינה נפגעת מאנטיביוטיקות אלו מאחר שהיא מוקפת ממברנה כפולה שלא מאפשרת מעבר קל של האנטיביוטיקות לאברון.
המבנה המולקולרי של הריבוזומים היה ידוע עוד משנות ה-70 של המאה ה-20. בתחילת שנות האלפיים הושגה הבנה של מבנה הריבוזומים ברזולוציות גבוהות, בסדר גודל של מספר אנגסטרומים (ככל שסדר הגודל קטן יותר, הרזולוציה גבוהה יותר) וכן הבנה של אופן הפעולה שלהם.
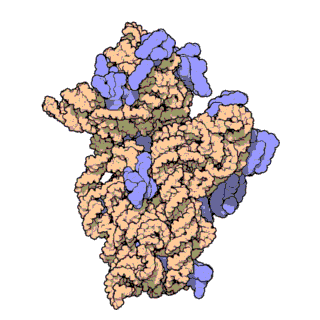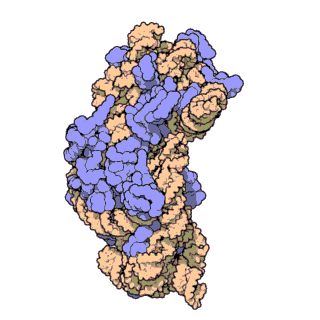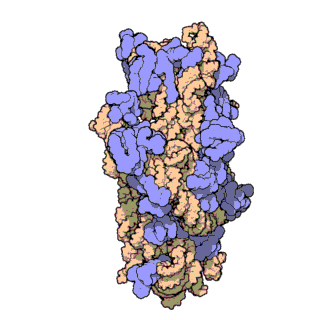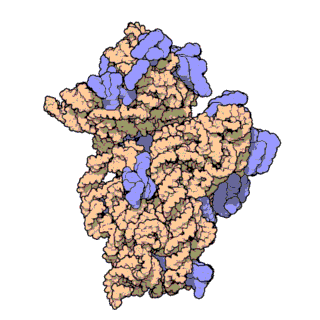
הפרסומים הראשונים בנגוע למבנה הריבוזומים ברמה המולקולרית התפרסמו בסוף 2000. ראשית התפרסם המבנה של תת-יחידה 50S של הארכאון Haloarcula marismortui[2]. מעט אחר כך התפרסם המבנה של תת-יחידה 30S של החיידק התרמופילי Thermus thermophilus[3]. זמן קצר לאחר מכן התפרסם מבנה מפורט יותר של תת-יחידה 30S[4]. על גילויים אלו זכו ונקטרמן רמאקרישנן מדוד גרשנבאום, תומאס סטייץ מאוניברסיטת ייל ועדה יונת ממכון ויצמן למדע בפרס נובל לכימיה בשנת 2009. במאי 2001 נפתר באמצעות קריסטלוגרפיה המבנה המלא של תת-יחידה 70S של החיידוק T. thermophilus ברזולוציה של 5.5 אנגסטרומים.
הריבוזומים החופשיים (Free Ribosomes) מצויים בציטופלזמה ובתוך אברוני המיטוכונדריה והכלורופלסט ומייצרים חלבונים שלרוב מיועדים להישאר בציטופלזמה או בתוך האברון המתאים.
ריבוזומים אחוזי קרום (Membrane Bound Ribosomes) נמצאים לרוב על גבי קרום אברוני הרשתית התוך-פלזמית (ER). הם מייצרים חלבונים ממברנליים – חלבונים החוצים את קרום התא או את קרום אחד האברונים. מחלקה נוספת של חלבונים שמסונתזים על ידי ריבוזומים אחוזי קרום הם חלבונים המופרשים מהתא דרך אקסוציטוזה (exocytosis). החלבון המסונתז על גבי ריבוזומים אחוזי ממברנה מוחדר לרוב בחלקו לתוך הרשתית התוך-פלזמית וכך נוצרים בו אזורים חודרי קרום – טרנסממברנליים.
כאשר יש צורך רב בתרגום, ניתן למצוא על גדיל mRNA כמה ריבוזומים המתרגמים בו זמנית, וכך נוצרים חלבונים רבים. למשל, ניתן למצוא פוליריבוזומים במח באזורי הסינפסה, ובמיוחד בהיפוקמפוס, הקשור ללמידה, שם נדרשים חלבונים רבים ליצירת Dendritic spine (אנ') חדשים המהווים את הקישור בין האקסון לדנדריט, ובעצם יוצרים בכך סינפסה[5].
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.