
აზოტმჟავა
ძლიერკოროზიული მინერალური მჟავა / From Wikipedia, the free encyclopedia
აზოტმჟავა,აზოტის სპირტი (HNO3) — ძლიერ კოროზიული მინერალური მჟავა.
| აზოტმჟავა | |
 | |
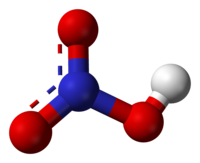 | |
 | |
| ზოგადი | |
|---|---|
| სისტემური სახელწოდება | აზოტმჟავა |
| ტრადიციული სახელწოდება | სამეფო წყალი, აზოტის სპირტი,Eau forte, წყალბადის ნიტრატი, Acidum nitricum |
| ფიზიკური თვისებები | |
| მდგომარეობა (სტ. პირ.) | უფერო, წითელი ან მუქი წითელი სითხე |
| სიმკვრივე | 1.5129 g cm−3 გ/სმ³ |
| თერმული თვისებები | |
| დნობის ტემპერატურა | -42 °C |
| დუღილის ტემპერატურა | 83 °C |
| თვითაალების ტემპერატურა | არააალებადი °C |
| ორთქლის წნევა | 48 mmHg (20 °C) |
| ქიმიური თვისებები | |
| ხსნადობა წყალში | განუსაზღვრელი გ/100 მლ |
| უსაფრთხოება | |
| NFPA 704 | |
| LD50 | 138 |
| კლასიფიკაცია | |
| CAS | 7697-37-2 |
| PubChem | 944 |
სუფთა სახით ნივთიერება უფეროა, მაგრამ ძველი ნიმუშები, როგორც წესი, ყვითელ შეფერილობას იღებენ, რაც ძირითადად მისი აზოტის ოქსიდებად და წყლად დაშლის გამო ხდება. კომერციულად ხელმისაწვდომი აზოტმჟავა მის 68% წყალხსნარს წარმოადგებს. როცა ხსნარი შეიცავს 86%ზე მეტ HNO3-ს, მას მბოლავი აზოტმჟავა ჰქვია. იმის მიხედვით, თუ რამდენი აზოტის დიოქსიდია მასში გახსნილი, მბოლავ აზოტმჟავას ეძახიან თეთრად მბოლავ აზოტმჟავას (WFNA) ან წითლად მბოლავ აზოტმჟავას (RFNA) (კონცენტრაცია 95%).
აზოტმჟავის ძირითადი გამოყენების სფეროა ნიტრირება — ნივთიერებისთვის (შეეხება ძირითადად ორგანული ნივთიერებებს) ნიტრო ჯგუფის დასამატებლად. ზოგიერთი მიღებული ნიტრო ნაერთები დარტყმა და თერმულად არასტაბილურია (ფეთქებადია), რამდენიმე მათგანი კი საკმაოდ მდგრადია სამხედრო და სამოქალაქო ამფეთქი ნივთიერებებისა და საღებავების საწარმოებლად. აზოტმჟავა ასევე გამოიყენება როგორც ძლიერი მჟანგავი.
