상위 질문
타임라인
채팅
관점
사이타라빈
위키백과, 무료 백과사전
Remove ads
사이타라빈(Cytarabine), 시타라빈, 사이토신 아라비노사이드 (ara-C)라고도 알려져 있으며, 화학요법제로 급성 골수성 백혈병 (AML), 급성 림프성 백혈병 (ALL), 만성 골수성 백혈병 (CML), 그리고 비호지킨 림프종을 치료하는 데 사용된다.[1] 정맥 주사 또는 피하 주사로 주사하거나 수막강내로 주사한다.[1] 지질소포 제형이 있으며, 이는 수막 침범 림프종에서 더 나은 결과를 가져올 수 있다는 예비 증거가 있다.[1]
흔한 부작용으로는 골수 억제, 구토, 설사, 간 문제, 발진, 구강 궤양 형성, 출혈 등이 있다.[1] 기타 심각한 부작용으로는 의식 상실, 폐 질환, 알레르기 반응이 있다.[1] 임신 중 사용은 태아에게 해를 끼칠 수 있다.[1] 사이타라빈은 항대사 물질과 뉴클레오사이드 유사체 계열 약물이다.[2] DNA 중합효소의 기능을 차단하여 작용한다.[1]
사이타라빈은 1960년에 특허를 받았고 1969년에 의료용으로 승인되었다.[3] 세계보건기구 필수 의약품 목록에 포함되어 있다.[4]
Remove ads
의학적 용도
사이타라빈은 주로 급성 골수성 백혈병, 급성 림프성 백혈병 (ALL) 및 림프종 치료에 사용되며,[5] 이곳에서는 유도 화학요법의 근간이 된다.
사이타라빈은 또한 항바이러스제 활성을 가지고 있으며, 전신성 헤르페스바이러스 감염 치료에 사용되어 왔다. 그러나 사이타라빈은 이 설정에서 그다지 선택적이지 않으며 골수 억제 및 기타 심각한 부작용을 유발한다. 따라서 ara-C는 독성 프로필로 인해 인간에게 유용한 항바이러스제가 아니다.[6]
사이타라빈은 또한 신경계 연구에서 배양에서 신경교 세포의 증식을 조절하는 데 사용되며, 신경교 세포의 양은 신경 세포에 중요한 영향을 미친다. 최근에는 사이타라빈이 NSC-34 운동 뉴런 유사 세포주에서 강건하고 지속적인 신경 분화를 촉진하는 것으로 보고되었다. 사이타라빈은 기계적 탈착 후 신경돌기 개시 및 재생을 위해 NSC-34 세포를 프라이밍하는 데 관용적이고 불필요하며 대부분 비가역적이다.[7]
Remove ads
부작용
사이타라빈의 고유한 독성 중 하나는 고용량 투여 시 소뇌 독성으로, 이는 운동실조로 이어질 수 있다. 사이타라빈은 과립구감소증 및 기타 신체 방어 기능 손상을 유발할 수 있으며, 이는 감염으로 이어질 수 있고, 혈소판감소증을 유발하여 출혈로 이어질 수 있다.
독성: 췌장염, 백혈구 감소증, 혈소판 감소증, 빈혈, 위장관 장애, 구내염, 결막염, 폐렴, 발열, 피부염, 손발바닥 홍반 이색증. 드물게 고용량 또는 빈번한 수막강내 Ara-C 투여 후 척수병증이 보고되었다.[8]
고용량 프로토콜에 사용될 때 사이타라빈은 뇌 및 소뇌 기능 장애, 안과 독성, 폐 독성, 심각한 위장관 궤양 및 말초신경병증 (드물게)을 유발할 수 있다.
부작용을 방지하고 치료 효율을 개선하기 위해 다양한 유도체 (아미노산, 펩타이드, 지방산 및 인산염 포함)가 평가되었으며, 다양한 전달 시스템도 평가되었다.[9]
Remove ads
작용 기전
요약
관점
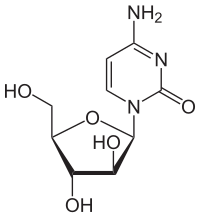
사이토신 아라비노사이드는 사이토신 염기와 아라비노스 당이 결합된 형태이다. 화학명은 1β-아라비노푸라노실사이토신인 항대사제이다. 유사한 화합물이 원래 발견된 특정 해면동물은 화학 방어를 위해 아라비노사이드 당을 사용한다.[10] 사이토신 아라비노사이드는 인간 데옥시사이토신과 충분히 유사하여 인간 DNA에 통합될 수 있지만, 세포를 죽일 만큼 충분히 다르다. 사이토신 아라비노사이드는 DNA 합성 과정을 방해한다. 그 작용 기전은 세포 주기가 S기 (DNA 합성)에 머무를 때 DNA를 손상시키는 사이토신 아라비노사이드 삼인산으로 빠르게 전환되기 때문이다. 따라서 체세포 분열을 위해 DNA 복제가 필요한 빠르게 분열하는 세포가 가장 큰 영향을 받는다. 사이토신 아라비노사이드는 또한 DNA[11] 및 RNA 중합효소와 DNA 합성에 필요한 뉴클레오타이드 환원효소도 억제한다. 사이타라빈은 뉴클레오사이드의 당 성분을 변경한 일련의 항암제 중 첫 번째이다. 다른 항암제는 염기를 변경한다.[12]
사이타라빈은 종종 지속적인 정맥 주입으로 투여되며, 이는 이중상 제거를 따른다. 즉, 초기 빠른 제거 속도와 그 이후의 느린 유사체 속도를 따른다.[13] 사이타라빈은 주로 hENT-1에 의해 세포로 운반된다.[14] 그런 다음 데옥시시티딘 키나아제에 의해 단일 인산화되어 결국 DNA 합성 중 DNA에 통합되는 활성 대사산물인 사이타라빈-5´-삼인산이 된다.
여러 저항 메커니즘이 보고되었다.[15] 사이타라빈은 혈청에서 시티딘 탈아미노효소에 의해 비활성 우라실 유도체로 빠르게 탈아미노화된다. 사이타라빈-5´-일인산은 데옥시시티딜레이트 탈아미노효소에 의해 탈아미노화되어 비활성 우리딘-5´-일인산 유사체가 된다.[16] 사이타라빈-5´-삼인산은 SAMHD1의 기질이다.[17] 또한 SAMHD1은 환자에서 사이타라빈 효능을 제한하는 것으로 밝혀졌다.[18]
항바이러스제로 사용될 때 사이타라빈-5´-삼인산은 바이러스 DNA 합성을 억제하여 작용한다.[19] 사이타라빈은 조직 배양 중 세포에서 헤르페스바이러스 및 백시니아 바이러스 복제를 억제할 수 있다. 그러나 사이타라빈 치료는 쥐 모델에서 헤르페스바이러스 감염에만 효과적이었다.
쥐에서 Ara-CTP (사이타라빈-5'-삼인산)는 문맥 공포 조절 이벤트의 장기 기억은 아니지만 단기 기억을 차단한다.[20] 기억 통합의 차단은 Ara-CTP가 DNA 비상동말단연결 경로를 억제하기 때문인 것으로 제안되었다.[20] 따라서 일시적인 DNA 파괴와 그 뒤를 잇는 비상동말단연결은 사건의 장기 기억 형성에 필요한 단계인 것으로 보인다.
역사
카리브해 해면 Cryptotheca crypta (현재 Tectitethya crypta)에서 아라비노스 함유 뉴클레오타이드를 분리하고 이러한 화합물이 DNA 합성 사슬 종결자 역할을 할 수 있다는 깨달음은 이러한 새로운 뉴클레오타이드를 잠재적인 항암 치료제로 탐구하게 만들었다.[21] 사이타라빈은 1959년 캘리포니아 대학교 버클리의 리처드 월윅, 월든 로버츠, 찰스 데커가 처음 합성했다.[22]
1969년 6월 미국 식품의약국의 승인을 받았으며, 처음에는 업존에서 Cytosar-U라는 브랜드 이름으로 미국에서 판매되었다.
이름
ara-C (아라비노푸라노실 시티딘)라고도 알려져 있다.[23]
- Cytosar-U
- Tarabine PFS (화이자)
- Depocyt (더 오래 지속되는 지질소포 제형)
- AraC
각주
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads