Fluorek rtęci(IV)
związek chemiczny / Z Wikipedii, wolnej encyclopedia
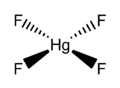
Fluorek rtęci(IV) (tetrafluorek rtęci), HgF
4 – nieorganiczny związek chemiczny z grupy fluorków, sól kwasu fluorowodorowego i rtęci na IV stopniu utlenienia, pierwszy znany związek rtęci(IV).
 |
Ten artykuł od 2017-04 zawiera treści, przy których brakuje odnośników do źródeł. |
| |||||||||||||||
| |||||||||||||||
| Ogólne informacje | |||||||||||||||
| Wzór sumaryczny |
HgF | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
276,58 g/mol | ||||||||||||||
| |||||||||||||||
| Podobne związki | |||||||||||||||
| Podobne związki | |||||||||||||||
| |||||||||||||||
Rtęć, podobnie jak inne pierwiastki grupy 12 układu okresowego (cynk i kadm), ma konfigurację elektronową s2d10 i zasadniczo tworzy wiązania z użyciem orbitalu s. Oznacza to, że najwyższy typowy stopień utlenienia rtęci w związkach wynosi II. Z tego powodu nierzadko prowadzi się spory co do słuszności zaliczania cynkowców do metali przejściowych.
Rozważania nad wyższymi stopniami utlenienia rtęci pojawiły się w latach siedemdziesiątych XX wieku, zaś przeprowadzone dwadzieścia lat później obliczenia wykazały, że związki rtęci(IV) o konfiguracji d8 i geometrii płaskokwadratowej mogą być trwałe w fazie gazowej. Doświadczalnie istnienie tego typu połączeń potwierdzono w 2007 roku, otrzymując HgF
4 na matrycy ze stałego neonu i argonu w temperaturze 4 K. Związek wykryto za pomocą spektroskopii w podczerwieni. Analiza w ramach między innymi teorii funkcjonału gęstości wskazuje, że w tworzenie wiązań zaangażowane są orbitale d. Rtęć zachowuje się więc tu jak typowy pierwiastek przejściowy. Niemniej, za W.B. Jensenem można powiedzieć, że warunki, w jakich istnieje HgF
4 daleko odbiegają od typowych warunków równowagowych i połączenie to powinno być traktowane raczej jako wyjątek.
Badania teoretyczne sugerują, że nietypowa w grupie 12 zdolność rtęci do tworzenia tetrafluorku wynika z relatywistycznej mechaniki kwantowej. Z obliczeń wynika, że dla „mniej relatywistycznych” (lżejszych) pierwiastków tej grupy, cynku i kadmu, tetrafluorki byłyby skrajnie niestabilne i rozpadałyby się do difluorków z eliminacją cząsteczki F
2. Z drugiej strony, tetrafluorek koperniku, powinien być stabilniejszy niż rtęci, lecz doświadczalne potwierdzenie takiej ewentualności spotyka się z problemem krótkiego czasu życia samego pierwiastka.