Лучшие вопросы
Таймлайн
Чат
Перспективы
Опиоиды
психоактивные химикалии Из Википедии, свободной энциклопедии
Remove ads
Опио́иды — вещества, способные связываться с опиоидными рецепторами организма, расположенными преимущественно в центральной нервной системе и желудочно-кишечном тракте. Опиоиды, обладающие структурным сходством с морфином, называют также опиа́тами[1], их молекулы имеют фенантреновую морфинановую основу.

Действие опиоидов на организм связывают с анальгетическим и седативным эффектами, угнетением дыхательного и кашлевого центров, ослаблением перистальтики кишечника. Опиоиды находят широкое применение в медицине в качестве мощных обезболивающих препаратов — опиоидных анальгетиков. Способность вызывать эйфорию обусловливает рекреационное использование опиоидов, которое может привести к зависимости и абстинентному синдрому.
Remove ads
История
Суммиров вкратце
Перспектива


Опиум применялся человеком ещё более 4000 лет назад[2]. В Минойской цивилизации почиталась богиня, увенчанная короной из коробочек опийного мака. Более поздние центры культивации опийного мака были обнаружены недалеко от Коринфа (современная Греция) и Афьона (современная Турция). Оттуда культивация мака распространилась на восток. До середины XVII века опиум применялся практически исключительно для обезболивания (в противоположность наркотическому применению)[3].
Курение опиума в рекреационных целях получило распространение в Китае во второй половине XVII века. С конца XVIII века Британская Ост-Индская компания, пользуясь монопольными привилегиями, ввозила огромные количества опиума в Китай, что впоследствии привело к Опиумным войнам[4].
В 1804 г. немецкий аптекарь Фридрих Сертюрнер впервые извлёк из опиума его основное действующее вещество, названное им «морфием» (современное название морфин было предложено Гей-Люссаком)[5]. В 1898 г. в медицинскую практику вошли этилморфин и героин, полусинтетические производные морфина[1]. Первый полностью синтетический опиоид, петидин (меперидин), был синтезирован в Германии в 1937 г., немного позднее был синтезирован метадон. В СССР использовалось производное петидина, тримеперидин (промедол)[6][7]. Фентанил был впервые синтезирован в Бельгии в конце 1950-х годов[8].
Remove ads
Строение

Опиоиды представляют собой класс препаратов разнообразной химической структуры. Наиболее распространённым структурным элементом опиоидов является бензольное кольцо, соединённое с атомом азота этильным или пропильным «мостиком». Эта структура придаёт опиоидам сходство с тирозином — аминокислотой, входящей в состав энкефалинов, простейших эндогенных опиоидных пептидов, и играющей важную роль в их взаимодействии с опиоидными рецепторами. Атом азота в структуре опиоидов, как правило, является частью пиперидинового кольца. Многие опиоиды являются третичными аминами[9][10].
Remove ads
Классификация
Суммиров вкратце
Перспектива
По действию
- Полные агонисты: трамадол, героин, гидроморфон, морфин, оксиморфон, метадон, меперидин, фентанил, алфентанил, суфентанил, ремифентанил, леворфанол;
- Частичные агонисты: кодеин, оксикодон, гидрокодон, пропоксифен, дифеноксилат;
- Агонисты-антагонисты смешанного действия: бупренорфин, нальбуфин, буторфанол, пентазоцин, налорфин (являются агонистами или частичными агонистами к одним типам опиоидных рецепторов и антагонистами к другим);
- Антагонисты: налоксон, налтрексон, налмефен.
По происхождению
- Растительного происхождения
- Алкалоиды опийного мака: морфин, кодеин, тебаин
- Другие природные опиоиды: митрагинин, сальвинорин А
- Полусинтетические
- Этилморфин, дигидроксикодеинон, гидроморфон, героин и др.
- Синтетические
- Эндогенные (вырабатываемые самим организмом)
- Энкефалин, эндорфин, динорфин, эндоморфин, ноцицептин.
По строению
Фенантрены
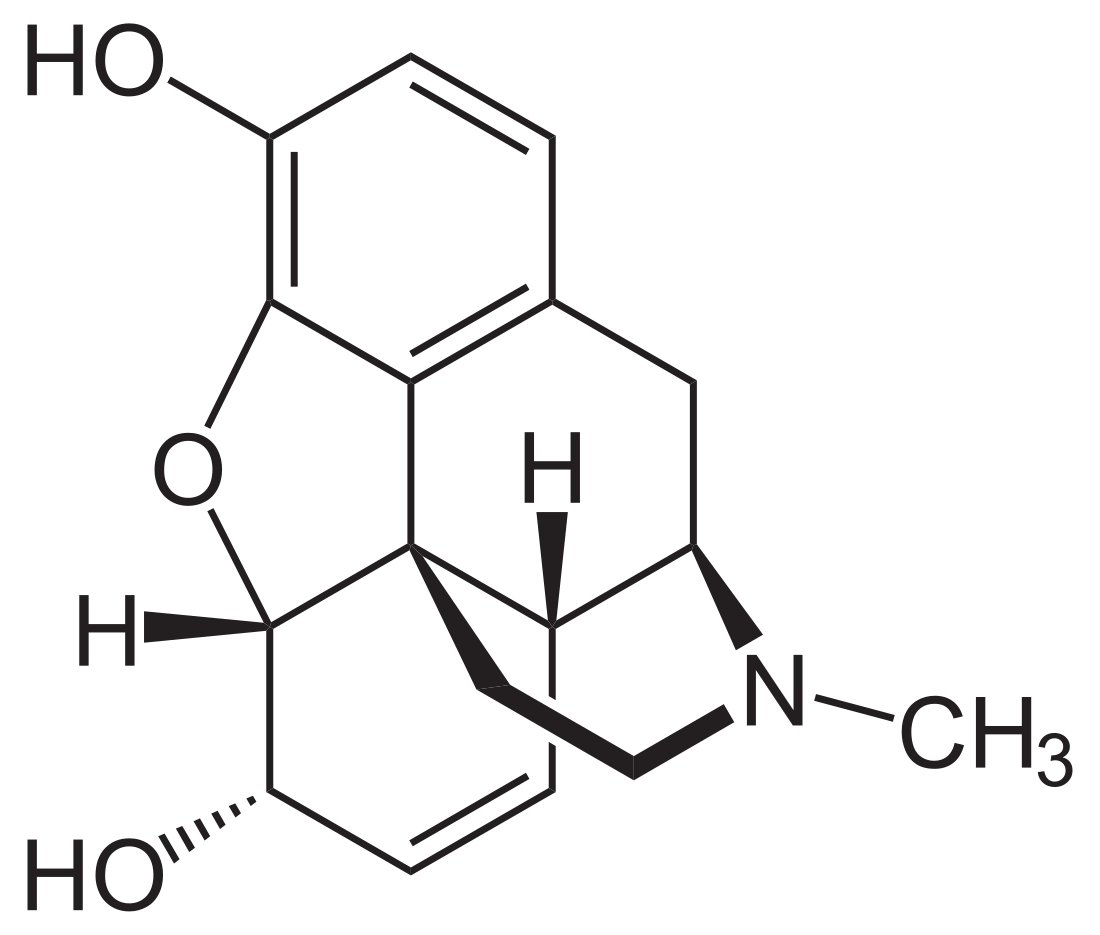
Фенантренами или 4,5α-эпоксиморфинанами называют группу природных и полусинтетических опиоидов (опиатов), близких по структуре к морфину[11][12]. Важнейшими структурными элементами морфина и других фенантреновых опиоидов являются ароматическое кольцо A и пиперидиновое кольцо D[9].
Размер группы замещения при атоме азота в морфиноподобных соединениях влияет на активность. Соединения с метильной группой при атоме азота, как правило, являются хорошими агонистами опиоидных рецепторов. Замена метильной группы на небольшие цепочки из 3-5 атомов углерода приводит к образованию опиоидных антагонистов, которые сохраняют сродство к опиоидным рецепторам, но не активируют их. Более крупные группы замещения при атоме азота могут возвращать соединению агонистические свойства: так, морфиноподобные соединения с фенилэтильной группой при атоме азота на порядок более активны, чем их соответствующие аналоги с метильной группой[9].
Гидроксильная группа при атоме C3 морфина также заметно влияет на свойства соединения. Замена её на метокси-группу приводит к образованию кодеина, очень слабого агониста μ-опиоидных рецепторов, 10 % которого метаболизируется в печени до морфина ферментом CYP2D6[13].
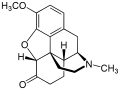
Изменения в кольце C могут приводить к получению соединений с увеличенной (по сравнению с морфином) активностью. Так, замена атома водорода в гидроксильной группе при C6 на метильную, этильную или ацетильную группы усиливает анальгезирующее действие соединения за счёт уменьшения поляризации молекулы, что делает её более липофильной и облегчает преодоление гемато-энцефалического барьера. Примером может являться 6-моноацетилморфин, активный метаболит героина. 6-кетоны гидроморфон и гидрокодон значительно более активны, чем морфин и кодеин соответственно[14][15].
Добавление гидроксильной группы при атоме C14 часто приводит к усилению действия соединения на μ-рецепторы, примерами чему являются оксикодон и оксиморфон. Модификация их структуры может приводить к образованию агонистов-антагонистов (нальбуфин) и антагонистов (налоксон, налтрексон). Реакция Дильса-Альдера с участием тебаина приводит к образованию производных 6,14-эндо-этенотетрагидротебаина, чаще называемых орипавинами. Примерами таких соединений являются эторфин и бупренорфин. Действие последнего в 20-30 раз сильнее, чем у морфина, при этом в отличие от морфина бупренорфин является частичным агонистом μ-рецепторов и антагонистом κ-рецепторов[14][16].
- 4,5α-эпоксиморфинаны (морфин и его производные)
Морфинаны
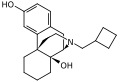
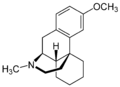
Структура морфинанов отличается от структуры морфина удалённым эпоксидным мостиком, образующим кольцо E. Несмотря на структурное сходство с морфином и его производными, получение морфинанов осуществляется посредством полного синтеза. Примером таких соединений являются леворфанол и буторфанол, более мощные, чем соответствующие производные морфина. Правовращающие изомеры, такие как декстрометорфан, не обладают опиоидной активностью[17][18].
Как и в случае производных морфина, замена N-метильной группы может приводить к образованию опиоидных антагонистов, а гидроксилирование в позиции 14 (как у буторфанола) усиливает действие соединения[19].
- Морфинаны
Бензоморфаны
6,7-бензоморфаны — соединения, содержащие только кольца A, B и D. Простейшие соединения такого типа — метазоцин (с метильной группой при атоме азота) и феназоцин (с фенилэтильной группой при атоме азота) являются агонистами μ-рецепторов. Напротив, аллильная и циклопропилметильная группы при атоме азота приводят к образованию смешанных агонистов-антагонистов (обычно проявляющих агонистические свойства по отношению к κ-рецептору и антагонистические по отношению к остальным). Примером таких соединений может служить пентазоцин — слабый агонист μ-рецепторов и агонист κ-рецепторов[20][21].
- Бензоморфаны
- Феназоцин
Фенилпиперидины
4-анилидопиперидины
Дифенилгептаноны
Remove ads
Синдром зависимости от опиоидов
Сроки возникновения психологической зависимости зависят от наркогенности препарата и способа его введения[22]. При употреблении медицинских препаратов, например морфина, зависимость возникает после 10—15 инъекций[22]. Героин — один из наиболее наркогенных опиоидов, зависимость от него возникает после 3—5 инъекций[22].
Физическая зависимость формируется позже, примерно после 4—6 недель систематического употребления опиоидов[23].
Remove ads
Побочные эффекты
Кратковременное нехроническое употребление опиодиов не связано с какой-либо физической или неврологической токсичностью. [источник не указан 127 дней]
Длительное употребление опиоидов вызывает гормональный дисбаланс как у мужчин, так и у женщин.[24] У мужчин вызванный опиоидами дефицит андрогенов приводит к аномально низкому уровню половых гормонов, в частности тестостерона.[25]
В педиатрии прогнозируемыми побочными эффектами приёма опиоидов является запор, зуд, тошнота и рвота. Последние три эффекта являются кратковременными и прекращаются через неделю, запор носит более постоянный характер. Поэтому приём опиоидов сопровождается приемом препаратов разжижающих стул и слабительных[26].
Remove ads
Литература
- Andrea M. Trescot et al. Opioid Pharmacology (недоступная ссылка — история) // Pain Physician. — 2008. — Т. 11, № 2S. — С. 133—153.
- Barash, Paul G. et al. Chapter 14. Opioids // Clinical Anesthesia, 5th Edition. — Lippincott Williams & Wilkins, 2006. — 1549 с. — ISBN 07817057452.
- Bertram G. Katzung. Chapter 31. Opioid Analgesics & Antagonists // Basic & clinical pharmacology. 11th edition. — McGraw-Hill Medical, 2009. — 1200 с. — ISBN 0071604057.
- David A. Williams, William O. Foye, Thomas L. Lemke. Chapter 19. Opioid Analgesics // Foye's principles of medicinal chemistry. 5th Edition. — Lippincott Williams & Wilkins, 2002. — 1114 с. — ISBN 0683307371.
Remove ads
Примечания
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads