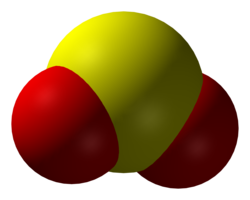
Sumpor dioksid
From Wikipedia, the free encyclopedia
Remove ads
Sumpor-dioksid (molekulska formula SO2) je bezbojni gas zagušljivog mirisa koji nastaje spaljivanjem sumpora na vazduhu. Teži je od vazduha. Rastvara se u vodi. Rastvor koji nastaje je kiseo jer gas reaguje sa vodom gradeći sumporastu kiselinu (H2SO3) čime se dokazuje da je sumpor-dioksid kiseli oksid. Sumporasta kiselina je nestabilna i lako se ponovo razlaže na sumpor-dioksid i na vodu.[7]
Rastvor sumpor-dioksida u vlažnoj okolini deluje kao izbeljivač tako što redukuje sastojke u materiji koja se izbeljuje.
Sumpor-dioksid je nusprodukt rada automobilskih motora i fabričkih postrojenja i zagađuje životnu sredinu. Napada sistem za disanje ljudi i životinja. Rastvarajući se u vazduhu uzrokuje kisele kiše koje uništavaju biljke, metalne konstrukcije i građevine.
Remove ads
Dobivanje
Sumpor dioksid se dobija izgaranjem sumpora s kisikom iz zraka:
- S + O2 → SO2
ili prženjem sulfidnih ruda, obično pirita:
- 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
Osobine
Pri običnoj temperaturi sumpor dioksid je gas, ali se može lako ukapljiti, zbog postojanja dipola u strukturi molekule.
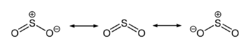
Sumpor dioksid ima neugodan miris i otrovan je za niže organizme, pa se upotrebljava za sterilizaciju suhog voća. U vinu služi kao antioksidans i antibiotik. Osim što sprječava njegovo kvarenje, služi i za održavanje odgovarajuće kiselosti. Sumpor dioksid ima redukciono djelovanje, jer može lahko preći u više oksidacijsko stanje. Ova osobina omogućava njegovo korištenje kao izbjeljivač. Sa vodom daje sulfitnu kiselinu, koja nije poznata u čistom stanju i postoji samo u vodenom rastvoru:
- SO2 + H2O → H2SO3
To je slaba kiselina i daje soli sulfite i hidrogensulfite. I sulfitna kiselina kao i sumpor dioksid ima redukciono djelovanje.
Remove ads
Reference
Vanjske veze
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads