Компактна нотација хемијских једињења From Wikipedia, the free encyclopedia
Хемијска формула или молекулска формула је формула која показује врсту и број атома који чине неки молекул. Молекулске формуле су ознаке хемијских једињења, облик приказивања њихових молекула; поред квалитативног састава, оне показују и квантитативни однос атома који сачињавају молекул хемијског једињења. Формуле се изражавају хемијским знацима; нпр. молекул хемијског једињења воде састављен је од два атома водоника и једног атома кисеоник, па је молекулска формула воде . Поред тога, молекулске формуле, на основу познатих атомских маса и валентности, показују однос маса атома који изграђују једињења (у овом случају 18 грама воде састоји се од 2 грама водоника и 16 грама кисеоника).


Молекулске формуле не показују унутрашњу структуру молекула, па се зато, нарочито у органској хемији, примењују рационалне формуле и структурне формуле. Рационалним формулама се, у ствари, скраћеним начином показује како су повезани атоми у молекулу нпр. молекулска формула етил-алкохола је , док ће његова рационална формула бити . Структурне хемијске формуле показују, поред квалитативног и квантитативног састава молекула једног хемијског једињења, још и начин на који су атоми и атомске групе у молекулима међусобно повезани. Структурна формула етил-алкохола изгледа овако:
Хемијска формула је један од начина представљања информација о хемијским пропорцијама атома који чине одређено хемијско једињење или молекул, користећи симболе хемијских елемената, бројеве, а понекад и друге симболе, попут уметања, цртица, заграда, зареза и знакова плус (+) и минус (–). Они су ограничени на једну типографску линију симбола, која може укључивати индексе и натписе. Хемијска формула није хемијски назив и не садржи речи. Иако хемијска формула може подразумевати одређене једноставне хемијске структуре, то није исто што и пуна хемијска структурна формула. Хемијске формуле могу у потпуности одредити структуру само најједноставнијих молекула и хемијских супстанци, и углавном су ограниченије снаге од хемијских имена и структурних формула.
Најједноставније врсте хемијских формула називају се емпиријске формуле, које користе слова и бројеве који означавају нумеричке пропорције атома сваке врсте. Молекулске формуле означавају једноставне бројеве сваке врсте атома у молекулу, без података о структури. На пример, емпиријска формула за глукозу је (двоструко више атома водоника од угљеника и кисеоника), док је његова молекулска формула.
Хемијска формула је запис састава хемијског једињења помоћу хемијских симбола. Хемијска формула може бити:
| Алуминијум сулфат има хемијску формулу . Облик алуминијум-сулфат хексадекахидрата је Al2(SO4)3·16 H2O. |
Хемијска формула је један од начина представљања информација о хемијским пропорцијама атома који чине одређено хемијско једињење или молекул, користећи симболе хемијских елемената, бројеве, а понекад и друге симболе, попут уметања, цртица, заграда, зареза и знакова плус (+) и минус (–). Они су ограничени на једну типографску линију симбола, која може укључивати индексе и натписе. Хемијска формула није хемијски назив и не садржи речи. Иако хемијска формула може подразумевати одређене једноставне хемијске структуре, то није исто што и пуна хемијска структурна формула. Хемијске формуле могу у потпуности одредити структуру само најједноставнијих молекула и хемијских супстанци, и углавном су ограниченије снаге хемијских имена и структурних формула.[1][2]
Најједноставније врсте хемијских формула називају се емпиријске формуле, које користе слова и бројеве који означавају нумеричке пропорције атома сваке врсте. Молекулске формуле означавају једноставне бројеве сваке врсте атома у молекулу, без података о структури. На пример, емпиријска формула за глукозу је (двоструко више атома водоника од угљеника и кисеоника), док је његова молекулска формула.
Тако нпр. формула означава молекул воде, која се састоји од двају атома водоника () и једног атома кисеоника (O).
| Једињење | Емпиријска формула | Молекулска формула | Сажета структурна формула | Структурна формула | Пројекцијска формула |
|---|---|---|---|---|---|
| Хлороводоник | HCl | HCl | HCl | HCl | |
| Ацетатна киселина | CH2O | C2H4O2 | CH3-CO-OH |  | |
| Етин | CH | C2H2 | HCΞCH | H-CΞC-H | |
| Бензен | CH | C6H6 | 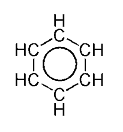 |  | |
| Етанол | C2H6O | C2H6O | CH3-CH2-OH |  | |
| Метоксиметан | C2H6O | C2H6O | CH3-O-CH3 |  | |
| Млечна киселина | CH2O | C3H6O3 | CH3-CH(OH)-COOH | 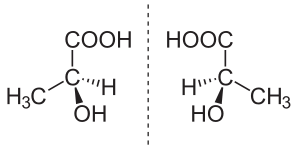 | |
| Глукоза | CH2O | C6H12O6 | HOCH2-[CH(OH)]4-CHO | 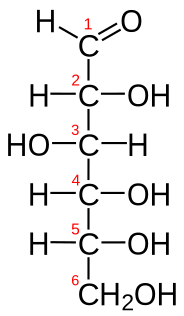 Fischerova Fischerova |  |
Формулску јединица је најмањи однос броја анјона и катјона у јонском једињењу који се приказује формулом једињења. Јонска материја је огроман скуп анјона и катјона који су повезани јонском везом (електростатском). У јонској материји наизменично су распоређени анјони и катјони, односно сваки анјон је окружен одређеним бројем катјона и обрнуто. Не постоји молекул јонског једињења већ је цело једињење један „велики молекул”. Зато формула јонског једињења има само најмањи однос броја анјона и катјона у једињењу, односно приказује формулску јединку. Формула 2 говори да се у калцијум хлориду катјони (2+) и анјони (–) налазе у односу 1:2 те је 2 формулска јединка калцијум хлорида.[3][4]
У најширем смислу свака формула представља формулску јединку.
Кристали хидратних соли имају у саставу везану кристалну воду. Формула једињења се пише, на пример: . Тачка у формули не представља знак множења већ је знак сабирања (плус). Вода је уклопљена у кристалну структуру једињења. Написана формула је сажети облик писања. Заправо формулу би правилније требало писати као: . Четири молекула воде се координирају с јоном бакра, док је пети молекул воде повезан са сулфатним јоном. Такође, заправо је . Угласте заграде у писању користе се за креирање формула комплексних једињења.
Формуле комплексних једињења, сажето се пишу као у претходним примерима, али најпризорније је формулу приказати „тродимензионо”.
Хемијске формуле разликују се према информацијама које пружају.
У било ком датом хемијском једињењу, елементи се увек међусобно комбинују у истој пропорцији. Ово је закон сталних односа маса.
Закон константног састава наводи да ће се у било ком одређеном хемијском једињењу сви узорци тог једињења састојати од истих елемената у истој пропорцији или односу. На пример, било који молекул воде се увек састоји од два атома водоника и једног атома кисеоника у односу 2: 1. Ако се погледају релативне масе кисеоника и водоника у молекулу воде, види се да 94% масе молекула воде чини кисеоник, а преосталих 6% је маса водоника. Ова масена пропорција биће иста за било који молекул воде.[5]
Алкен зван бут-2-ен има два изомера, које хемијска формула не идентификује. Релативни положај две метилне групе мора бити назначен додатним записом који означава да ли су метилне групе на истој страни двоструке везе ( или ) или на супротним странама једна од друге ( или ).[6]
Као што је горе поменуто, да би се представиле пуне структурне формуле многих сложених органских и неорганских једињења, могуће је да је потребна хемијска номенклатура која превазилази расположиве ресурсе који су горе коришћени у једноставним кондензованим формулама. Примери се могу видети у номенклатури органске хемије и номенклатури неорганске хемије 2005. Поред тога, линеарни системи именовања, попут Међународног хемијског идентификатора (), омогућавају рачунару да конструише структурну формулу, а поједностављени систем за линијски унос молекула (SMILES) омогућава унос читљивији човеку. Међутим, сви ови системи номенклатуре превазилазе стандарде хемијских формула, и технички су системи именовања хемикалија, а не системи формула.
За полимере у кондензованим хемијским формулама, заграде се постављају око јединице која се понавља. На пример, молекул угљоводоника који је описан као , молекул је са педесет понављајућих јединица. Ако је број понављајућих јединица непознат или променљив, слово се може користити за означавање ове формуле: .
За јоне, наелектрисање на одређеном атому може се означити натписом са десне стране. На пример, + или 2+. На овај начин може се приказати и укупан набој на наелектрисаном молекулу или полиатомском јону. На пример: или SO42−. Треба имати на уму да се + и - користе уместо +1 и -1.
За сложеније јоне, заграде [ ] се често користе за затварање јонске формуле, као у , која се налази у једињењима као што је ]. Заграде ( ) се могу угнездити у заграде да означе понављајућу јединицу, као у . Овде, указује да јон садржи шест група везаних за кобалт и [ ] обухвата целу формулу јона са наелектрисањем +3.
Ово је строго опционо; хемијска формула је важећа са или без информација о јонизацији, а хексаминкобалт() хлорид се може записати као или . Угаоне заграде се, попут заграда, понашају у хемији као у математици, групишући појмове - оне нису посебно примењени само за стања јонизације. У овом последњем случају, заграде указују на 6 група свих истог облика, везаних за другу групу величине 1 (атом кобалта), а затим је цео сноп, као група, везан за 3 атома хлора. У првом случају је јасније да је веза која повезује атоме хлоре јонска, а не ковалентна.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.