Cijanogen azid
From Wikipedia, the free encyclopedia
Remove ads
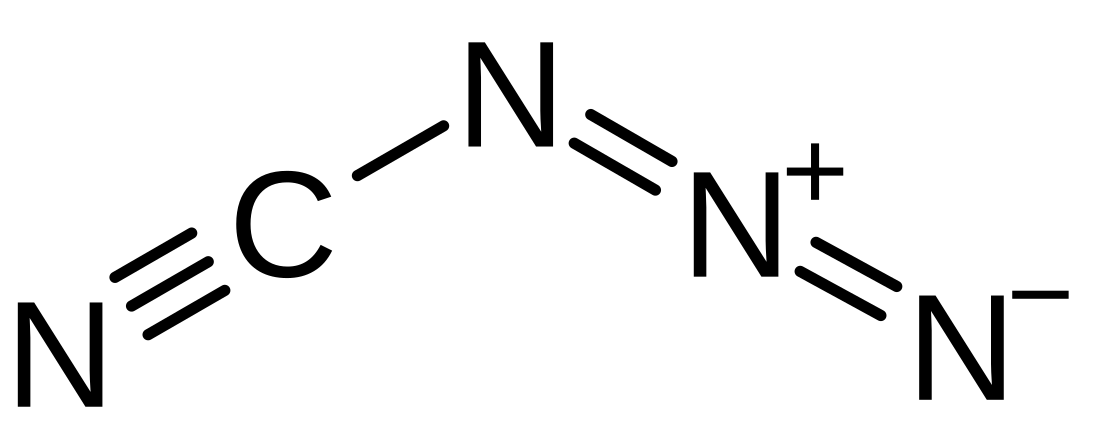
Cijanogen azid, N3CN ili CN4, je azidno jedinjenje ugljenika i azota koje je uljasta, bezbojna tečnost na sobnoj temperaturi. [7] To je veoma eksplozivna hemikalija koja je rastvorljiva u većini organskih rastvarača i sa kojom se normalno rukuje u razblaženom rastvoru u ovom obliku. [7][8][9] Prvi put ga je sintetizovao FD Marš u DuPontu ranih 1960-ih. [7][10] Postojale su ranije tvrdnje da je otkriveno kao kristalna čvrsta supstanca, koje su bile netačne. [11]
Cijanogen azid je primarni eksploziv, iako je previše nestabilan za praktičnu upotrebu kao eksploziv i izuzetno je opasan izvan razblaženog rastvora. [12][13] Njegova upotreba u hemiji bila je kao reagens pripremljen za upotrebu u sintezi hemikalija kao što su diaminotetrazoli, bilo u razblaženom rastvoru ili kao gas pod sniženim pritiskom. [14][15][16][11][17][18][19] Može se sintetizovati na temperaturi ispod sobne iz reakcije natrijum azida sa rastvorenim cijanogenim hloridom [7] ili cijanogen bromidom, [10] u rastvaraču kao što je acetonitril; ova reakcija mora biti obavljena pažljivo zbog proizvodnje nusproizvoda osetljivih na udarce. [10][17]
Remove ads
Ekstrakcija
Cianazid se može pripremiti reakcijom natrijum azida sa cijanogen hloridom ili cijanogen bromidom u nepolarnim rastvaračima kao što su acetonitril, etil acetat, metilen hlorid, toluen ili cikloheksan u temperaturnom opsegu između 10—25 °C (50—77 °F; 283—298 K). [4][5]
Nakon što se soli odvoje, jedinjenje se može dobiti destilacijom. Ovo se mora uraditi sa velikim oprezom zbog velike nestabilnosti jedinjenja ili ga treba izbegavati ako je moguća upotreba u rastvoru. [5]
Remove ads
Svojstva
Cijanazid je bezbojno ulje koje može da detonira izuzetno snažno pod blagim termičkim ili mehaničkim stresom. [20] Rukovanje u rastvoru je relativno bezbedno. Jedinjenje je rastvorljivo u većini organskih rastvarača i u vodi. U organskim rastvaračima, raspadanje se odvija sporo da bi se formirao azot. Poluživot 27% rastvora u acetonitrilu je 15 dana na 25 °C (77 °F; 298 K). Rastvori u acetonitrilu ili etil acetatu mogu se čuvati praktično neraspadnuti godinu dana na temperaturama između −20—0 °C (−4—32 °F; 253—273 K). Kada se zagreje na 40 °C (104 °F; 313 K)u vodi, dolazi do spore hidrolize do karbamazida. Natrijumova so 5-azido-1 H-tetrazola se polako formira u 10% rastvoru natrijum-hidroksida na sobnoj temperaturi. [4][5] Tokom pirolize u gasnoj fazi na 200 °C (392 °F; 473 K), azodikarbonitril se formira preko cijanonitrina kao međuproizvoda i eliminacije azota. [21]
Struktura jedinjenja u gasnoj fazi je ispitivana merenjem difrakcije elektrona u gasnoj fazi. Ugaoni molekul ima ugao veze između azido i cijano grupe od 114°. Na 175°, cijano grupa nije vezana sasvim linearno za azido azot. [22]
Remove ads
Upotreba
Jedinjenje reaguje sa zasićenim alkanima uz eliminaciju azota preko intermedijera cijanonitrena da bi se formirali alkilcijanamidi. Oni se mogu redukovati na odgovarajuće amine korišćenjem redukcionih agenasa kao što je litijum, aluminijum, hidrid. [23][24] Studije o n-heksanu, 2,3-Dimetilbutanu, 2,2-Dimetilbutanu, cikloheksanu, cikloheptanu i ciklooktanu su pokazale da se reaktivnost prema C-H vezama naglo povećava od primarnih ka tercijarnim strukturama. [23][24]

Cijanazid prolazi kroz reakcije cikloadicije sa alkenima, što može dovesti do aziridina i alkiliden cijanamida. Alkiliden cijanamidi se formiraju preko cikličnih triazolinskih intermedijera. Odnos proizvoda zavisi od strukture alkena. [6] Korišćenjem izobutana kao početnog alkena, proizvodi 2-butil cijanamid i N-cijano-2,2-dimetilaziridin nastaju u odnosu 1,4:1. [5][25] Sa drugim alkenima, kao što su eten, propen, 1-buten, dva izomera 2-butena, 2-metil-but-2-en, 2,3-dimetil-2-buten, 3,3-Dimetil-1-buten ili 2-heksen, slična reakcija je primećena sa preferencijom za alkiliden cijanamide kao proizvod. [25]

U slučaju ciklopentena, reakcija sa cikličnim alkenima skoro u potpunosti dovodi do odgovarajućeg imina cijanamida, koji se zatim može hidrolizovati u ciklopentanon. Nasuprot tome, sa norbornenom, aziridin je glavni proizvod. [25]

Kod cikloalkena sa trisupstituisanim dvostrukim vezama, redukcija prstena se takođe može primetiti, kao u primeru 1-metilcikloheksena da bi se dobio derivat ciklopentana. [25] U prisustvu litijum perhlorata, proširenje prstena do derivata cikloheptana može se postići u reakciji metilencikloheksana. [26][27]

U reakcijama na povišenim temperaturama, cijanonitren se formira kao intermedijer iz cijanamida uz eliminaciju azota. Ovo reaguje sa zasićenim ugljovodonicima i formira alkil cijanamide. [24] Sa benzenom je moguće proširenje prstena do cijanoazepina. Ova reakcija se takođe može izvesti sa toluenom, p-ksilelom, metil benzoatom, hlorobenzenom, fluorobenzenom, heksafluorobenzenom , trifluorometilbenzenom i benzotrihloridom sa visokim prinosom. [28]

Reakcija sa hidrazinom čini 1,5-Diamino-1H-Tetrazol dostupnim preko azidohidrazo intermedijera. [29]

Remove ads
Reference
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads


![{\displaystyle {\mathrm {NaN} {\vphantom {A}}_{\smash[{t}]{3}}{}+{}\mathrm {ClCN} {}\mathrel {\longrightarrow } {}\mathrm {N} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {CN} {}+{}\mathrm {NaCl} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/3b751cd1f727f8630603ec07574178b678a431fc)
![{\displaystyle {\mathrm {NaN} {\vphantom {A}}_{\smash[{t}]{3}}{}+{}\mathrm {BrCN} {}\mathrel {\longrightarrow } {}\mathrm {N} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {CN} {}+{}\mathrm {NaBr} }}](http://wikimedia.org/api/rest_v1/media/math/render/svg/5de9e0b16227c9b2e013041ed1f6ba9f009451d3)
![{\displaystyle {\mathrm {N} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {CN} {}\mathrel {\longrightarrow } {}\mathrm {NCN} {}+{}\mathrm {N} {\vphantom {A}}_{\smash[{t}]{2}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/36ea5ab0b24ce319f4063d2cd4b889d67ca80856)
![{\displaystyle {\mathrm {N} {\vphantom {A}}_{\smash[{t}]{3}}\mathrm {CN} {}+{}\mathrm {NCN} {}\mathrel {\longrightarrow } {}\mathrm {NC} {-}\mathrm {N} {=}\mathrm {N} {-}\mathrm {CN} {}+{}\mathrm {N} {\vphantom {A}}_{\smash[{t}]{2}}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/1ffb81d93758a400f99e0af061c0d0ec78b88fe3)