வேதிச் சேர்மம் From Wikipedia, the free encyclopedia
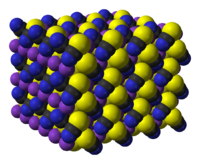
பொட்டாசியம் தயோசயனேட்டு (Potassium thiocyanate) KSCN என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படுகிறது. தயோசயனேட்டு எதிர்மின் அயனியின் முக்கியமான உப்பாகவும் போலி ஆலைடுகளில் ஒன்றாகவும் இது கருதப்படுகிறது. பெரும்பாலான கனிம உப்புகளைக் காட்டிலும் பொட்டாசியம் தயோசயனேட்டு மிகக்குறைவான உருகுநிலையைக் கொண்டுள்ளது.
 | |
| பெயர்கள் | |
|---|---|
| வேறு பெயர்கள்
பொட்டாசியம் சல்போசயனேட்டு பொட்டாசியம் ஐசோதயோசயனேட்டு பொட்டாசியம் தயோசயனைடு பொட்டாசியம் உரோதனைடு | |
| இனங்காட்டிகள் | |
| 333-20-0 | |
| ChEBI | CHEBI:30951 |
| ChemSpider | 9150 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 516872 |
| வே.ந.வி.ப எண் | XL1925000 |
| |
| UNII | TM7213864A |
| பண்புகள் | |
| KSCN | |
| வாய்ப்பாட்டு எடை | 97.181 கி மோல்−1 |
| தோற்றம் | நிறமற்றது. நீர் உறிஞ்சும் திறன் கொண்ட படிகங்கள் |
| மணம் | Odorless |
| அடர்த்தி | 1.886 கி/செ.மீ3 |
| உருகுநிலை | 173.2 °C (343.8 °F; 446.3 K) |
| கொதிநிலை | 500 °C (932 °F; 773 K) (சிதையும்) |
| 177 கி/100 மி.லி (0 °செல்சியசு) 217 கி/100 மி.லி (20 °செல்சியசு) | |
| கரைதிறன் | அசிட்டோன்: 21.0 கி/100 மி.லி எத்தனால்: கரையும் |
| −48.0•10−6 cm3/mol | |
| தீங்குகள் | |
| பொருள் பாதுகாப்பு குறிப்பு தாள் | ICSC 1088 |
| ஈயூ வகைப்பாடு | நச்சு (T) |
| R-சொற்றொடர்கள் | R20/21/22 R32 R52/53 |
| S-சொற்றொடர்கள் | (S2) S13 S61 |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose) |
854 மி.கி/கி.கி (வாய்வழி, எலி)[1] |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | பொட்டாசியம் சயனேட்டு பொட்டாசியம் சயனைடு |
| ஏனைய நேர் மின்அயனிகள் | சோடியம் தையோசயனேட்டு அமோனியம் தையோசயனேட்டு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
நீரிய பொட்டாசியம் தயோசயனேட்டு கிட்டத்தட்ட பருமன் அடிப்படையில் Pb(NO3)2 உடன் வினைபுரிந்து Pb(SCN)2, சேர்மத்தைக் கொடுக்கிறது. இந்த வினையில் உருவாகும் ஈயம்(II) தயோசயனேட்டைப் பயன்படுத்தி அசைல் குளோரைடுகளை ஐசோதயோசயனேட்டுகளாக மாற்ற முடியும். [2] மேலும் பொட்டாசியம் தயோசயனேட்டு எத்திலீன் கார்பனேட்டை எத்திலீன் சல்பைடாகவும் மாற்றுகிறது. [3] இச்செய்முறைக்காக பொட்டாசியம் தயோசயனேட்டு முதலில் நீர்நீக்கத்திற்காக வெற்றிடத்தில் உருக்கப்படுகிறது. இதேபோன்றதொரு வினையில் பொட்டாசியம் தயோசயனேட்டு வளையயெக்சீன் ஆக்சைடை தொடர்புடைய எபிசல்பைடாக மாற்றுகிறது. [4]
கார்பனைல் சல்பைடு தயாரிப்புச் செயல்முறையில் தொடக்க நிலை வினைபடுபொருளாக பொட்டாசியம் தயோசயனேட்டு பயன்படுத்தப்படுகிறது.
நீரிய பொட்டாசியம் தயோசயனேட்டு திரைப்படம் மற்றும் நாடகங்களில் எதார்த்தமான இரத்தம் போன்ற காட்சி விளைவுகளுக்கு பயன்படுத்தப்படுகிறது. ஒரு மேற்பரப்பில் வர்ணமாக இதைப் பூசலாம் அல்லது நிறமற்ற கரைசலாக வைத்துக் கொள்ளலாம். பெரிக் குளோரைடு கரைசலுடன் அல்லது இதையொத்த Fe3 அயனிகள் கொண்ட பிற கரைசல்களுடன் தொடர்பு கொள்ளும்போது வினையின் காரணமாக தயோசயனேட்டு இரும்பு அணைவு அயனி உருவாவதால் இரத்த சிவப்பு நிறக் கரைசல் தோன்றுகிறது.
ஆய்வகங்களில் இரும்பு(III) ((Fe3+) அயனியைக் கண்டுபிடிக்க உதவும் சோதனையில் பொட்டாசியம் தயோசயனேட்டு பயன்படுகிறது.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.