பெரிலியம் நைட்ரைடு
From Wikipedia, the free encyclopedia
Remove ads
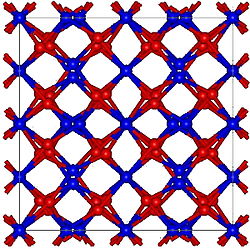
பெரிலியம் நைட்ரைடு (Beryllium nitride) என்பது Be3N2,என்ற மூலக்கூறு வாய்ப்பாடு கொண்ட பெரிலியம் தனிமத்தின் நைட்ரைடு உப்பு ஆகும். பகுதிப்பொருள்களாக உள்ள பெரிலியம் மற்றும் நைட்ரசன் தனிமங்களில் இருந்து உயர் வெப்பநிலையில் (1100 முதல் 1500 0 செ)[2] பெரிலியம் நைட்ரைடு தயாரிக்க முடியும். பெரிலியம் அசைடு போலில்லாமல் பெரிலியம் நைட்ரைடு வெற்றிடத்திலேயே சிதைவடைந்து பெரிலியம் மற்றும் நைட்ரசனைக் கொடுக்கிறது.[2] மேலும் இது விரைவாக நீராற்பகுப்பு அடைந்து பெரிலியம் ஐதராக்சைடு மற்றும் அமோனியாவைக்[2] கொடுக்கிறது. கனசதுர α-Be3N2 வடிவுடன் சிதைவுற்ற புளோரைட்டு எதிர் அமைப்பு மற்றும் அறுகோண β-Be3N2[2] ஆகிய பல்லுருத் தோற்றங்களில் பெரிலியம் நைட்ரைடு காணப்படுகிறது. 1800 முதல் 1900 0 செல்சியசு வெப்பநிலையில், அமோனியா வாயுப் பாய்ச்சலில் சிலிக்கான் நைட்ரைடுடன் (Si3N4 ) வினைபுரிந்து BeSiN2 சேர்மத்தைத் தருகிறது.[2]
Remove ads
தயாரிப்பு
700 முதல் 1400 0 செல்சியசு வெப்பநிலையில் பெரிலியம் உலோகத் தூளை ஆக்சிசனற்ற சூழலில் உலர் நைட்ரசனுடன் வினைபுரியச் செய்வதன் மூலம் பெரிலியம் நைட்ரைடைத் தயாரிக்கலாம்.
பயன்கள்
வெப்பந்தாங்கும் பீங்கான் தயாரிப்பில்[3], அணுக்கரு உலைகளில், மற்றும் கதிரியக்கக் கார்பன் – 14 உற்பத்தியில் பெரிலியம் நைட்ரைடு பெரிதும் பயன்படுகிறது.
வினைகள்
கனிம அமிலங்களுடன் பெரிலியம் நைட்ரைடு வினை புரிந்து அமோனியாவையும் அமிலத்துடன் தொடர்புடைய உப்புகளையும் உருவாக்குகிறது.
- Be3N2 + 6 HCl → 3 BeCl2 + 2 NH3
காரக் கரைசல்களுடன் வினைபுரியும் போது ஒரு பெரிலேட்டை உருவாக்கி அமோனியாவை வெளியேற்றுகிறது.
- Be3N2 + 6 NaOH → 3 Na2BeO2 + 2 NH3
அமிலங்கள் மற்றும் காரங்களுடன் வினைபுரியும் போது தீவிரத்துடனும் வேகத்துடனும் நடைபெறும் வினைகள் தண்ணீருடன் வினைபுரியும் போது மெதுவாக நிகழ்கிறது.
- Be3N2 + 6 H2O → 3 Be(OH)2 + 2 NH3
ஆக்சிசனேற்றிகளுடன் வினைபுரியும் போது வேதிவினையானது அதிதீவிரமாக நடைபெறுகிறது. 0 செல்சியசு வெப்பநிலையில் பெரிலியம் நைட்ரைடு காற்றில் ஆக்சிசனேற்றம் அடைகிறது.
மேற்கோள்கள்
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads