热门问题
时间线
聊天
视角
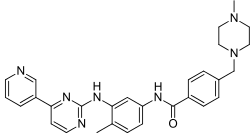
伊马替尼
化合物 来自维基百科,自由的百科全书
Remove ads
伊马替尼(INN:imatinib),商品名 Gleevec 及 Glivec,是一种酪胺酸激酶抑制剂,用于治疗慢性骨髓性白血病,胃肠道基质肿瘤等癌症,属于第一代/旧一代靶向药物。中文商品名为格列卫,港澳称为加以域,台湾称为基利克[1]。
伊马替尼由瑞士诺华公司研制销售,最早是使用在有费城染色体易位的慢性骨髓性白血病,后来逐渐被发现对多种癌症有疗效[8]。到2011年,该药已被美国FDA批准用于治疗10种不同癌症。对于慢性骨髓性白血病,位于第9和22对的染色体各自断裂一小段互换连接,造成骨髓细胞功能出现异常,大量制造不正常白血球,转位的染色体又称为“费城染色体”异常。伊马替尼可以有效地抑制费城染色体基因,使磷酸化反应无法被催化、染色体的功能丧失,从而抑制不正常的白血球增生。伊马替尼可与酪氨酸激酶活性位置结合,并阻止其活动。
通过伊马替尼及有类似作用机制的相关药物的开发,慢性粒细胞白血病患者的五年生存率提高近一倍,从1993年的31%,到2003年至2009年的59%(格列卫于2001年由美国食品药品监督管理局FDA批准)。相比以前的药物,伊马替尼副作用较小,让很多患者过上正常的生活。伊马替尼治疗患有胃肠道基质肿瘤平均存活接近5年,之前则是9至20个月。
伊马替尼使慢性颗粒性细胞白血病患者的十年生存率从以前的不到50%,增加到了现在的90%左右,并且绝大多数患者可以正常工作和生活。
伊马替尼是人类历史上第一个成功研制的小分子靶向药物。伊马替尼的开发者布莱恩·德鲁克尔、尼古拉斯·莱登获得了2009年美国拉斯克奖和2012年日本国际奖。
伊马替尼于2001年获美国批准用于医疗用途。[3]它已列入世界卫生组织基本药物标准清单之中。[9]英国自2017年起开始有通用名药物销售。[10]
Remove ads
医疗用途
美国食品药物管理局(FDA)已批准无论是在成人或儿童,伊马替尼作为一线治疗费城染色体阳性慢性骨髓性白血病/慢性粒细胞白血病的药物。这种药物被批准在多个费城染色体阳性CML病例,其中包括干细胞移植后,紧急爆发危机的,新诊断的。第一代的伊马替尼有多年临床数据,广为医生所用。新一代/第二代治疗药物有“达沙替尼”及“尼洛替尼”,医疗效果更为显著。
最新《欧洲白血病网络(ELN)治疗指引》显示:
- 治疗方案3个月, BCR-ABL 病变基因数量 ≤10%
- 治疗方案6个月, BCR-ABL 病变基因数量 <1%
- 治疗方案12个月, BCR-ABL 病变基因数量 ≤0.1%
- 治疗方案36个月, BCR-ABL 病变基因数量 ≤0.0032% (即MR 4.5水平)的百分比
如采用标靶治疗药物方案未能达标及出现副作用,应及早与医生讨论,改变治疗方案。
最新指引指出,若无法于三个月内达到指标,即可考虑转用新一代靶向药物例如尼洛替尼或达沙替尼作治疗。
Remove ads
2002年,美国FDA首次批准用于晚期GIST患者。2012年2月1日,伊马替尼被批准用于手术切除后KIT阳性肿瘤,以帮助防止复发。这种药物还批准用在不能手术切除的KIT阳性的GIST肿瘤。
美国食品药物管理局已批准伊马替尼用于治疗成人复发或难治性费城染色体阳性的急性淋巴细胞白血病(Ph+ ALL),骨髓增生异常/骨髓增殖性疾病与血小板衍生的生长因子受体基因重组相关联的,侵略性系统性肥大细胞增多症无或未知的D816Vc-KIT基因突变,增多综合征和/或慢性嗜酸粒细胞性白血病谁拥有FIP1L1-PDGFRα融合蛋白激酶(CHIC2等位基因缺失)或FIP1L1-PDGFRα融合蛋白激酶阴性或未知的,无法切除,复发和/或转移性隆突性皮肤纤维。2013年1月25日,格列卫被批准用于儿童费城染色体阳性的急性淋巴细胞白血病(Ph+ ALL),治疗进行性丛状神经纤维瘤相关的第一型神经纤维瘤病,早期研究表明潜在的伊马替尼用于使用所述的c-Kit酪氨酸激酶阻断特性。
副作用
使用后最常见的副作用有恶心、呕吐、腹泻、头痛、腿痛/痉挛、体液潴留、视觉障碍、瘙痒性皮疹、抵抗力下降、瘀伤或出血、食欲不振、[11]体重增加、血细胞数量减少(嗜中性白血球低下、血小板减少症、贫血)和水肿。[12]
报导指出某些人使用伊马替尼与发生左心室功能障碍有关联,有时甚至在没有先前心脏病的情况下发展为充血性心力衰竭。 伊马替尼的临床试验未报告心脏不良反应,但报告有显著高发的外周水肿案例,其中一些病例被归类为严重。[13] 患者活检化验以及接受大剂量伊马替尼的小鼠均表现出心脏毒性的细胞迹象。 心脏毒性作用似乎是由细胞质酪氨酸蛋白激酶ABL1受抑制所介导。[13]
多项针对人类和动物的研究表明如果青春期前的儿童使用伊马替尼,可能会延缓正常的生长(更具体说是骨骼伸长),但部分儿童在青春期可能出现至少部分的追赶性生长。[14]
导致这种副作用的原因尚不清楚,可能涉及到对生长激素(GH)相关途径的干扰(青春期前的生长依赖GH,而青春期生长则由GH和性激素协同促进)。[14]
使用伊马替尼可能会导致头发变浅/脱色或变深/重新著色(和其他一些酪氨酸激酶抑制剂的情况相似)和/或皮肤以及牙龈色素沉着过度。 头发颜色改变的中位发病时间为治疗开始后4周(但可能会在治疗开始后一年内发生),与使用剂量有关联,且在停药或减量后可逆。[15] 黑色素细胞表面表达的C-kit受体是伊马替尼的生物学靶点之一。[15]
禁忌症和注意事项
对伊马替尼过敏是唯一已知不能使用伊马替尼禁忌症。[16]使用伊马替尼需要谨慎的情况有:[17]
- 肝功能损伤
- 严重充血性心力衰竭或左心室功能障碍的风险,尤其是合并其他疾病的患者
- 怀孕(具胚胎-胎儿毒性风险)
- 体液潴留的风险
- 儿童或青少年生长发育迟缓的风险
过量
医界伊马替尼过量的临床经验有限。[18]治疗以支持疗法为主。[18]由于伊马替尼在血浆中高度蛋白结合,透析对去除伊马替可能无效。
作用机制


伊马替尼是2-苯基氨基嘧啶衍生物,其功能如同若干酪氨酸激酶的特异性抑制剂。它占据酪氨酸激酶(Tyrosine kinase,TK)活性部位,从而导致活性降低。有大量TK的酶在体内,包括胰岛素受体。伊马替尼特异于ABL(Abelson原癌基因)的激酶域,c-kit和PDGF-R(血小板衍生的生长因子受体)。慢性粒细胞白血病,费城染色体导致了ABL与BCR(断点簇区)的融合蛋白,称为BCR-ABL。由于这是现在一个组成型活性的酪氨酸激酶,伊马替尼用于减少BCR-ABL活性。酪氨酸的活性部位激酶各自具有一个结合位点的ATP。由酪氨酸激酶催化的酶的酶活性是所述末端磷酸从ATP转移至酪氨酸残基上的基片,称为蛋白酪氨酸磷酸化的一个过程。伊马替尼通过结合ATP上接近BCR-ABL结合位点而工作,锁死它以关闭或自抑制结构,因此抑制了酶的活性,该蛋白质的半竞争性。这一事实解释了为什么通过改变其平衡朝打开或活化其结构,许多BCR-ABL基因突变会导致抗伊马替尼。伊马替尼是相当有选择性的BCR-ABL-它也抑制上述其它目标(c-kit和PDGF-R)。
简单的说伊马替尼的作用机制是对特异性酪氨酸激酶的ATP结合位点的竞争性和选择性的封锁,
- 例如,B.Abl,Bcr-Abl,c-Kit和PDGF-Rezeptor。通过此阻断磷酸基团向基板转印。
为了生存,细胞需要通过蛋白质信号(讯息传递),让他们活着。一些蛋白质在此讯息传递中使用磷酸基团作为“开”的开关。此磷酸基团是由酪氨酸激酶酶化加入。在健康的细胞中,这些酪氨酸激酶的酶化,根据需要被接通或关闭。在费城染色体阳性慢性颗粒细胞白血病细胞中,一个酪氨酸激酶,BCR-ABL,被粘贴在“开”位置,并不断地加入磷酸基团。伊马替尼阻止这种BCR-ABL酶,并停止不断地加入磷酸基团。其结果是,这些细胞停止生长,甚至死亡。
由于BCR-ABL酪氨酸激酶的酶只存在于肿瘤细胞中,而不存在于正常细胞中,伊马替尼的工作原理,作为标靶治疗的一种形式,只有癌细胞通过伊马替尼药物而死亡。
在这方面,伊马替尼是癌症治疗中的第一个,显示这种标靶作用,而经常被援引作为研究癌症治疗的一个范例。
Remove ads
药物动力学
当给予伊马替尼经口服被迅速吸收,并且有非常高的生物可利用度(口服剂量的98%到达血液中)。伊马替尼的代谢发生在肝脏,借由几个同工酶的细胞色素P450系统的调节,包括在较小程度上和CYP3A4、CYP1A2,CYP2D6,CYP2C9、CYP2C19。其主要代谢产物“N去甲基哌嗪衍生物”,也很活跃。排除的主要途径是在胆汁和粪便;只有一小部分的药物在尿中排泄。大多数伊马替尼作为代谢产物被消除;只有25%以不变的型式被消除。伊马替尼及其主要代谢物各自的半衰期是18至40小时。
历史
伊马替尼于1990年代末由汽巴 - 嘉基的科学家(在1996年它与山德士合并成为诺华公司)发明,其主要由生物化学家尼古拉斯·莱登领导的团队(包括伊丽莎白·布奇丹格和于尔格·齐默尔曼,和用其开展临床实验治疗慢性粒细胞白血病的俄勒冈健康与科学大学的肿瘤学家德鲁克)驱动。
其他主要的贡献者包括医生和科学家卡洛斯·甘巴科尔蒂-帕瑟里尼、意大利米兰比可卡大学(于血液学方面)、英国伦敦哈默史密斯医院的约翰·戈德曼,及斯隆· 凯特琳癌症纪念中心的查尔斯·索耶斯;并最终在德鲁克医师率领下的临床试验确认其在慢性颗粒性白血病的疗效。
伊马替尼是通过合理的药物设计开发的。其后发现了费城染色体突变和过度活跃BCR-ABL蛋白,研究者筛选化学库找到一种药物,会抑制蛋白质。随着高效筛选,他们发现2-苯基氨基嘧啶。然后对这个配体进行了测试,并通过引入甲基和苯甲酰胺基的修饰以赋予它增强结合性能,从而产生伊马替尼。
药物合成

交互作用
因为伊马替尼主要由肝脏酶CYP3A4代谢,影响这种酶的活性的物质,会改变药物的血浆浓度(简称CYP3A4抑制剂)。一个例子酮康唑增加伊马替尼活性,因此有阻断CYP3A4的副作用,同样伊曲康唑、克拉霉素、氯霉素、利托那韦、奈法唑酮和柚子汁等等也是如此,相反的像利福平和圣约翰草降低了药物的活性,因此会冒着治疗失败的风险。伊马替尼还充当CYP3A4、2C9和2D6的抑制剂,增加了一些其它药物如辛伐他汀、环孢素、匹莫齐特、华法林、美托洛尔以及可能对乙酰氨基酚的血浆浓度。该药物通过未知的机理也减少左旋甲状腺素钠的血浆水平。就像其他的免疫抑制剂,施用活疫苗是禁忌。
社会与文化

有超过100位癌症专家于2013年在医学期刊《血液》上发表一封信,指出许多新型癌症药物(包括伊马替尼)的价格高得令人望而却步,让美国患者无力负担,且这类药物价格和利润水平之高已到不符道德标准的地步。 参与签署的人包括伊马替尼的研发者布莱恩·德鲁克尔、卡洛·甘巴科尔蒂-帕塞里尼和约翰·高曼。[21][22]他们提出伊马替尼参考当时的标准治疗药物 - 干扰素的价格来制定售价,于2001年的一年索价为30,000美元(相当于2023年的51,622美元),诺华制药以此价格将可在两年内收回其最初的开发成本。他们提起当伊马替尼无意间成为畅销药后,诺华制药在2012年更将一年用药价格提高到92,000美元(相当于2023年的122,098美元),当年公司该药物销售金额达到47亿美元。 也有其他医生同样对这种价格表示不满。[23][24][25]
根据一份分析报告,此药物到2016年的平均一年用药批发价已上升至120,000美元(相当于2023年的152,346美元)。 而竞争新药上市时的定价更高,诺华制药随之也提高其产品的价格。[26]
一项由必治妥施贵宝制药于2012年资助的经济分析估计中,提起接受伊马替尼治疗的患者可延长7.5年至17.5年的预期寿命。[27]
Gleevec100毫克片剂一片的国际价格为20至30美元之间,[28]其通用名药物(学名药)价格便宜,可低至每片仅2美元。[29]
诺华公司1998年在印度为伊马替尼的专利权提出了诉讼,当时印度已同意加入世界贸易组织(WTO),并应由与贸易有关的知识产权协定(TRIPS)协议下的全球知识产权标准做为约束。诺华公司打了七年有争议的法律战,并采取了各种方式,在各种的情况下向印度最高法院抗辩。[来源请求]
根据印度专利法,2005年之前,印度只对药物制造方法授予专利,而对药物本身的化学成分并不授予专利。因此,在其他国家取得专利的药物,印度公司可以通过其他生产方法生产较便宜的仿制版本。
根据世界贸易组织知识产权的有关条款,从2005年1月1日起,作为WTO成员国的印度应该结束过渡期,修改专利法,并开始给药品的化学成分授予专利。
印度专利法修改之后,诺华公司生产的抗癌药Gleevec(格列卫)在印度提出专利申请。然而,印度专利局于2006年1月拒绝了诺华的申请,理由是此药为"已知物质的新形式"。 [30][31]2006年5月,诺华就印度专利局的决议,向印度高等法院提出诉状,并对印度专利法提出异议,认为印度专利法违反了WTO知识产权的相关规定。
根据印度制药公司Cipla的报告,1998年该公司仿制生产的三种外国专利药的复合制剂,在3年内5次降价,成为南非、巴西、泰国等国进口药品的主要来源。目前[何时?],美国上市的17种抗艾滋病药品,均已被该公司仿制。
此案在发达国家也引起了高度关注。2007年1月23日,为了观察此案对国际社会的影响,欧洲议会就诺华诉印度政府一案举行听证会。来自不同政党的欧洲议会议员、诺华公司驻欧盟代表、欧洲仿制药企业联盟代表、国际医疗人道救援组织无国界医生、国际乐施会等组织的代表共40余人参加了听证。
听证会上,诺华提出自己的申诉理由,认为这是一个知识产权保护的问题,而不是药物可及性的问题。诺华可通过捐赠使患者得到格列卫。诺华称事实上,印度国内,在捐赠项目范围中的慢粒白血病患者,已经有99%的人获得免费的格列卫。诺华的捐赠项目已经为超过6600名印度患者和全球80个国家的19,000名患者提供了免费的格列卫。[32]
国际专利法允许一国在特殊情况下实行专利强制许可(Compulsory license),对这种药品进行仿制。
印度最高法院2013年判决维持印度专利局拒绝专利申请的决定。[33]
其他
2018年7月在中国大陆上映的电影《我不是药神》,电影改编自于2015年发生的陆勇案,片中虚构的药物“格列宁”即为伊马替尼。[34]
参考文献
外部链接
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads