热门问题
时间线
聊天
视角
呋喃
有机化合物 来自维基百科,自由的百科全书
Remove ads
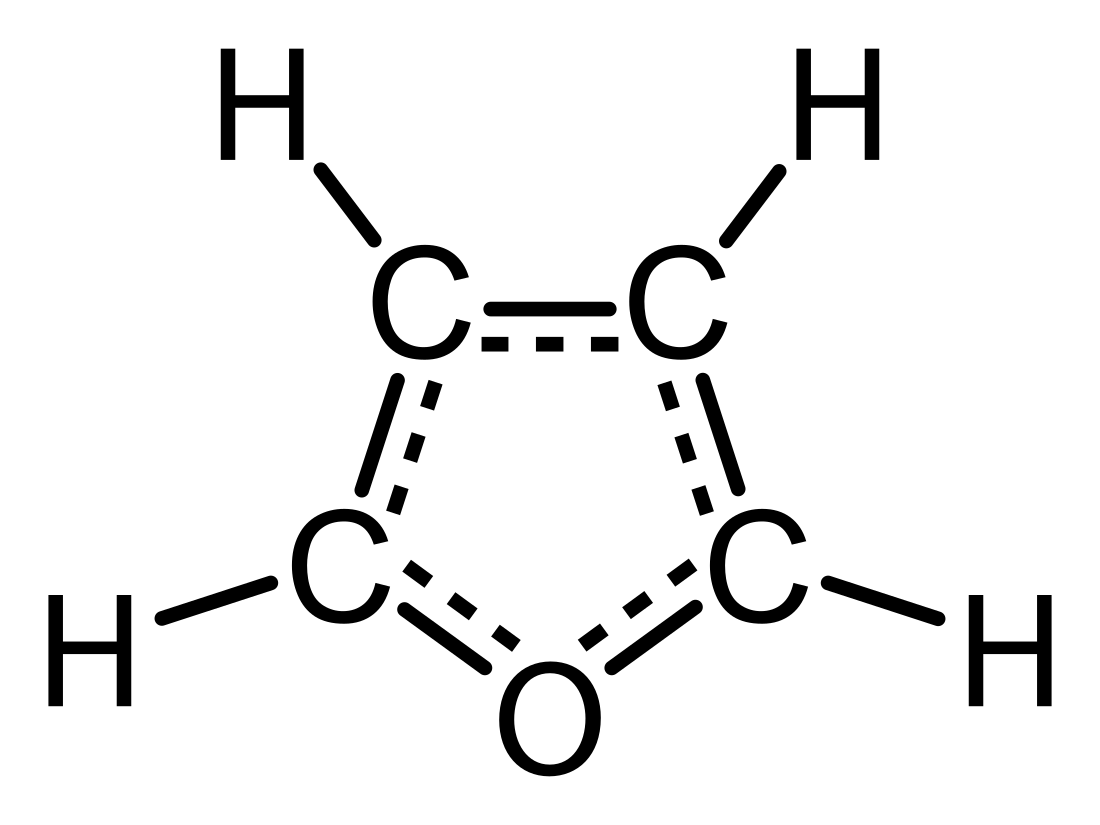
呋喃(英語:furan,IUPAC:oxole)[1],化學用名氧雜茂[2][3]或噁茂[需明示出處],是一種五元芳香性雜環有機物,其五元環含有四個碳原子、一個氧原子和兩個環內共軛雙鍵,並具有類似於苯環的6個π電子大共軛體系[4]。有呋喃環的化合物為其同系物。
呋喃是無色、可燃、易揮發液體,沸點接近室溫。呋喃有毒且為2B類可能致癌物質[5]。常作為合成其他複雜有機物的起始原料[6]。性質與苯相似,可由松木蒸餾得到,可溶於丙酮、醇、醚等多種常見有機溶劑,微溶於水。為多種重要工業化學品與藥物的前驅體,如常用作溶劑的四氫呋喃[7]。
Remove ads
歷史
「呋喃」的英文單詞furan來自拉丁文單詞furfur(米糠)。[8]1780年,卡爾·威廉·舍勒發現2-糠酸,是最先發現的呋喃衍生物;1831年,德貝萊納報道另一種重要衍生物糠醛;1870年,有德國化學家成功製備呋喃。[9][10]
製取
工業可由鈀催化糠醛脫羰基生產呋喃,或用氯化銅水溶液催化氧化1,3-丁二烯:[6]
實驗室中,可先將糠醛氧化為呋喃-2-甲酸,再脫羧成呋喃[11]。也可熱分解戊糖獲得;也可用固體纖維素,尤其松木。
Feist-Bénary合成是經典合成路線。帕爾-克諾爾合成用1,4-二酮與五氧化二磷反應,是簡單的方法。另外,回收噻吩的合成工藝中, 1,4-二酮和勞森試劑反應的副產品也可以得到呋喃。
化學性質
呋喃的氧原子有對孤對電子在共軛軌道平面形成大Π鍵,共軛平面共6粒電子,符合4n+2規則,是芳香物(見休克爾規則),「易取代難加成」。氧的另外一對孤對電子向外伸展。氧原子本身符合sp2雜化。
芳環使呋喃的化學行為不太似其它不飽和雜環。
參考文獻
外部連結
參見
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads