热门问题
时间线
聊天
视角
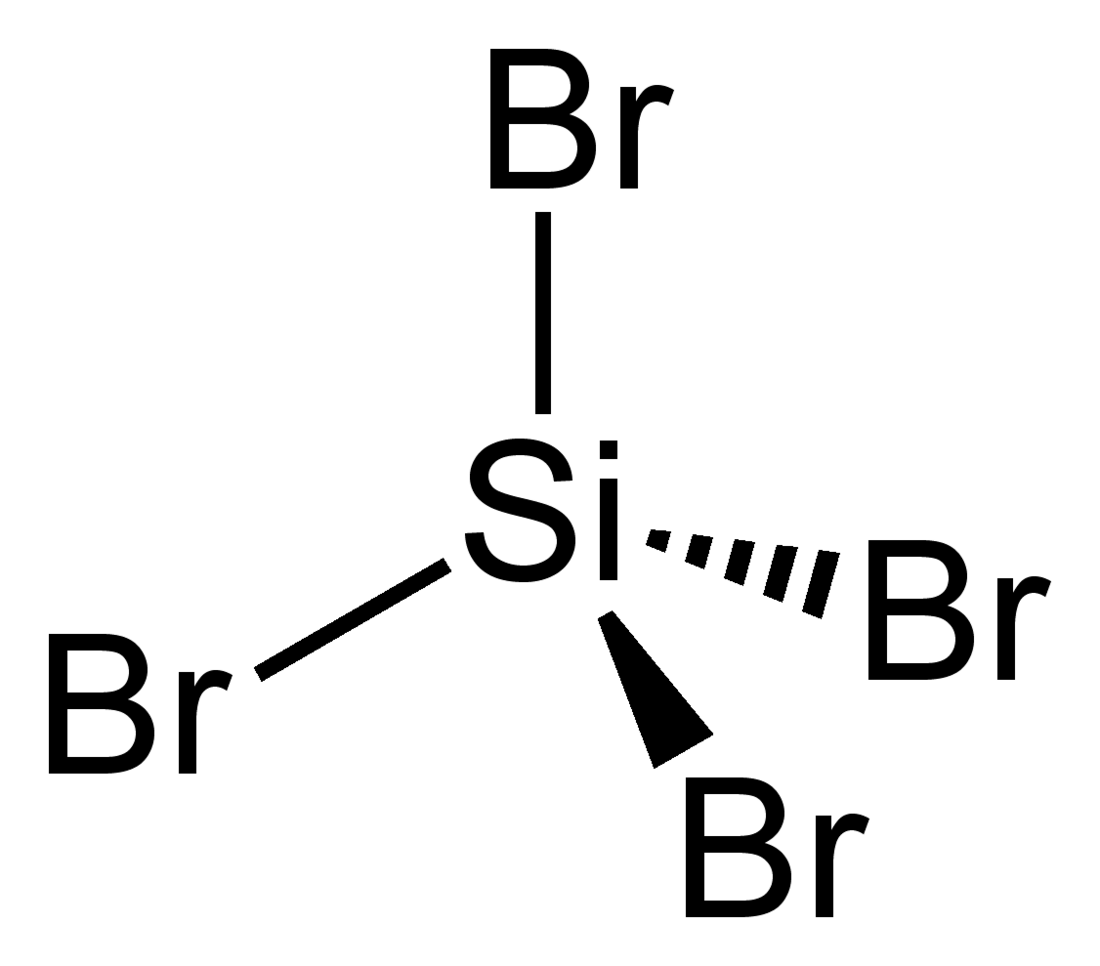
四溴化矽
化合物 来自维基百科,自由的百科全书
Remove ads
四溴化矽,又稱溴化矽,一種無機化合物。無色發煙液體,具強烈刺激性。暴露在空氣中變黃。[2]
Remove ads
性質
在空氣中很容易水解,生成二氧化矽和溴化氫。生成的溴化氫溶在空氣中的水裡形成酸霧,使得四溴化矽具有「發煙」現象。[1][3]
- SiBr4 + 2 H2O → SiO2 + 4 HBr
- SiBr4 + 4 ROH → Si(OR)4 + 4 HBr
- SiBr4 + 8 HNR2 → Si(NR2)4 + 4 HNR2·HBr
兩種不同的鹵化矽混合後加熱到合適的溫度,可以生成多種複合鹵化矽。[5]
- 2 SiBr4 + 2 SiCl4 → SiBr3Cl + 2 SiBr2Cl2 + SiBrCl3
- Si2Cl6 + Si2Br6 → Si2ClnBr6-n
四鹵化矽的性質會顯著地受當中的鹵素影響,其影響亦會在混合的鹵化物中出現。
四鹵化矽的熔點、沸點和鍵長會隨著其中鹵素的原子量增大而升高或變長,但鍵能則隨著其中鹵素原子量的增大而降低。
製備
- Si + 2Br2 → SiBr4
矽和溴化氫反應可以生成60%-70%的SiHBr3,同時生成四溴化矽和SiH2Br2。[8]
- Si + 3 HBr → SiHBr3 + H2
- Si + 4 HBr → SiBr4 + 2H2
- Si + 2 HBr → SiH2Br2
用途
參考文獻
外部連結
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads