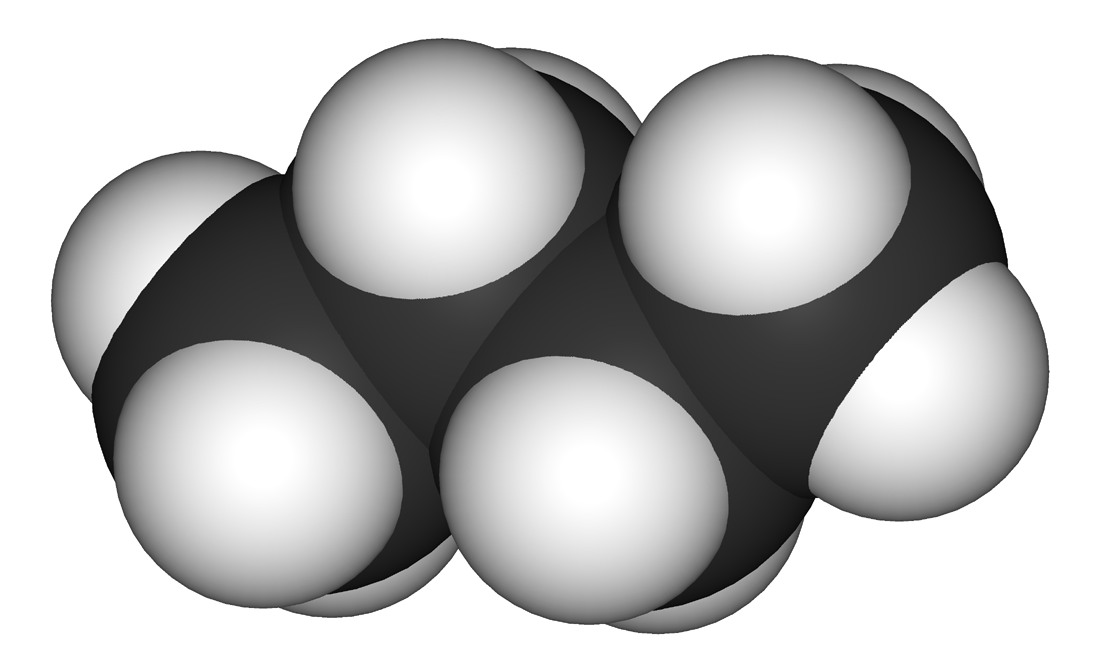
Butan
chemická sloučenina From Wikipedia, the free encyclopedia
Remove ads
Název butan se používá jako:
- systematický název pro nerozvětvený alkan se čtyřmi atomy uhlíku v molekule, (funkční vzorec CH3CH2CH2CH3), triviálním názvem n-butan
- společný název pro izomery alkanu se sumárním vzorcem C4H10; jsou dva a to n-butan a isobutan (triviální název), systematicky methylpropan (vzorec CH(CH3)3)
- označení směsi obou izomerů butanu
Tento článek je o obou izomerech butanu; infobox pak obsahuje informace pouze o nevětveném butanu; podrobnosti o isobutanu jsou uvedeny samostatně.
Oba butany jsou velmi hořlavé, bezbarvé, snadno zkapalnitelné plyny bez zápachu. Název butan je složen z částí but- podle acidum butyricum – latinského názvu pro kyselinu máselnou, karboxylovou kyselinu se stejným počtem atomů uhlíku v molekule a -an, přípony označující alkany.
Rotace okolo centrální chemické vazby C-C tvoří dvě konformace (trans a gauche)[2].
Remove ads
Reakce
Při dostatku kyslíku se butan spaluje na oxid uhličitý a vodní páru. Při nedostatku kyslíku může vznikat také uhlík (saze) a oxid uhelnatý.
- 2 C4H10 + 13 O2 → 8 CO2 + 10 H2O
n-butan je surovinou v DuPontově katalytickém procesu přípravy maleinanhydridu:
- 2 H3C-CH2-CH2-CH3 + 7 O2 → 2 C2H2(CO)2O + 8 H2O
n-butan, podobně jako všechny uhlovodíky, podléhá chloraci volnými radikály, kdy vznikají 1-chlor- a 2-chlorbutan, a dále i deriváty s vyšším počtem atomů chloru. Různá relativní míra chlorace je částečně vysvětlena odlišnými vazebnými disociačními energiemi, 425 a 411 kJ/mol u dvou typů C-H vazeb. Dva centrální atomy uhlíku mají mírně slabší vazby C-H.
- Struktura izomerů butanu
- n-butan
- isobutan
Remove ads
Použití

Butan se prodává v láhvích jako palivo pro vařiče a podobné účely. Směs butanu s propanem (a dalšími uhlovodíky) se komerčně nazývá propan-butan. Pro použití ve formě motorového paliva se však tato propan-butanová směs prodává pod zkratkou LPG.[3]
Butan je kromě toho v určité míře i složkou benzinu, surovinou pro výrobu základních petrochemikálií při parním krakování, používá se jako palivo v cigaretových zapalovačích a jako hnací plyn ve sprejích.
Velmi čisté formy, zvláště isobutanu, lze používat jako chladivo a ve značné míře tedy nahrazují halomethany nebezpečné pro ozónovou vrstvu, například v domácích chladničkách a mrazničkách. Hořlavost butanu není příliš velkým problémem, protože množství obsažené v zařízení není tak velké, aby vytvořilo výbušnou směs se vzduchem v místnosti. Operační tlak butanu je nižší než u halomethanů, například R-12, proto systémy s tímto plynem (např. automobilové klimatizace) nebudou při použití butanu fungovat optimálně.

Remove ads
Účinky na zdraví
Butan je prostý asfyxant a jeho toxické účinky jsou dány vytlačováním kyslíku. Nemá žádné přímé systémové účinky[4]. Inhalace butanu může způsobit euforii, ospalost, narkózu, asfyxii, srdeční arytmii a omrzliny. Může dojít i k smrti způsobené asfyxií a fibrilací komor.
Butan je nejčastěji zneužívanou těkavou látkou ve Velké Británii a v roce 2000 způsobil 52 % úmrtí „spjatých s rozpouštědly“[5]. Při vstřikování butanu přímo do krku se kapalina expanzí rychle ochlazuje na –20 °C a může způsobit prodloužený laryngospasmus[6]. Syndrom „náhlé čichačovy smrti“ (SSD), poprvé popsaný Bassem v roce 1970[7], je nejčastější prostou příčinou smrtí spjatých s rozpouštědly, tvoří 55 % známých smrtelných případů[6].
Odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads