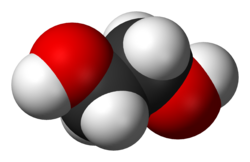
Ethylenglykol
chemická sloučenina From Wikipedia, the free encyclopedia
Remove ads
Ethylenglykol (psaný také jako etylenglykol; často též jen glykol), systematický název ethan-1,2-diol (nebo 1,2-ethandiol), v průmyslu známý také jako Fridex, je alkohol se dvěma -OH skupinami (diol), chemická sloučenina široce používaná v nemrznoucích chladicích kapalinách pro automobily. V čisté formě jde o viskózní jedovatou kapalinu sladké chuti, bez barvy a zápachu.
Remove ads
Výroba
Ethylenglykol se vyrábí z ethylenu přes ethylenoxid. Ethylenoxid reaguje s vodou za vzniku ethylenglykolu podle této chemické rovnice:
Tuto reakci lze katalyzovat kyselinami nebo zásadami, anebo může probíhat v neutrálním prostředí za zvýšené teploty. Nejvyšší zisk ethylenglykolu se dosáhne při kyselém nebo neutrálním pH s velkým přídavkem vody. Za těchto podmínek lze získat až 90 % ethylenglykolu (z teoreticky dosažitelného množství). Hlavními vedlejšími produkty jsou oligomery diethylenglykol, triethylenglykol a tetraethylenglykol.
Molekula ethylenglykolu byla zpozorována ve vesmíru.[2]
Ethylenglykol vzniká i biologickými procesy, jako odpadní produkt trávení polyethylenu larvou zavíječe voskového.[3][4]
Remove ads
Použití
Chladicí kapaliny

Hlavní použití ethylenglykolu je v chladicích kapalinách, například v automobilech a osobních počítačích. Díky nízkému bodu tuhnutí ho lze použít i jako odmrazovací kapalinu pro skla dopravních prostředků a pro letadla. Ethylenglykol se také často používá ve vodních okruzích klimatizačních systémů, a to buď v chladičích a vzduchových tepelných výměnících umístěných venku, anebo v systémech, kde je potřeba chladit pod bod tuhnutí vody.[5]
Zpomalování hydratace
Ethylenglykol se široce používá pro zpomalování tvorby klatrátů zemního plynu v dlouhých plynovodech, které vedou zemní plyn z plynových polí do zpracovatelského zařízení. Ethylenglykol lze z plynu získat zpět a znovu použít jako inhibitor, a to po čisticím procesu, kdy se odstraňuje voda a anorganické soli.
Průmysl
Ethylenglykol je čím dál důležitější pro výrobu plastů, zejména polyesterových vláken a pryskyřic, včetně polyethylentereftalátu používaného pro nápojové láhve. Schopnost ethylenglykolu fungovat jako nemrznoucí kapalina ho činí důležitou složkou vitrifikačních směsí pro nízkoteplotní uchovávání biologických tkání a orgánů.
Menší množství ethylenglykolu se využívá pro výrobu kondenzátorů, jako meziprodukt pro výrobu 1,4-dioxanu a jako antikorozní aditivum do kapalinových chladicích systémů osobních počítačů.
Chemická výroba
Ethylenglykol lze použít také v organické syntéze jako chránicí skupinu pro karbonylové skupiny. Reakce ketonu nebo aldehydu s ethylenglykolem poskytuje, za přítomnosti kyselého katalyzátoru (např. kyselina p-toluensulfonová, BF3·Et2O), cyklický acetal (2-alkyl 1,3-dioxolan), který je odolný proti zásadám a jiným nukleofilům. Chránicí skupina 1,3-dioxolanu může být následně odstraněna, například další kyselou hydrolýzou.[6] V následujícím příkladu je izoforon chráněn pomocí ethylenglykolu s mírným přídavkem kyseliny p-toluensulfonové. Aby se rovnováha reakce posunula na pravou stranu, byla azeotropickou destilací odstraněna voda[7].

Geotermální systémy
Ethylenglykol se často používá v geotermálních topných/chladicích systémech. Ethylenglykol je zde médiem, které proudí smyčkami potrubí geotermálních systémů a přenáší teplo přes geotermální tepelné čerpadlo. Ethylenglykol získává energii ze zdroje (jezero, oceán, studna) nebo ji naopak odevzdává, v závislosti na tom, zda systém topí nebo chladí.
Laboratorní použití
Ethylenglykol často nachází využití v laboratořích pro vysrážení bílkovin v roztocích. To je obvyklým předstupněm frakcinace, purifikace a/nebo krystalizace. Lze ho také použít pro ochranu funkčních skupin, aby nebyly zreagovány během organické syntézy. Funkční skupina v původním složení se získá jednoduše přidáním vody a kyseliny.
Ethylenglykol se běžně používá pro uchovávání preparátů ve školách, často při pitvách. Dá se říct, že je bezpečnější než formaldehyd, ale tato bezpečnost je sporná.[zdroj?]
Jiná použití
Vysoká teplota varu ethylenglykolu a jeho afinita k vodě z něj činí ideální desikant při zpracování zemního plynu. Nadbytek vodní páry se na plynových polích obvykle odstraňuje glykolovou dehydratací. Ethylenglykol stéká dolů z vrcholu věže a je ve styku se směsí vodní páry a uhlovodíkových plynů stoupající odspodu. Glykol chemicky odstraňuje vodní páru a zajišťuje tak, že na vrcholu věže odchází suchý plyn. Glykol a voda se pak oddělují a glykol se vrací zpět do věže.
Kromě odstraňování vody může ethylenglykol také snížit teplotu, při které se tvoří hydráty. Čistota glykolu používaného pro potlačení hydratace (monoethylenglykol) je typicky okolo 80 %, přičemž glykol používaný pro dehydrataci (triethylenglykol) je typicky 95–99%. Navíc vstřikované množství pro potlačení hydratace je mnohem menší než množství obíhající v glykolových dehydratačních věžích.
Ethylenglykol lze používat také při výrobě některých vakcín, byť sám pak není přítomen v injekcích.[zdroj?] Bývá v malém množství (1–2 %) přidáván do leštidel na boty a do některých inkoustů a barviv. Ethylenglykol se někdy používal i pro ošetření dřeva proti hnilobě a houbám, jak preventivně, tak pro likvidaci napadení. V několika případech byl použit k ošetření částečně shnilých dřevěných předmětů, aby mohly být vystaveny v muzeích. Je jeden z mála úspěšných prostředků proti hnilobě dřevěných lodí, a je relativně levný. Ethylenglykol může být i jednou z přísad do roztoků k čistění obrazovek, společně s hlavní součástí isopropylalkoholem.
Remove ads
Toxicita
Hlavní nebezpečí ethylenglykolu je při požití. Kvůli své sladké chuti ho někdy děti a zvířata požijí velké dávky, dostanou-li se k nemrznoucím směsím. Smrtelná dávka je udávána mezi 0,8 až 1,7 g/kg, případ úmrtí je zaznamenán i pod 0,5 g/kg, naopak přežití i pro dávky řádově vyšší.[8][9]
Při požití se příznaky otravy projevují ve třech krocích, počínaje zvracením, pak nastane metabolická acidóza a kardiovaskulární poruchy, a nakonec akutní selhání ledvin. Hlavní příčinou toxicity není ethylenglykol samotný, nýbrž jeho metabolity. Nejpodstatnějšími metabolity způsobujícími toxicitu jsou kyseliny glykolová a šťavelová.
Klinickou diagnózu otravy lze nejspolehlivěji provést měřením ethylenglykolu v krvi. Avšak mnoho nemocnic nemá možnost provést tento test a musí se při diagnóze spoléhat na abnormality v biochemii organismu. Diagnóze může pomoci také rozbor moči na přítomnost krystalů šťavelanu vápenatého. Léčba spočívá v počáteční stabilizaci pacienta a následném použití antidot. Mezi používaná antidota patří ethanol a fomepizol. Antidota účinkují blokací enzymu odpovědného za metabolizaci ethylenglykolu a proto mohou zastavit rozvoj otravy. Pro lepší odstraňování ethylenglykolu a jeho metabolitů z krve lze také použít hemodialýzu. Jakmile se provádí léčba, je prognóza obecně dobrá a většina pacientů se zcela uzdraví.
Otrava je poměrně častá kvůli sladké chuti ethylenglykolu. Proto se v rámci prevence do nemrznoucích kapalin přidává denatonium-benzoát, který má hořkou chuť.
V České republice se staly mediálně známými dva případy žen, které se pokusily otrávit své dcery přidáním nemrznoucí směsi pod obchodním názvem Fridex do potravin a nápojů. V jednom případě bylo prokázáno, že matka nechala dítě záměrně několik hodin bez lékařské pomoci a sledovala jak trpí silnými bolestmi. Obě děti otravu přežily, ovšem musely být ve vážném stavu dlouhodobě hospitalizovány a utrpěly trvalé poškození organismu. Obě matky byly odsouzeny za pokus o vraždu k nepodmíněným trestům.[10][11]
První pomoc: Při požití Fridexu se doporučuje podat otrávenému větší množství tvrdého alkoholu (např. vodky), tím utlumíme metabolismus ethylenglykolu, protože tělo bude přednostně odbourávat ethanol z vodky. Pozor ale na sekundární otravu ethanolem!
Remove ads
Průmyslová rizika
Ethylenglykol se začíná rozpadat při 110–120 °C.[chybí zdroj][rozpor] Je potřeba si uvědomit, že rozpad začíná v situaci, kdy celková (průměrná) teplota je pod tímto limitem, protože povrchové teploty v tepelných výměnících a ohřívačích se mohou místně snadno dostat nad uvedené hodnoty.
Elektrolýza roztoků ethylenglykolu se stříbrnou anodou vede na exotermickou reakci. U katastrofálního požáru Apolla 1 byla jako jedna z možných příčin dovozena taková reakce chladiva složeného z ethylenglykolu a vody. Směs ethylenglykolu a vody se může v nízkotlaké atmosféře čistého kyslíku vznítit a hořet.
Remove ads
Reference
Externí odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads