Massefylde
Matematisk mængdeenhed From Wikipedia, the free encyclopedia
Remove ads
Massefylde er forholdet mellem et stofs masse og dets rumfang. Massefylde er altså masse per rumfang. En liter vand har større tæthed end en liter luft og dermed større massefylde. Massefylde omtales også som densitet eller massetæthed. Vægtfylde er en ældre betegnelse, som dog stadig er i almindelig brug uden for fagkredse, og rumvægt anvendes udelukkende som kornmål. Massefylde betegnes med det græske bogstav (rho).



Massefylden er både temperatur- og trykafhængig.[1] Trykafhængigheden er typisk ret lille for faste stoffer og væsker, og langt mere udtalt for gasser. De fleste stoffers massefylde falder typisk, når temperaturen stiger, da stoffer typisk udvider sig ved opvarmning og trækker sig sammen ved afkøling, uden at massen ændres (for vand gælder dette dog kun for temperaturer over ca. 4 °C). Tilsvarende stiger massefylden typisk, når trykket stiger.[1] For gassers vedkommende gælder, at ideale gassers volumen er eksakt proportional med produktet af tryk og temperatur, og for andre gasser tilnærmelsesvis.[1] Da et stofs massefylde altså afhænger af temperatur og tryk, bør man derfor også altid angive, ved hvilken temperatur og hvilket tryk, en given massefylde er målt.
Tidligere benyttede man et aræometer til at måle massefylden.
Remove ads
Beregning
Rumfang kaldes også volumen og måles i liter, kubikmeter eller en anden enhed til måling af rumfang.
Masse måles i gram, kilogram eller en anden enheder til at måle masse.
For at beregne massefylden benyttes følgende formel:
- Rumfang/volumen betegnes som V
- Masse betegnes som m
- Massefylde betegnes som
Ved større mængder angives massefylden typisk i kg/m3, og ved mindre mængder i g/cm3; 1 kg/m3 svarer til 1000 g/cm3.
Remove ads
Arkimedes
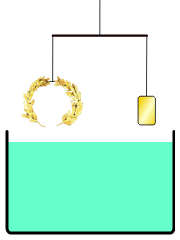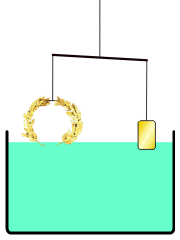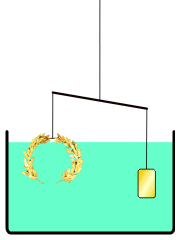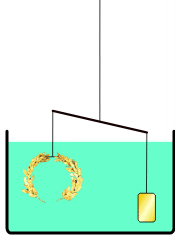
Hvis et stofs massefylde er mindre end en væskes massefylde, kan stoffet flyde på væskeoverfladen. Hvis stoffet har en større massefylde, synker det ned i bunden af væsken. Der ses bort fra væskens overfladespænding. Denne opdrift kaldes Arkimedes' princip efter den græske matematiker og fysiker Arkimedes.
Arkimedes skulle finde ud af, hvor meget guld der var i kong Hieron 2's kongekrone. Kongen mistænkte guldsmeden for at snyde ved at kun benytte halvdelen af det guld, han havde fået af kongen, og bruge sølv for resten. Hvis man kunne bestemme densiteten, ville det være muligt at afgøre, om der var sølv i kongekronen, fordi sølv er lettere end guld. Imidlertid kan massefylden ikke alene findes ved vejning. Man er nødt til også at kende rumfanget. Historien fortæller, at Arkimedes fandt løsningen, mens han var i bad. Hvis han sænkede kongekronen ned i badekarret, skulle mængden af vand stige. Rumfanget af kongekronen ville da være lig med rumfanget af stigningen. Således ville han kunne beregne massefylden af kongekronen som vægten divideret med rumfanget. Da sølv har en mindre massefylde end guld, lykkedes det Arkimedes at vise, at guldsmeden havde snydt kongen.
En anden måde at gøre det på er at balancere kongekronen og rent guld på en vægt. Ved nedsænkning i vand vil der være en større opdrift på kongekronen, hvis der er blandet sølv i (se billedet). Denne erkendelse førte til formuleringen af Arkimedes' lov: Når et legeme sænkes ned i vandet, taber det lige så meget i vægt, som den fortrængte væske vejer (Arkimedes' lov, formuleret omkring 250 f.kr.).
Remove ads
Forskellige stoffers massefylde og ydergrænser
Sorteret efter stoftype og dernæst massefylde:
Remove ads
Se også
Kilder, referencer og eksterne henvisninger
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads



