Top-Fragen
Zeitleiste
Chat
Kontext
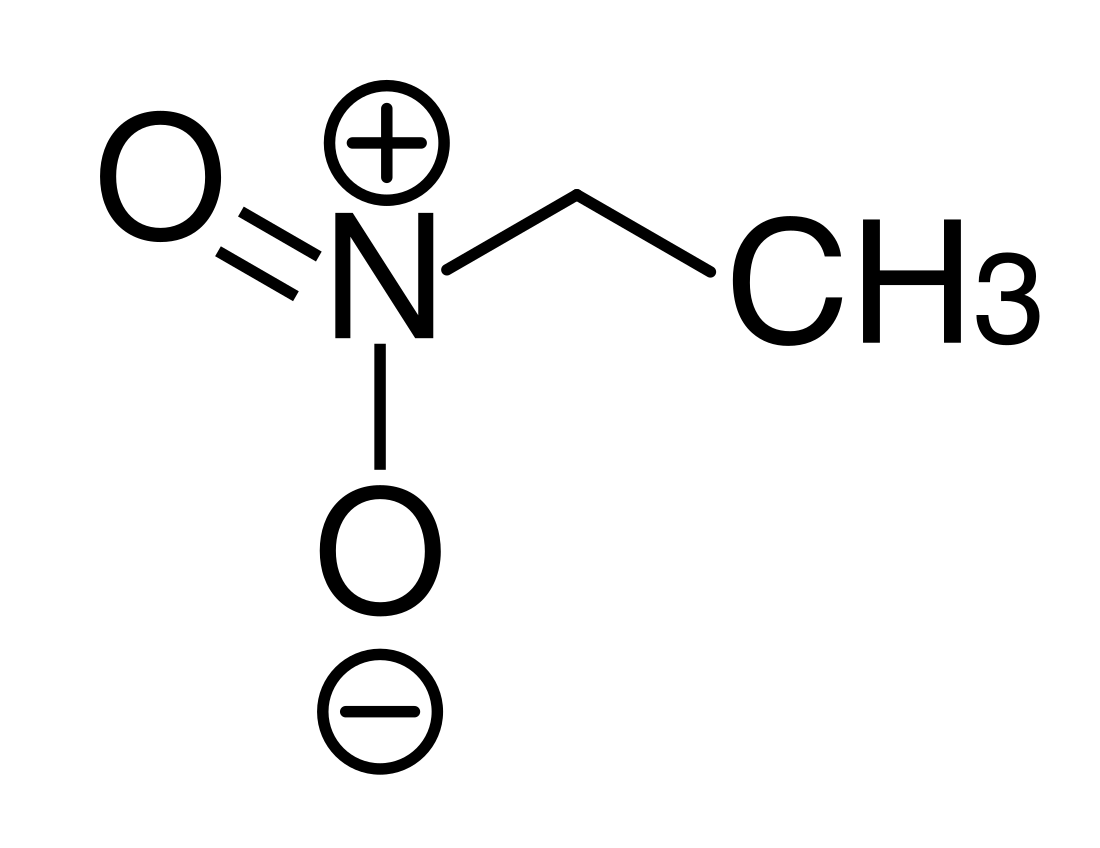
Nitroethan
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Remove ads
Nitroethan ist eine organische chemische Verbindung, die zur Gruppe der aliphatischen Nitroverbindungen, den Nitroalkanen gehört.
Remove ads
Geschichte
Die deutschen Chemiker Victor Meyer und O. Stüber stellten Nitroethan im Jahr 1872 als erste aliphatische Nitroverbindung aus Ethyliodid und Silbernitrit her.[8][9][10]
Darstellung und Gewinnung
Die Herstellung der Verbindung kann durch die Umsetzung von Ethyliodid mit Natriumnitrit in Dimethylformamid erfolgen.[11] Die industrielle Herstellung erfolgt in einer Gasphasennitrierung von Propan mittels Salpetersäure. In dieser Reaktion entstehen vier Nitroalkane: Nitromethan, Nitroethan, 1-Nitropropan und 2-Nitropropan.[12]
Eigenschaften
Zusammenfassung
Kontext
Physikalische Eigenschaften
Nitroethan ist eine farblose Flüssigkeit, die bei Normaldruck bei 115 °C siedet.[13] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,71267, B = 1671,266 und C = −31,963 im Temperaturbereich von 252 bis 387 K[14], sowie mit A = 1,74671, B = 207,774 und C = −269,20 im Temperaturbereich von 390 bis 459 K.[15] Die Verdampfungsenthalpie beträgt bei 25 °C 41,6 kJ·mol−1, am Siedepunkt 38,0 kJ·mol−1.[12][16] Die Verbindung schmilzt bei −89,52 °C[17] mit einer Schmelzenthalpie von 9,853 kJ·mol−1.[18] Die Wärmekapazität bei 25 °C beträgt 134,22 J·mol−1·K−1 bzw. 1,79 J·g−1·K−1.[18] Nitroethan ist mit Wasser nur begrenzt mischbar. Mit zunehmender Temperatur steigen die Löslichkeiten von Nitroethan in Wasser und von Wasser in Nitroethan nur in geringem Maße an.[12]
Löslichkeiten zwischen Nitroethan und Wasser[12] Temperatur °C 25 70 Nitroethan in Wasser in Ma-% 4,7 6,6 Wasser in Nitroethan in Ma-% 1,1 3,0
Mit einem Wassergehalt von 29,0 Ma% bildet die Verbindung ein bei 87,22 °C und Normaldruck siedendes Azeotrop.[12]
Chemische Eigenschaften
Die Verbindung kann sich ähnlich wie Nitromethan explosionsartig zersetzen.[19] Die Explosionswärme beträgt 3115 kJ·kg−1 (H2O (l)) bzw. 2893 kJ·kg−1 (H2O (g)), das Normalgasvolumen 1277 l·kg−1.[20] Der explosionsartige Zerfall kann durch Zusätze, wie Ammoniak oder starke Säuren sensibilisiert werden. In Mischungen mit Kohlenwasserstoffen und anderen oxidierbaren Substanzen kann es zur Entzündung und Explosion kommen. Mit Basen, wie Metalloxiden, Metallhydroxiden oder Metallcarbonaten werden hochinstabile Nitronate gebildet.[21]

Sicherheitstechnische Kenngrößen
Nitroethan bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt von 28 °C.[22][2] Der untere Explosionsgrenze liegt bei 3,4 Vol.‑% (106 g/m³).[2] Die Grenzspaltweite wurde mit 0,84 mm bestimmt.[22] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIB.[22] Die Zündtemperatur beträgt 410 °C.[22][2] Der Stoff fällt somit in die Temperaturklasse T2.
Remove ads
Verwendung
Nitroethan wird in der organischen Chemie zur Synthese verschiedenster Stoffe verwendet, da das an die Nitrogruppe gebundene Kohlenstoffatom durch die Mesomeriestabilisierung des Anions einen aciden Charakter besitzt. So bilden Nitroalkane mit Basen Salze. Eine der wichtigsten Reaktionen ist hierbei die Henry-Reaktion; je nach Bedingungen lassen sich Nitroalkene oder Nitroalkohole bilden. Diese Reaktion ist eine wichtige Möglichkeit zur Knüpfung von C–C-Bindungen.[23] Zudem eignet sich Nitroethan als Speziallösemittel. Im Nageldesign findet Nitroethan als Feilhilfe Verwendung.
Remove ads
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads