
Amonia nitrito
kemia kombinaĵo / From Wikipedia, the free encyclopedia
Amonia nitrito aŭ NH4NO2 estas neorganika salo rezultanta el reakcio inter la nitrita acido kaj amonia hidroksido. Ĝi trovatas kiel palflava kristaloj, kiu malkomponiĝas kiam varmigita al 60 °C−70 °C estigante nitrogenon kaj akvon. Ĝi malkomponiĝas pli rapide kiam miksita en koncentrita solvaĵo ol kiam seka kristalo.
| Amonia nitrito | |||
 | |||
| Kemia strukturo de la amonia nitrito | |||
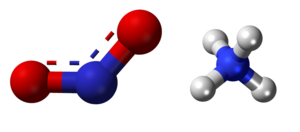 | |||
| Kemia strukturo de la amonia nitrito | |||
| CAS-numero-kodo | 13446-48-5 | ||
| ChemSpider kodo | 24223 | ||
| Fizikaj proprecoj | |||
| Aspekto | palflavaj kristaloj, kiu malrapide malkomponiĝas en nitrogenon kaj akvon. | ||
| Molmaso | 64.06 g mol−1 | ||
| GHS etikedigo de kemiaĵoj[1] | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H272, H319 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P220, P221, P264, P280, P305+351+338, P337+313, P370+378, P501 | ||
Ĝi prepareblas per oksidado de la amoniako kun la hidrogena peroksido, aŭ pere de precipita reakcio inter la "baria aŭ plumba II nitrito" kaj amonia sulfato, aŭ "arĝenta nitrito kun amonia klorido, aŭ amonia perklorato kun kalia nitrito. La precipitaĵo filtriĝas kaj la solvaĵo koncentriĝas. Senkoloraj kristaloj estiĝas kiuj estas akvosolveblaj kaj malkomponiĝas en la ĉeesto de acido, kun liberigo de nitrogeno.

