Proteoom
From Wikipedia, the free encyclopedia
Remove ads
Proteoom on teatud liigis, teatud isendis või muus teatud füsioloogilises tervikus konkreetsel ajahetkel esindatud valkude kogum. Näiteks võib rääkida inimese (Homo sapiens) proteoomist, aga ka inimese maksa proteoomist või patsiendi kopsuvähi metastaasi proteoomist. Proteoom on olemuslikult muutlik: näiteks võib teatud koes leiduvate valkude koosseis ja/või nende pöörduvate biokeemiliste modifikatsioonide valim muutuda, olenevalt organismi vanusest või tervislikust seisundist.

Proteoomi uuringud on eriti olulised nii rakendusliku teaduse (näiteks haiguste diagnoosimine või ravi) kui ka baasteaduse seisukohalt (näiteks evolutsionaarsete või arengubioloogiliste mehhanismide kindlakstegemine). Proteoomi alaosaks võivad olla ka muud "oomid": näiteks räägitakse retseptoomist (retseptori rolliga molekulide kooslus, millest põhiosa moodustavad valgud),[1] sekretoomist (rakkude sekreteeritavate ja sekretsiooni eest vastutavate molekulide kooslus, millest valgud moodustavad samuti suure osa)[2] või kinoomist (valkude fosforüülimist katalüüsivate ensüümide proteiinkinaaside kooslus).[3]
Mõiste autoriks peetakse Marc Wilkinsit,[4] kes tutvustas seda avalikult 1994. aastal. Trükis ilmus see esimest korda 1995. aastal osana Wilkinsi doktoritööst.[5]
Remove ads
Inimese proteoomi keerukus
Valkude arv
Lähtudes põhimõttest, et ühe geeni põhjal valmistatakse rakus üht tüüpi valku (keemilise struktuuri poolest), võiks inimorganismi proteoomis sisalduda maksimaalselt veidi üle 20 000 erineva valgu.[6] Tegelikult on inimorganismi proteoomi keerukus oluliselt suurem tänu järgmistele protsessidele:
- Geeni pealt "maha loetud" (transkribeeritud) mRNA erinev splaissimine ehk eel-mRNA molekuli selline töötlus, kus molekuli osade fragmentide (nn intronite) väljalõikamisel ühendatakse allesjäänud fragmendid (nn eksonid) mitmel eri viisil (inglise keeles alternative/differential splicing).
- Erinevused üksiku aminohappe tasemel (üksiku aminohappe polümorfismid). Need tulenevad omakorda erinevustest valku kodeeriva DNA tasemel (teatud tüüpi üksiku nukleotiidi polümorfismid).
- Translatsioonijärgsed modifikatsioonid ehk valgumolekuli koostisse kuuluvate aminohappejääkide erinevate funktsionaalrühmade külge eri omadustega lisafragmentide pöörduv ühendamine.[7]
Selline struktuurne mitmekesisus viib olukorrani, kus ühes geenis sisalduva info põhjal tehtud valk võib esineda hinnanguliselt üle 10 keemilise struktuuri poolest erineva molekulina,[8] kuigi teaduskirjanduses on pakutud ka oluliselt suuremaid numbreid.[7] Teatud lähenduses peegeldab aga vaadeldava bioloogilise objekti proteoom siiski objektis sisalduvat mRNA kogumit ehk transkriptoomi.
Valkude üldised struktuursed aspektid
Arvestades valkude suurt mitmekesisust ja nende ebaühtlast paigutust organismis ning isegi rakus, on üsna raske sõnastada valkude levinumaid parameetreid keemilise struktuuri ja muude omaduste poolest. Siiski on seda üritatud teha eri organismide jaoks[9] ning inimese proteoomi puhul on tulemus järgmine:
- Aminohappejääkide arv: vahemikus 250–430 (oleneb sellest, kas arvutatakse genoomi või reaalse proteoomi andmete alusel: väiksemate valkude osakaal proteoomis on suurem);
- Molekulmass: vahemikus 28 000 – 47 000 Da ehk 28–47 kDa (arvutades valemi järgi, mis ei eelda translatsioonijärgsete modifikatsioonide olemasolu: Mw = 110 ∙ #AA, kus Mw on valgu molekulmass, #AA on aminohappejääkide arv ja korrutustegur tuleneb kahekümne nn standardse aminohappejäägi keskmisest molekulmassist);
- Lineaarne mõõde voltunud valgu puhul (nt molekuli pikkus): 3–6 nm;
- Molaarne kontsentratsioon rakus: 10 nM – 1 μM.[10]

Sellise hüpoteetilise keskmistatud valgu jaoks on veelgi raskem leida reaalset vastet, kuid suhteliselt hästi sobib mudeliks näiteks proteiinkinaasi A ehk cAMP-sõltuva proteiinkinaasi ehk PRKACA) katalüütiline alaühik, tüüp α (geeni tähis PRKACA).[11] PRKACA omab kaks isovormi (alternatiivse splaissingu tõttu tekkinud valgu vormid) molekulmassidega ligi 40,6 kDa ja 39,8 kDa ning globulaarset "munakujulist" struktuuri (kristallstruktuuride[12] alusel on pikim mõõde ligi 60 Å ning lühim mõõde ligi 40 Å). Organismis on PRKACA üsna levinud[13] ning eri kudedes varieerub selle kontsentratsioon palju (nt vereliistakutes või see ulatuda lausa 3 μM-ni).[14]

Kui rääkida äärmustest inimese valkude molekulmassi skaalal, siis kõige suurem valk on suhteliselt hästi teada. See on titiin,[15] geeni TTN kodeeritav valk, mis on oluline lihaste töö tagamiseks ja kuulub vöötlihaste ehitusüksuste ehk sarkomeeride koostisse. Titiini molekul on suhteliselt elastne, kuid selle keskmine pikkus on ligi 1 μm ning inimese titiini levinumad isovormid sisaldavad 27 000 – 36 000 aminohappejääki.[16] Väiksemate valkude puhul tuleb kõigepealt defineerida, millist molekuli tuleks nimetada veel peptiidiks ja millist – juba valguks. Kui kokkuleppeline piir jookseb nt 100 aminohappejäägi juures, siis on inimorganismi talitluse seisukohalt tuntuimaks väiksemate valkude rühmaks ilmselt histoonid (näiteks inimese histoon H3.1 koosneb 136 aminohappejäägist ning omab molekulmassi veidi üle 15 kDa).[17] Histoonid on üliolulised DNA pakendamiseks rakutuumas, kuid need reguleerivad ka geenide avaldumist. Lühim füsioloogiliselt oluline peptiid on aga glutatioon, mis sisaldab kõigest 3 aminohappejääki (Glu, Cys ja Gly) ning omab väga suurt tähtsust redokstasakaalu hoidmisel rakkudes.[18][19]
Remove ads
Proteoom kui ravimite sihtmärkide allikas

Allpool vaadeldakse illustratiivseid näiteid, kuidas häired proteoomi eri tasemetel võivad põhjustada haigusi või aidata kaasa haiguste arengule. Tähelepanuväärne on just asjaolu, et protsessi on sageli kaasatud korraga mitmed tegurid, mistõttu tuleb haiguse mehhanismide seletamiseks lähtuda mitte niivõrd üksikust valgust, kuivõrd põhjuslikest seostest proteoomi talitlemisel. Igas alaosas esitatakse näiteid ka võimalikest raviviisidest, mis on juba kliinilises kasutuses või mida intensiivselt arutatakse tänapäeva teaduskirjanduses.
Polümorfismid üksiku aminohappe tasemel
Püsivad muutused valgu aminohappelises järjestuses on tingitud kodeeriva DNA nukleotiidijärjestuse muutustest ning seega on pigem geeniuuringute pärusmaaks. Samas on näidatud,[20][21] et patoloogiliseks kujunevad sellised aminohapete polümorfismid, kus algne aminohappejääk asendub keemilise struktuuri poolest väga erineva aminohappejäägiga. See on loogiline, sest muundunud aminohappelise järjestusega valk ei saa siis sageli omandada korralikku 3D-struktuuri (kuna selleks on vajalik kindel valgumolekulisisene vastastikmõjude muster) ning seega ei saa luua ka tüüpilisi vastastikmõjusid teiste valkudega. Näiteks võib välja tuua järgmised patoloogilises proteoomis levinud polümorfismid (st ei vaadelda konkreetseid valke, vaid muutusi aminohappelises koostises üle proteoomi tervikuna):
- Arginiinijääk (R, Arg) asendub histidiinijäägiga (H, His): kuigi mõlema puhul kannab aminohappejäägi külgahel füsioloogilise pH juures positiivset laengut, on külgahela pikkus ja vesiniksidemete loomise võime oluliselt erinev ning His külgahel asub sageli looma vastastikmõjusid metalliioonidega (nt Zn);2+
- Alaniinijääk (A, Ala) asendub treoniinijäägiga (T, Thr): Ala külgahel on väike ja hüdrofoobne, aga Thr külgahel sisaldab kiraalset tsentrit ning hüdroksüülrühma, millel on vesiniksideme donoorsed ja aktseptoorsed omadused;
- Glutamiinhappe jääk (E, Glu) asendub lüsiinijäägiga (K, Lys): füsioloogilise pH juures on Glu külgahel laetud negatiivselt, aga Lys oma positiivselt – seega käituvad need aminohappejäägid väga erinevalt laeng-laeng vastastikmõjude loomise seisukohalt.[22]



Kui aga rääkida konkreetsetest proteoomi liikmetest, mis on patoloogiate puhul enim muteerutud, siis näiteks erinevate kasvajate puhul esineb enim mutatsioone valgus TP53, millele järgnevad PIK3CA ja PTEN.[23] Terves organismis on TP53 oluline DNA vigastuste parandamises ning rakusurma käivitamises ning seepärast on selle valgu funktsiooni mahasuruvad mutatsioonid organismile ohtlikud. PIK3CA ja PTEN on aga ensüümid, mille füsioloogilised rollid on täpselt vastandlikud – esimene katalüüsib raku kasvuks hädavajaliku raja aktiveerumist, teine on aga raja loomulikuks piduriks. Vähkkasvajatele on omane PI3KCA anomaalselt suur aktiivsus (aktiveerivate mutatsioonide tulemusena) ja/või PTEN puudulik aktiivsus (inaktiveerivate mutatsioonide tulemusena). PIK3CA anomaalselt suure aktiivsuse mahasurumiseks saab kasutada selektiivseid inhibiitoreid. Näiteks on Ameerika Ühendriikide Toidu- ja Ravimiamet kiitnud heaks idelalisiibi, alpelisiibi ja duvelisiibi kasutamise metastaatilise rinnavähi, kroonilise lümfoidse leukeemia ja väikese lümfotsüütse lümfoomi raviks.[24]
Anomaalne proteolüüs
Valkude proteolüüsi saab liigitada täielikuks (valgumolekuli lagundamine aminohapeteni) ja osaliseks (valgumolekuli "lõikamine", mis katkestab ahelat kindlas kohas ja mille tulemusena tekib ühest molekulist kaks või enam kindla struktuuriga lõiku).

Valgumolekuli süntees on raku jaoks energeetiliselt üsna kulukas (1 aminohappejäägi ahelasse lülitamiseks kulub ligi 5 ATP molekuli).[25] Seepärast alluvad valkude täieliku lagundamisega seotud raku koostisosad (proteasoomid) üldiselt rangele kontrollile ning lagundamiseks suunatavaid valgumolekule märgistatakse rakus spetsiaalse järjestusega (ubikvitiin, mis kuulub samuti translatsioonijärgsete modifikatsioonide alla).[26] Vähirakkudes võib aga sünteesitavate ning lagundatavate valkude tasakaal olla häiritud: näiteks lagundatakse liiga intensiivselt valke, mis vastutavad tavaolukorras rakkude kasvu pidurdumise ning rakkude programmeeritud surma ehk apoptoosi käivitamise eest. Seetõttu kasutatakse vähiravis muuhulgas ka proteasoomi inhibiitoreid – näiteks bortesomiibi.[27]

Valkude osalist proteolüüsi (inglise keeles tuntud ka kui truncation) viivad läbi ensüümid proteaasid. Tüüpilisteks näideteks valkudest, mille puhul osaline lagundamine on vajalik organismi normaalseks talitluseks, on preprohormoonid ja zümogeenid. Nagu nimigi vihjab, tekivad preprohormoonide "lõikamisel" sisenõrenäärmete rakkudes valgulised või peptiidsed hormoonid,[28] mida seejärel sekreteeritakse ringesse. Zümogeenide "lõikamisel" tekivad aga aktiivsed ensüümid – sageli toodetakse organismis zümogeenidena neidsamu proteaase, sest on oluline, et proteaas muutuks aktiivseks vaid organismi teatud lokatsioonis, mitte otse selles rakus, kus proteaasi eelmolekuli toodetakse.[29] Näiteks toodetakse seedimiseks olulist ensüümi trüpsiini kõhunäärmes esialgu zümogeeni vormis (trüpsinogeen) ning trüpsinogeeni osaline proteolüüs toimub peensooles, kus trüpsiin peakski aitama lagundada toidus sisalduvaid valke. Kui aga trüpsinogeen peaks iseeneslikult aktiveeruma juba pankreases (seda soodustavad teatud aminohapete polümorfismid trüpsinogeeni molekulis, näiteks valgu 122. aminohappejäägi arginiini mutatsioon histidiiniks ehk Arg122His), tekib haiguslik seisund – pärilik krooniline pankreatiit.[30]
Osalise proteolüüsi häired, kus valgujärjestus katkestatakse vales kohas, on seotud ka neurodegeneratiivsete haigustega: tekkinud anomaalse struktuuriga valgud võivad valesti voltuda ja hakata kokku kleepuma (vt detailsemalt järgmises alapealkirjas).
Valkude anomaalne voltumine

Kuigi valgu struktuuri saab kirjeldada aminohappelise järjestuse abil (nn primaarne struktuur), on valgu ülesannete teostamiseks organismis ülioluline valgu 3D-struktuur. Selles esinevad piirkonnad, kus aminohappelised järjestused moodustavad teatud korrapäraga ruumilisi mustreid (sekundaarseid struktuure), aga ka paindlikuma iseloomuga silmused. Kuigi tänapäeval on eksperimentaalseid tehnikaid, mis võimaldavad valgu 3D-struktuuri kindlaks teha,[31] ja ka arvutuslikke algoritme, mis võimaldavad prognoosida valgu 3D-struktuuri primaarse struktuuri alusel,[32][33] jäävad paljude valkude ruumilised struktuurid seni tundmatuks. See on üks suuremaid takistusi valkudega seostuvate ravimite arenduse seisukohalt.
Voltumise põhimõtted
Ajalooliselt on pakutud, et füsioloogilises keskkonnas peaks vähemalt väiksemate veeslahustuvate globulaarsete (kerakujuliste) valkude jaoks kehtima reegel, et valgu kolmemõõtmeline struktuur on otseselt määratud valgu primaarstruktuuriga. See reegel (nn Anfinseni dogma) eeldab, et ribosoomidel värskelt sünteesitud valguahel peaks tsütoplasmas ajapikku iseeneslikult omandama õiget ruumilist struktuuri (voltuma), sest see struktuur on ühtlasi antud süsteemi (komponendid: valk, vesi, ioontugevus, pH) energeetiliseks miinimumiks.[34]

Reaalsuses ei ole iseenesliku voltumise "äraootamine" kuigi mõistlik, eriti pikemate valgumolekulide puhul, mis sageli sisaldavad ka hüdrofoobseid alasid. Kui ahela süntees ribosoomil on alles pooleli, võivad valgumolekuli valmis sünteesitud hüdrofoobsed lõigud hakata omavahel kokku kleepuma (agregeeruma) tänu hüdrofoobsetele vastastikmõjudele. Seepärast on rakus olemas spetsiaalsed abistavad valgud šaperonid, mis seostuvad valmiva valguahelaga ja kaitsevad seda agregeerumise eest.[35] Lisaks loob šaperoni enda hüdrofoobne sisemus soodsa keskkonna hüdrofoobsete aminojärjestuste iseeneslikuks voltumiseks (nt alfaheeliksi moodustumiseks). Sellist šaperonide tüüpi nimetatakse inglise keeles holdase (verbist hold 'hoidma') ning kuigi need loovad need ei riku Anfinseni dogmat, sest valgusünteesi lõpus šaperonid dissotsieeruvad valmis ahelalt ning jääb kehtima põhimõte, et voltunud valk on energeetiliselt stabiilsem kui mittevoltunud aminohappeline järjestus. Šaperonide teist tüüpi nimetatakse inglise keeles foldase (verbist fold 'voltima') ja need kasutavad ATP energiat selleks, et "painutada" tekkiva valgu ahelat sobilikuks ruumiliseks kujuks. Sellised šaperonid rikuvad Anfinseni dogmat, sest voltunud valk on sel juhul energeetiliselt vähem stabiilne kui mittevoltunud aminohappeline järjestus (ehk valgu voltumiseks peab süsteemile energiat juurde andma).[36]
Patoloogilised seisundid

Valkude voltumise häireid esineb mitmetes haigustes. Valesti või osaliselt voltunud valk ei ole sageli funktsionaalne, ehk see ei ole suuteline moodustama vastastikmõjusid teiste valkude ja väikeste biomolekulidega ning seetõttu ka panustama organismi normaalsesse toimimisse. Näiteks viib teatud mutatsioon (Cys203Arg) silma võrkkesta kolvikestes asuvas retseptoris (opsiinis OPN1MW) selleni, et retseptoris ei teki sisemolekulaarset disulfiidsilda Cys126-Cys203. Tulemuseks ei omanda OPN1MW normaalset ruumilist struktuuri ega moodusta kompleksit retinaaliga (pigment, mille keemiline struktuur muundub footoni pealelangemisel). See muudab kolvikesed kokkuvõttes tundetuks rohelise valguse suhtes ning on värvipimeduse levinud tüübi põhjuseks.[37]
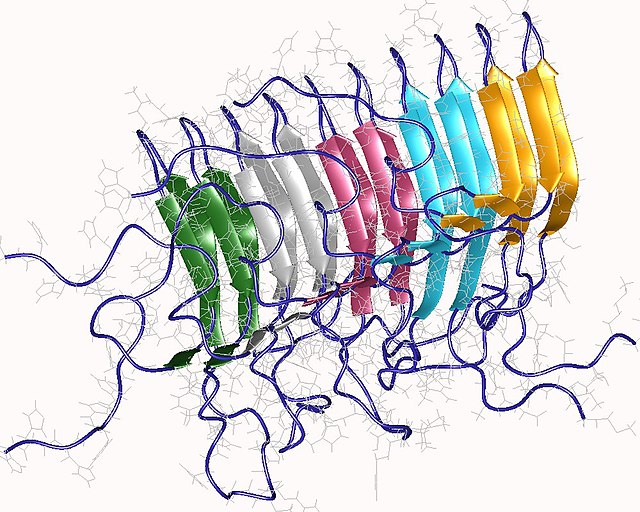
Teiselt poolt võib valesti voltunud valk hakata kleepuma teiste valesti voltunud või osaliselt voltunud valkude külge, tekitades mittelahustuvaid klompe (agregaate). Sellised agregaadid ei võimalda rakkudel normaalselt talitleda, häirides rakusiseseid dünaamilisi protsesse (näiteks ainete transport või tsütoskeleti ümberkorraldumine) ja ka suhtlust rakkude vahel, ning tekitavad sageli põletikulist vastust organismis, mille käigus võivad saada kannatada ka suhteliselt terved põletiku naabruses asuvad rakud. Ajusiseste agregaatide teke on seotud näiteks järgmiste patoloogiatega:
- Priionid: põhiliselt inimese valgu PNRP teatud isovormid, mis on ise valesti voltunud ning mis organismi sattumisel põhjustavad ka teiste valkude normaalse ruumilise struktuuri kadumist ning kleepumist priioni tekitatud agregaatide külge.[38]
- Alzheimeri tõve puhul esineb kaht tüüpi agregaate: peptiidist amüloid β koosnevad naastud (inglise keeles amyloid plaques) ja hüperfosforüülitud valgust tau koosnevad tängud (inglise keeles neurofibrillary tangles).[39] Fosforüülimist ja tau näidet käsitletakse detailsemalt ülejärgmises alapealkirjas. Amüloid β on aga 40–42 aminohappejäägist koosnev peptiid, mis tekib amüloidi eelvalgu APP anomaalsel proteolüütilisel lagundamisel β- ja γ-sekretaaside poolt (terves organismis teostavad APP proteolüüsi α- ja γ-sekretaasid). Amüloid β moodustab iseloomulikke β-lehtedest koosnevaid fibrille, mis pikenemisel liidavad endaga üha rohkem amüloid β molekule.[40]
- Parkinsoni tõve, multisüsteemse atroofia ja Lewy kehakeste dementsuse puhul tekitab agregaate valk α-sünukleiin (SNCA).[41] Uuringud on näidanud, et SNCA agregeerimist soodustavad mutatsioonid Ala53Thr, Ala30Pro ja Glu46Lys; neid mutatsioone omavatel isikutel on geneetiline eelsoodumus Parkinsoni tõve varaseks kujunemiseks.[42]

Seni puuduvad mainitud haiguste raviks kahjuks võimalused, kuid teaduskirjanduses on arutletud selliste tehnoloogiate üle, mis võimaldaksid sisestada patsiendi organismi rakkudesse lisašaperone.[43] Selline raviviis võimaldaks täiustada kontrolli valkude voltumise üle ning hoida ära agregaatide edasist kasvamist. Paraku ei ole kindel, kas selline tehnoloogia võimaldaks võidelda juba moodustunud agregaatidega – see on oluline, kuna neurodegeneratiivsete haiguste varajane diagnostika pole ka seni arendatud.[44]
Vähkkasvajatele on aga omane pigem šaperonide "ületootmine".[45] Põhjuseks on ilmselt asjaolu, et pidevalt jagunevates kiirekasvulistes rakkudes toimub elutegevuse tagamiseks vajalike valkude süntees anomaalselt suure tempoga – ning vastusena sellisele survele areneb rakkudes kaitsemehhanism, mis tagab kõrgendatud kontrolli valkude voltumise üle.[46] Selle nähtuse kohta öeldakse ka, et vähirakkudel on arenenud šaperonsõltuvus (inglise keeles chaperon additiction) ning onkoteraapiate arendamisel on muuhulgas pakutud võimaliku lähenemisena šaperonide (nt HSP90) aktiivsust blokeerivate ühendite ehk inhibiitorite kasutamist.[47][48]
Valgustruktuuri loomuliku dünaamilisuse (konformatsioonilise muutlikkuse) kadu
Selleks, et valgud saaksid täita oma funktsioone organismis, on oluline mitte ainult valgumolekulide korrektne voltumine, vaid ka 3D-struktuuri teatud lokaalne paindlikkus. Näiteks on selline konformatsiooniline muutlikkus oluline lihaste töös (lihasvalkude kompleksi ruumiline kuju peab võimaldama lihase nii kokkutõmbunud kui lõdvestunud olekut), aga ka retseptorite vahendatud signaaliülekandes (retseptori kuju peab muutuma, vastusena väliskeskkonnast saabunud keemilisele või füüsikalisele impulsile) või ensüümide vahendatud katalüüsis (efektiivseks toimimiseks peab valk olema suuteline siduma katalüüsitava reaktsiooni lähteaineid ning ka vabastama reaktsiooni produkte).[49][50] Valkude konformatsioonilise muutlikkuse kadumisega on otseselt või kaudselt seotud mitmed haigused, millest vaid mõni näide on toodud allpool.
Sirprakne aneemia

Sirprakse aneemia puhul on punaverelibledel tavalise kettakujulise vormi asemel sirbikujuline profiil. See haigus on tingitud punaverelible toimevalgu hemoglobiini β-alaühikus esinevast aminohappelisest polümorfismist Glu6Val. Normaalse hemoglobiini struktuur koosneb kahest α- ja kahest β-alaühikust ning hapniku seostumine ühe alaühiku heemi külge põhjustab struktuurset muutust, mille tõttu iga järgmine alaühik seob hapnikku kiiremini kui eelmine. Sama loogika kehtib ka hapniku vabastamise kohta, mis võimaldab hemoglobiinil efektiivselt teostada gaasivahetust, liikudes kopsudest kudedesse ja tagasi.[51] Muteerunud hemoglobiini puhul ei kaasne hapniku seostumisega aga β-alaühiku ruumilise struktuuri muutust ning jäigad valgumolekulid agregeerivad, muutes ka terve punaverelible kuju. Kui inimesel on muteerunud mõlemalt vanemalt päritud kromosoom 11 hemoglobiini β-alaühikut kodeeriv järjestus, kujuneb sirprakne aneemia eriti raskekujuliseks, kuna organismis ei toimi normaalne gaasivahetus ning sirprakse kujuga punaverelibled võivad kergesti moodustada trombe. Kui aga tegemist on vaid ühelt vanemalt päritud mutatsiooniga, on sümptomid pehmemad ning sirpraksete punavereliblede olemasolu võib olla hoopis eeliseks piirkondades, kus on levinud malaarianakkus. Nimelt ei suuda malaariaparasiit Plasmodium sirpraksetes punaverelibledes edukalt paljuneda.[52][53]
Philadelphia kromosoom

Philadelphia kromosoomiks nimetatakse anomaalset geenijärjestust kromosoomis 22, mis tekib kromosoomist 9 pärineva nukleotiidiahela ümberpaigutumisel (translokatsioonil) kromosoomi 22. See kromosoomi 22 piirkond kodeerib valku ABL1 (Abelsoni türosiinkinaas 1) ning ümberpaigutumise tulemusena tekib sellest liitvalk (fusioon) BCR-ABL1, mis esineb sageli kroonilise müeloidse leukeemiaga patsientidel.[54]

Tervetes rakkudes on ABL1 vaikimisi mitteaktiivses olekus: molekul voltub nii, et selle N-terminaalses osas paiknevad SH2 ja SH3 domeenid blokeerivad juurdepääsu katalüütilisele domeenile. Ainult juhul, kui ABL1 aktiveeritakse teiste proteiinkinaaside poolt, toimub struktuuri osaline avanemine. BCR-ABL1 puhul ei ole aga molekul võimeline omandama suletud konformatsiooni – tulemuseks on türosiinkinaas pidevalt aktiivne. Kuigi normaalse ABL1 aktiivsus on organismi eluks vajalik, viib selle anomaalselt suur aktiivsus vähi tekkeni. Seetõttu kasutatakse Philadelphia kromosoomiga patsientide ravis BCR-ABL1 inhibiitoreid (nt imatinibi), mis blokeerivad türosiinkinaasi katalüüsivõimet.[55]
Häired translatsioonijärgsete modifikatsioonide tasemel
Valkude translatsioonijärgsete modifikatsioonide (TJM) näol on tegemist teatud fragmentide lisamisega valmissünteesitud valgu funktsionaalrühmade külge. Valgu modifitseeritavateks rühmadeks on nukleofiilsed funktsionaalrühmad (hüdroksüül-, tiool-, amino- või karboksüülrühmad), mis paiknevad kas aminohappejääkide külgahelates või valgumolekuli otstes (sisuliselt asendatakse üks hapniku, väävli või lämmastikuaatomi küljes olev vesinik lisatava fragmendiga). TJM on pöörduvad, ehk siis neid saab valgumolekuli küljest ka eemaldada – kusjuures nii TJM lisamist kui eemaldamist katalüüsivad spetsiaalsed ensüümid.[56][57]
Lisatavaid fragmente on mitmeid, nii keemilise struktuuri kui suuruse poolest:[58][59]
TJM lisamise tulemusena muutub modifitseeritava funktsionaalrühma võime luua vastastikmõjusid teiste funktsionaalrühmadega (sama molekuli või teiste molekulide koostises). Kuigi näiliselt ei pruugi muutus valgumolekulis tunduda suur, võib TJM oluliselt muuta valgu kaasatust signaaliradadesse, mõjutades valk-valk interaktsioone, valgu lokalisatsiooni jm.[56] Sel viisil võimaldavadki TJM lülitada ümber valgu aktiivsust, ilma et rakk peaks teostama valgu lagundamist ning seejärel taas aja- ja energiakulukat valgusünteesi. Tervetes rakkudes osaleb TJM läbiviimises hinnanguliselt kuni 5% geenidest. Samas võivad TJM anomaaliad, mis enamasti lähtuvad TJM lisavate või eemaldavate ensüümide anomaalsest aktiivsusest, olla seotud mitmete haigustega.[58]
Eespool sai alapealkirjades "Polümorfismid üksiku aminohappe tasemel" ja "Philadelphia kromosoom" käsitletud näiteid proteiinkinaaside anomaalse aktiivsuse kohta vähkkasvajates; allpool vaadeldakse veel mõningaid seoseid TJM ja patoloogiate vahel.
Tau hüperfosforüülimine Alzheimeri tõves

Alzheimeri tõve seos valkude anomaalse voltumisega on mainitud alapealkirjas eespool. Valk tau, mis on tervetes neuronites oluline mikrotuubulite stabiilsuse tagamiseks, moodustab Alzheimeri tõve diagnoosiga patsientide neuronites lahustumatuid agregaate. Need agregaadid põhjustavad omakorda muutusi neuronite struktuuris ja panustavad neuronite surma.[60]
Teadusuuringud on näidanud, et tau agregeerumise põhjuseks on tingitud valku anomaalselt rohkest fosforüülitusest (st tau sisaldab 3–4 korda rohkem fosforüülrühmi kui tervetes neuronites). Hüperfosforüülitud tau ei seostu mikrotuubulitega. Seni pole selge, millis(t)e proteiinkinaasi(de) anomaalselt suur aktiivsus panustab tau hüperfosforüülimisse, kuid kandidaatidena on pakutud tsükliini-sõltuvat proteiinkinaasi Cdk5 ja glükogeeni süntaasi kinaasi GSK3-β. Samuti on näidatud, et Alzheimeri tõvega patsientide ajus on anomaalselt väike fosfataasi PP2A aktiivsus (ning fosfataasid katalüüsivad fosforüülrühma eemaldamist valkudelt).[61]
Histoonide TJM seos vähiga

Valgud histoonid on olulised DNA pakendamiseks rakutuumas (vt ka eespool alapealkiri "Valkude üldised struktuursed aspektid"). Seepärast võimaldavad histoonide TJM kas (A) muuta DNA ja histoonide kompleksi ehk kromatiini pakendamise tihedust või (B) moduleerida mRNA sünteesi käivitavate või pidurdavate valkude aktiivsust – ning sel viisil reguleerida geenide avaldumist. Näiteks histoonide Lys atsetüülimine eemaldab füsioloogilise pH juures positiivselt laetud lüsiinijäägilt positiivse laengu; tekkiv atsetüülitud Lys ei moodusta enam negatiivselt laetud DNA-ga kompleksi ning geenitranskriptsioon on soodustatud. Histoonide Arg ja Lys metüülimine mõjutab aga transkriptsiooni aktivaatorite ja repressorite juurdepääsetavust DNA-le.[62][63][64]
Teadusuuringute põhjal selgus kaks histoonide TJM-vahendavat ensüümide rühma, millel on anomaalselt suur aktiivsus erinevates vähkkasvajates. Need ensüümid on valkude arginiini metüültransferaasid (PRMT), mis katalüüsivad histoonide Arg metüülimist, ning histoonide deatsetülaasid (HDAC), mis katalüüsivad histoonidelt atsetüülrühma eemaldamist. PRMT ja HDAC liigse aktiivsuse täpne toimemehhanism (nt avalduvate geenide tasemel) pole hetkeseisuga lõplikult selge ja võib oleneda konkreetse kasvaja molekulaarsest profiilist.[65][66] Küll on aga Ameerika Ühendriikide Toidu- ja Ravimiamet kiitnud heaks HDAC inhibiitorite (nt vorinostati) kasutamist T-rakuliste lümfoomide ravis[67] ning PRMT mitmed inhibiitorid (nt ühend GSK3326595) on läbimas kliinilisi katsetusi.[68]
Häired valkude tegevuse ruumilis-ajalisel kooskõlastamisel
Selleks, et organism tervikuna ja rakk selle ehitusüksusena saaks normaalselt talitleda, on oluline, et proteoomi vahendatud signaaliülekandes kehtiksid teatud põhimõtted:
- hierarhiline ülesehitus (st osad komponendid reageerivad muutustele varem kui teised),
- võimendus (sissetulevat impulssi peab saama n-ö üles skaleerida),
- tagasisidestatus (st ajaliselt hiljem aktiveeruvad komponendid peavad signaliseerima neist varem aktiveerunud komponentidele) ning
- pöörduvus (st algne olukord tuleb taastada, et süsteem muutuks taas reaktsioonivõimeliseks).[69][70][71]
Need põhimõtted võimaldavad koordineerida ajas ja ruumis väga keerulisi protsesse, alates embrüonaalsest arengust kuni une-ärkvelolekutsüklini. Üsna loogiline on ka see, et häired valkude aktiivsuse kooskõlastamisel ajas või ruumis põhjustavad tõsiseid haigusi. Lihtsuse mõttes vaadeldakse siinkohas ainult ühe raku tasemel käsitletavaid näiteid.
Rakutsükkel ja selle kontrollpunktide häired
Rakutsükkel on järjestikuste protsesside kogum, mis kindlustab enamiku keharakkude korduva jagunemise. Rakutsüklis eristatakse eri faase: jagunemise järel rakk kasvab (G1-faas, G tuleneb ingliskeelsest sõnast gap, kuigi mõnikord mõistetakse seda ka sõnana growth), kahekordistab DNA komplekti ja tsentrosoomi (S-faas, sõnast "süntees"), kasvab veelgi ja valmistub uueks jagunemiseks (G2-faas) ning lõpuks jaguneb (M-faas, sõnast "mitoos").[72]

Rakutsükli sujuvat käiku kindlustab mitmete ensüümide kooskõlaline aktiivsus, milles keskset rolli mängivad tsükliinisõltuvad proteiinkinaasid (CDK) ja nende aktivaatorid – valgud tsükliinid. Ilma tsükliinita ei ole CDK-d katalüütiliselt aktiivsed ning igal CDK-l (millest enamikus rakkudes on ekspresseerunud CDK1, CDK2 ja CDK4 või 6) on oma eelistatud aktivaator (tsükliini tüüp: A, B, D või E). Rakk ei ekspresseeri tsükliine korraga, vaid rakutsükli eri faasidele on iseloomulik eri tsükliinide suurenenud aktiivsus, kusjuures iga tsükliini taseme (ja seega tsüklini-CDK kompleksi aktiivsuse) kasvamisel käivitub järjekorras järgmise tsükliini ekspressioon ning samas enamasti lõpeb järjekorras eelmise tsükliini tootmine. Selles ahelprotsessis on raske eristada algust ja lõppu, kuid üldiselt peetakse rakutsükli "algatajateks" tsükliini D, mis seostub kinaasiga CDK4 või CDK6. Tsükliin D koos oma sidumispartneritega käivitavad G1-S üleminekule omast tsükliini E tootmist (seostub eelistatult kinaasiga CDK2), mis omakorda käivitab S-G2 üleminekul tsükliini A tootmist (seostub samuti kinaasiga CDK2, aga ka CDK1). Lõpuks käivitatakse mitoosifaasis olulise tsükliini B tootmine, mis seostub eelistatult kinaasiga CDK1.[73][74]
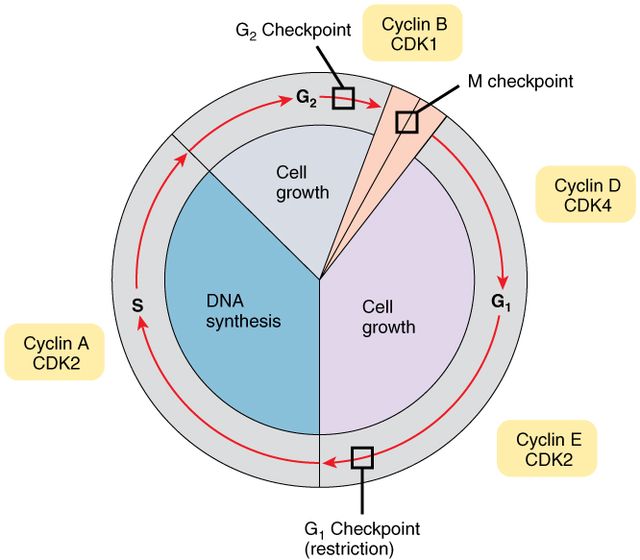
Rakutsüklis esineb mitu "sisseprogrammeeritud" kontrollpunkti, millest enamasti eristatakse kolme:
- raku suuruse ja geomeetria kontrollpunkt G1 lõpupoole (tehakse kindlaks, et rakk omab piisavalt valke S-faasi jaoks);
- DNA sünteesi kontrollpunkt S-faasi jooksul (tehakse kindlaks, et kahekordistamise tulemusena tekkib algsega identne koopia);
- kääviniidistiku kontrollpunkt M-faasi keskel (tehakse kindlaks, et lahknevate kromosoomide tütarkromatiidid on kääviniidistiku külge kinnitunud viisil, mis võimaldab neid viia lahku jaguneva raku eri poolustele).[75]

Kontrollpunkte teostavad samuti kooskõlaliselt mitmed erinevad valgud (näiteks DNA replikatsiooniga seotud ensüümid, tsentrosoomide või DNA-ga seonduvad kinaasid ja fosfataasid jm). Nende koostöö kindlustab, et rakutsükli läbimise järel tekib emarakust kaks identset tütarrakku. Kui rakk ei läbi kontrollpunkti, pidurdatakse edasiste sündmuste käik ning püütakse tuvastatud vigu parandada (näiteks käivitatakse DNA parandus või antakse rohkem aega lahknevate tütarkromatiidide korrektseks kinnitamiseks kääviniidistiku külge). Vigade paranduse ebaõnnestumisel suunatakse rakk programmeeritud rakusurma ehk apoptoosi.[76] Kui aga mõni kontrollpunkt ei toimi normaalselt, ehk siis ignoreeritakse reaalselt esinevate vigade olemasolu, võib see kokkuvõttes viia raku geneetilise ebastabiilsuseni, mis on omane vähkkasvajatele. Näiteks on näidatud, et paljudes kasvajates esineb anomaalselt suur CDK4/6 aktiivsus ja ka nn Aurora-kinaaside aktiivsus, mis võimaldab rakul pääseda kontrollpunktide "normide" täitmisest.[77] Seepärast on nii CDK4/6 kui Aurora-kinaasid ravimiarenduse jaoks olulised sihtmärgid ning CDK4/6 inhibiitoreid (nt palbotsikliib) on Ameerika Ühendriikide Toidu- ja Ravimiamet kiitnud heaks teatud tüüpi rinnavähi ravis.[78]
Valkude rakusisese lokalisatsiooni olulisus

Raku normaalseks toimimiseks on oluline, et teatud valkude aktiivsus oleks piiritletud mitte ainult ajaliste, vaid ka ruumiliste teguritega. Nii saavad transkriptsioonifaktorid mõjutada geenide avaldumist ainult siis, kui valgud ise asuvad rakutuumas (mitte näiteks tsütoplasmas). Abistamaks valkude liikumist eri organellide vahel on evolutsiooni käigus kujunenud teatud aminohappelised järjestused (inglise keeles localization signals), mis annavad rakusisestele mehhanismidele märku sellest, kus peaks rakusiseselt asuma just antud järjestust sisaldav valk – või kus see asuda ei tohiks. Näiteks on olemas aminohappelised järjestused, mille "ettenäitamisel" transporditakse valk rakutuuma (nn nuclear localization signal ehk NLS), ning samas aminohappelised järjestused, mille "ettenäitamisel" transporditakse valk rakutuumast välja (nn nuclear export signal ehk NES). Valkude ruumilist kuju arvestades ei pruugi sellised aminohappelised järjestused alati olla vaikimisi valgu välispinnal ehk "nähtaval" rakus sisalduvate teiste molekulide jaoks, vaid need võivad ka "paljastuda" valgu ruumilise struktuuri muutmisel (vt ka alapealkiri "Valgustruktuuri loomuliku dünaamilisuse (konformatsioonilise muutlikkuse) kadu").[79][80]

Haruldased, kuid ilmekad näited valgu rakusisese lokalisatsiooni olulisusest on seotud valguga SRY. Seda valku kodeerib Y-kromosoomil paiknev geen ning selle valgu aktiivsus on seotud sooliste tunnuste arenguga. Nimelt kulgeb inimese sugunäärmete areng esialgu nii XX- kui XY-genotüübiga loodetel esialgu ühtemoodi, kuid mingil hetkel lülitub XY-lootel sisse Y-kromosoomi vahendatud signaalirada (ning selle puudumisel arenevad lootel vaikimisi pigem naissoole omased sootunnused). Just SRY on üks mitmetest transkriptsioonifaktoritest, mis on oluline meesloote varases arengustaadiumis munandite normaalseks moodustumiseks. Oma ülesannete teostamiseks peab SRY lokaliseeruma rakutuuma ning SRY valgus on ka kaks NLS-tüüpi järjestust.[81]
Swyeri sündroom on haruldane hüpogonaidism, millele on omane mutatsioonide esinemine SRY geenis. Mõned nendest mutatsioonidest tingivad muidu funktsionaalse SRY tootmist, kuid üksiku aminohappe polümorfismi tõttu ei ole selle NLS järjestus õige – seetõttu ei pääse ribosoomidel toodetud SRY rakutuuma ega saa oma rolli transkriptsioonifaktorina täita.[82] Tulemusena kujunevad XY-genotüübiga lootel erandlikult naissoo tunnused (munasarjad ei ole küll funktsionaalsed, sest östrogeenide kõrge taseme tootmiseks on vaja kaht X-kromosoomi).[83] Teisalt on SRY-ga seoses võimalik ka hoopis teine stsenaarium, mis tingib XX-genotüübi puhul erandlikult meessoo tunnuste arengut (üks de la Chapelle sündroomi alatüüpidest). See sündroom on seotud isiku isa organismis toimunud spermatogeneesi iseärasusega, kus rekombinatsiooni käigus toimub juhuslik SRY-kodeeriva geeni ümberpaigutumine Y-kromosoomilt X-kromosoomile. Sellise X-kromosoomi pärandumisel järglasele asub SRY geeni kodeeritud valk loote arengu teatud staadiumis tööle ning vaatamata kahe X-kromosoomi olemasolule, arenevad lootel meessoo tunnused.[84]
Nii de la Chapelle kui Swyeri sündroomiga isikud on viljatud, kuid Swyeri sündroomi puhul on patsiendil olemas funktsionaalne emakas – seega võib patsient soovi korral rasestuda, kasutades doonori munarakku.[81][84]
Remove ads
Proteoom kui biomarkerite allikas

Kui artikli senine tekst suuresti keskendus proteoomile kui võimalike ravisihtmärkide kogumile, siis allpool keskendutakse proteoomi komponentide olulisusele biomarkeritena. Biomarkeri definitsioone on mitmeid,[85][86] kuid üldiselt on tegemist loodusliku molekuliga, mis leidub/võib leiduda inimorganismi kudedes või kehavedelikes ning mille sisaldus või aktiivsus on organismi tervisliku seisundi indikaatoriks. Lähtudes kliinilisest rakendusest, võib biomarkereid kasutada mitmeti: tuvastamaks patsiendi eelsoodumust haiguseks, diagnoosimaks haiguse olemasolu, määramaks haiguse staadiumit, valimaks sobivaimat raviskeemi või jälgimaks ravi edukust.[87]
Valkude kõrval võivad biomarkeriteks olla loomulikult teisedki väiksemad ja suuremad biomolekulid: näiteks keskenduvad tänapäeval mitmed uuringud rakuvaba DNA rollile vähi biomarkerina[88][89] ja rakuvälise RNA rollidele eri tervislike seisundite (muuhulgas raseduse komplikatsioonide) biomarkerina.[90][91] Biomarkereid võib uuritavas proovis tuvastada nii individuaalselt (st eesmärgiks on määrata ühe kindla molekuli sisaldus või aktiivsus) kui kogumina.
Üksikud valgulised biomarkerid
Kuna valgulisi biomarkereid kasutatakse paljude tervislike seisundite hindamiseks, siis allpool tabelis toodud näidete valim ei ole kindlasti kuigi täielik. Ülevaadet vähi biomarkeritest annab näiteks vastav lehekülg Vikipeedias. Selle tabeli eesmärgiks on aga pigem illustreerida, et:
- markeri olemasolu ei pea olema tingimata märgiks mingisugusest haiguslikust seisundist;
- valgud, mille olemasolu on täiesti normaalne organismi varases arengustaadiumis, võivad osutuda täiskasvanud indiviidi puhul haiguslikeks biomarkeriteks; ning
- üksiku markeri tuvastamine ei pruugi luua selgust diagnoosist, vaid vajatakse lisainfot muude analüüside (sh teiste biomarkerite tuvastuse) näol.
Kõiki eespool mainitud, aga ka paljusid muid biomarkereid määratakse patsientide proovides igapäevaselt haiglate laborites ja meditsiinilaborites.[110][111] Vabatahtlikel veredoonoritel määratakse verekeskustes enne vere võtmist hemoglobiini taset ning osa võetud verest kasutatakse HIV- ja hepatiit C vastaste antikehade ning hepatiit B antigeeni analüüsiks (lisaks sellele analüüsitakse nimetatud viiruste sisaldust ka vastavate PCR-testidega).[112][113] Mõningaid valgulisi biomarkereid, nt hCG-d või SARS-CoV-2 viiruse nukleokapsiidivalku, on võimelised suure usaldusväärsusega tuvastama ka käsimüügis kättesaadavad kiirtestid.
Valguliste biomarkerite kogumid

Biomarkerite tähtsuse kasv haiguste diagnoosimisel ja teraapiate edukuse jälgimisel on käinud käsikäes tehnilise arenguga: uued tehnoloogiad võimaldavad biomarkereid bioloogilistes proovides selektiivselt ja efektiivselt tuvastada. Tehnoloogiate arengu üheks sihtmärgiks on olnud ka korraga mitme biomarkeri tuvastus proovis (nn multipleksanalüüs, kus tüvi "pleks" on vihjab komplekssusele), mis võimaldaks kokku hoida analüüsi aega, abireagente ja ka bioloogilise proovi hulka. Kuigi see lähenemine nõuab sageli põhjalikku optimeerimist (nt kõigi analüütide sisaldus ei ole proovis samas suurusjärgus ning mõnede biomarkerite tuvastus on paratamatult tundlikum kui teiste oma), on viimase 20 aasta jooksul toimunud multipleksanalüüside jõuline edenemine.[114]

Tuntuim tehniline lahendus valkude, aga ka muude biomolekulide analüüsis on 1995. aastal tutvustatud Luminex xMAP tehnoloogia, mis ühendab immunoensüümanalüüsi (ELISA) ja voolutsütomeetria (FC) eeliseid.[115] Luminex xMAP protokolle on mitmeid,[116] näiteks võimaldab see tuvastada proovis korraga mitmeid tsütokiine (immuunvastust vahendavad väikesed valgud) või mitmeid maatriksi metalloproteinaase (Ca2+/Zn2+-sõltuvad valgud, mis lagundavad rakuvaheainet ja osalevad ka rakkudevahelises signaaliülekandes). Teiste tehniliste lahendustena proteoomi multipleksanalüüsides on aga pakutud näiteks mikrovedelikunduse vormingusse üle viidud ELISA-t[117] ja ka optilise mikroskoopia eritehnikaid.[118] Kliinilistes rakendustes on multipleksanalüüsidest olnud palju abi näiteks elundite siirdamisel, kus on vaja korraga hinnata doonori ja retsipiendi markerite profiili sobivust ning reageerida kiiresti juhul, kui retsipiendi organismis siiski käivitub transplantaadi äratõukereaktsioon.[119][120]
Uute valguliste biomarkerite avastamiseks on aga kasutatud sõrmejäljemeetodit (fingerprinting) ja mille tehniliseks teostuseks kasutatakse enamasti massispektromeetriat,[121][122] kuigi on teateid ka näiteks Raman-spektroskoopial põhinevaid lähenemisi.[123] Lähenemise tuum seisneb korraga paljudest markeritest tulenevate signaalide mõõtmises ühes proovis (nt massi-laengu suhtes või elektromagnetilise kiirguse neelduvused), kusjuures meetodi arendusjärgus on teada, kas proov pärineb tervelt doonorilt või teatud haigusega patsiendilt. Selle asemel, et keskenduda seejärel ühe või mõne valgu või selle fragmendi tuvastamisele, tehakse signaalide kompleksne analüüs, identifitseerimaks haigusele omast signaalide mustrit (sellest ka sarnasus sõrmejäljega: üks joon ei ole piisavalt informatiivne, kuid joonte muster aitab sõrmejälje omanikku kindlalt tuvastada). Mustrite äratundmiseks fingerprinting-analüüsides kasutatakse sageli ka tehisintellekti eeliseid.[124][125]
Baasteaduslikes uuringutes on fingerprinting-analüüse kasutatud nt neurodegeneratiivsete haiguste, vähkkasvajate ja infektsioonhaiguste valguliste biomarkerite profiili avastamiseks, püüdluses aidata kaasa paremate diagnostiliste meetodite arengule.[121][123][125] Hiljutistest arengutest paistab silma fingerprinting-analüüside kasutamine ka hindamaks haigustekitajate või vähirakkude tundlikkust erinevate ravimeetodite suhtes, mis võib tuua tulevikus fingerprinting-analüüse palju lähemale kliinilistele rakendustele personaalmeditsiinis.[122][126]
Remove ads
Proteoomialased andmebaasid ja algoritmid
Infot proteoomi eri aspektide kohta (nt valkude ekspressioonitasemed eri kudedes, seos patoloogiliste seisunditega, aminohappeline järjestus, 3D-struktuur) leiab mitmetest andmebaasidest, millest üldisemad on käsitletud allpool. Need andmebaasid on rahvusvahelise teadlaskonna arendatud ja laialdaselt tunnustatud ning proteoomi uuringutega tegelevad teadlased kasutavad neid igapäevaselt. Kuna tegemist on aga vabalt juurdepääsetavate, kasutajasõbralike ning pidevalt täienevate ressurssidega, võiksid need pakkuda huvi ka laiemale sihtrühmale.
FASTA
FASTA on tegelikult tekstipõhine vorming, mille võtsid kasutusele David J. Lipman ja William R. Pearson.[127] FASTA vorming on kasutusel mitmes biokeemia andmebaasides[128] kas nukleotiidi- või aminohappejääkide järjestuse üleskirjutamiseks vastavalt nukleiinhapete või valgumolekulide puhul. Järjestuse ees paikneb enamasti märk ">" või ";" ning sellele järgneb molekuli nimetus või identifikaator (nt UniProt-kood ehk accession number,[129] vt alapealkiri allpool).


Identifikaatori järel uuel real kirjutatakse aminohappejäägid, kasutades ühetähelisi kokkuleppelisi lühendeid (nt alaniin – A, trüptofaan – W) ning alustades valgu N-terminaalist. Harva kasutatakse ka lisatähistust:
- B tähistab asparagiinhapet (tavaline tähistus D) või asparagiini (tavaline tähistus N),
- J tähistab isoleutsiini (tavaline tähistus I) või leutsiini (tavaline tähistus L),
- O tähistab pürrolüsiini,
- U tähistab selenotsüsteiini,
- Z tähistab glutamiinhapet (tavaline tähistus E) või glutamiini (tavaline tähistus Q),
- X tähendab suvalist aminohapet,
- "-" tähendab määramatu pikkusega tühikut.
FASTA-vormingu ühes reas on enamasti 80 tähemärki ning 80 aminohappejäägist pikemad ahelad jätkuvad järgmisel real (st see ei tähenda, et valgu koostises oleks mitu ahelat). FASTA alusel on mugav võrrelda näiteks erinevusi valgu kahe või enama isovormi aminohappelises koostises (vt ka järgmine alapealkiri).
Näide: histoon H3.1 järjestus FASTA-vormingus:[17]
>sp|P68431|H31_HUMAN Histone H3.1 OS=Homo sapiens OX=9606 GN=H3C12 PE=1 SV=2 MARTKQTARKSTGGKAPRKQLATKAARKSAPATGGVKKPHRYRPGTVALREIRRYQKSTE LLIRKLPFQRLVREIAQDFKTDLRFQSSAVMALQEACEAYLVGLFEDTNLCAIHAKRVTI MPKDIQLARRIRGERA
BLAST
BLAST on algoritm, mille on välja töötanud Samuel Karlin ja Steven Altschul.[130] BLAST võimaldab leida sarnasusi kahes nukleotiidi- või aminohappejääkide järjestuses ning ühtlasi võrdleb kumbagi võrreldavat järjestust andmebaasides oleva infoga, tuvastades geene või valke, millesse antud järjestus kuulub. Näiteks saab BLAST-algoritmi abil võrrelda sarnasust (homoloogiat) kahest eri organismist pärinev valgu vahel, mis võimaldab teha esimeses lähenduses järeldusi ka nende funktsioonide sarnasuse kohta.
BLAST algoritmi saab tasuta kasutada online-režiimis[131] ning kõige mugavam on sisestada võrreldavaid järjestusi FASTA-vormingus (vt alapealkiri eespool). Ka analüüsi tulemus (Alignments) kuvatakse modifitseeritud FASTA-vormingus, kus kaks võrreldavat järjestust on paigutatud kohakuti ning järjestuste vahel paikneb võrdlusriba. Võrdlusribal on teatud viisil näidatud identsed aminohappejäägid kahes järjestuses (nt aminohapete ühetäheliste lühenditena või vertikaalsete joontena). Keemiliste omaduste poolest sarnaseid aminohappejääke (nt Lys ja Arg) tähistatakse võrdlusribal märgiga "+". Vasakul ja paremal pool järjestustest on näha aminohappe järjekorranumbrit kummaski järjestuses, millest alates algoritm tuvastas sarnasusi. Samuti kuvatakse statistika võrdluse tulemusena leitud identsete ja sarnaste aminohappejääkide arvu kohta.
Näide: inimese (Homo sapiens) ja veise (Bos taurus) insuliini järjestuste võrdlus algoritmiga BLAST[132] – väljavõte analüüsi väljundist (võrdlusriba on näidatud allajoonituna):
Query: RecName: Full=Insulin; Flags: Precursor [Homo sapiens] Query ID: P01308.1 Length: 110 Sbjct: RecName: Full=Insulin; Flags: Precursor [Bos taurus] Sequence ID: P01317.2 Length: 105
Range 1: 1 to 105
Method:Compositional matrix adjust., Identities:84/110(76%), Positives:86/110(78%), Gaps:5/110(4%)
Query 1 MALWMRLLPLLALLALWGPDPAAAFVNQHLCGSHLVEALYLVCGERGFFYTPKTRREAED 60
MALW RL PLLALLALW P PA AFVNQHLCGSHLVEALYLVCGERGFFYTPK RRE E
Sbjct 1 MALWTRLRPLLALLALWPPPPARAFVNQHLCGSHLVEALYLVCGERGFFYTPKARREVEG 60
Query 61 LQVGQVELGGGPGAGSLQPLALEGSLQKRGIVEQCCTSICSLYQLENYCN 110
QVG +EL AG LEG QKRGIVEQCC S+CSLYQLENYCN
Sbjct 61 PQVGALEL-----AGGPGAGGLEGPPQKRGIVEQCCASVCSLYQLENYCN 105
UniProt

UniProt on mitme asutuse (Euroopa Bioinformaatika Instituut,[133] USA Protein Information Resource[134] ja Šveitsi Bioinformaatika Instituut)[135] koostööna valminud andmebaas,[136] millest on kujunenud proteoomi uuringutega tegeleva teadlaskonna käsiraamat. 12. oktoobri 2022 seisuga sisaldas andmebaas infot kokku 288 533 erineva valgu kohta, mis pärinevad kokku 14 372 liigist.[137] Liikidest on enim esindatud inimese (Homo sapiens), koduhiire (Mus musculus), hariliku müürlooga (Arabidopsis thaliana), rändroti (Rattus norvegicus) ja pagaripärmi (Saccharomyces cerevisiae tüvi ATCC 204508 / S288c) proteoomide liikmed.
Andmebaas võtab kokku info mitmetest allikatest. Kuigi sissekannete detailsus oleneb konkreetsest valgust, antakse ülevaade järgmiste üksikasjade kohta (vt nt sissekanne inimese insuliini kohta):[138]
- Valgu erinevate isovormide aminohappelised järjestused ja molekulmass;
- Valgu struktuursed eripärad: tuntud ehitusüksused ehk domeenid, mida saab ennustada primaarstruktuuri põhjal, ning eksperimentaalsed andmed või ennustused 3D-struktuuri kohta;
- Valgu teadaolevad mutatsioonid, mis on seotud haiguslike seisunditega;
- Valgu teadaolevad translatsioonijärgsed modifikatsioonid;
- Valgu rakusisene lokalisatsioon ning ekspressioonitase organismi eri kudedes;
- Valgu tuntud rollid rakus ja organismis, sh "koostöö" teiste valkudega.
UniProt andmebaasi kasutatakse ka proteoomi massispektromeetriliste uuringute tulemuste interpreteerimiseks (st tuvastamaks, millise valgu järjestusest pärineb mõõdetud massi ja laengu suhtega aminohappeline järjestus).
Human Protein Atlas (HPA)

Andmebaas HPA[139] loodi mitme Rootsi teadusasutuse eestvedamisel: Kuninglik Tehnikainstituut (KTH), Uppsala Ülikool, Science for Life Laboratory (SciLifeLab) ja Karolinska Instituut. Kui eespool käsitletud UniProt sisaldab andmeid mitmesuguste organismide valkude kohta, siis HPA keskendub just inimese proteoomile ning sisaldab hulgaliselt mikroskoopiapilte valkude kohta kudede ja rakkude kontekstis (selektiivne immunovärving fikseeritud näidistes). Konkreetsemalt vaadeldakse järgmisi detaile (vt nt sissekanne inimese epidermaalse kasvufaktori retseptori kohta):[140]
- valgu ja sellele vastava mRNA ekspressioonitase eri elundites üldiselt ning eraldi sissekandena detailselt aju eri osades;
- valgu ja sellele vastava mRNA ekspressioonitase eri elundite kudedes (terved koed), aga ka eri vähkkasvajate kudedes;
- valgu ja sellele vastava mRNA ekspressioonitase enimkasutatavates rakuliinides koos detailse infoga rakusisese lokalisatsiooni kohta igas rakuliinis;
- valgu roll vähipatsientide elumuse prognoosi seisukohalt (st kas valgu kõrgendatud ekspressioonitase on seotud pigem pikenenud või pigem lühenenud elumusega).
Samuti leiab andmebaasist infot konkreetse organi ja koe teadaoleva proteoomi kohta.[141]
HPA andmebaas on ülimalt mugav ressurss teadustööks vajalike selektiivsete antikehade valikuks, aga näiteks ka huvipakkuvate valkude kohta kõrge lahutusega visuaalsete materjalide leidmiseks, mis on sobilikud referaatide ja loengute jaoks. 16. novembri 2022 seisuga sisaldas andmebaas infot kokku 17 268 inimese valgu kohta, mille tuvastamiseks kulus kokku 27 173 selektiivset antikeha (vt statistika andmebaasi kodulehe[139] alumises osas).
Muud andmebaasid

Loomulikult leiab proteoomi kohta hulgaliselt ka spetsiifilisemaid andmebaase, mis keskenduvad valkude iseloomustamisel pigem konkreetsele omadusele. Näiteks:
- Mitme valkude kristallograafiaga tegeleva asutuse ühise jõupingutusena rajatud Protein Data Bank (PDB)[142] sisaldab infot eri organismide valkude 3D-struktuuride kohta. Valdav osa nendest struktuuridest on mõõdetud erinevate eksperimentaalsete meetodite abil (põhiliselt röntgendifraktsioonanalüüs, aga ka tuumamagnetresonantsspektroskoopia, neutrondifraktsioon, elektronmikroskoopia jms). Hiljuti on PDB-sse lisandunud ka arvutuslike algoritmide abil (eriti AlphaFold)[32][33] modelleeritud 3D-struktuurid. Uute valkude kristallograafiaalaste uurimistööde tulemuste avaldamisel on paljud teadusajakirjad seadnud kohustuslikuks kriteeriumiks eksperimentaalsete andmete üleslaadimist PDB andmebaasi, kuna see tagab ühtlasi andmete usaldusväärsust ja avatust.
- Uute suuremahuliste proteoomikaalaste uurimistööde tulemuste publitseerimisel on paljud teadusajakirjad seadnud kohustuslikuks kriteeriumiks eksperimentaalsete andmete üleslaadimise andmebaasi ProteomicsDB.[143] See Müncheni Tehnikaülikooli ja Cellzome GmbH koostöös välja töötatud andmebaas koondab massispektromeetriliste uuringute andmeid inimese, koduhiire, hariliku müürlooga ja hariliku riisi proteoomide kohta. Lisaks andmehoidla rollile võimaldab ProteomicsDB võrrelda oma katsete andmeid varasematega, teha andmeanalüüse ning visualiseerida suuremahulisi andmemassiive.
- Kinexus Bioinformatics Corporationi välja töötatud andmebaasid KinaseNET[144] ja PhosphoNET[145] keskenduvad inimorganismi teatud ensüümidele – proteiinkinaasidele. KinaseNET võimaldab muuhulgas otsida teatud proteiinkinaasi teadaolevaid substraate ning PhosphoNET võimaldab – vastupidi – otsida fosforüülitud järjestuste jaoks substraatides kõige tõenäolisemaid proteiinkinaase. Nende andmebaaside puuduseks on asjaolu, et arendaja on lõpetanud KinaseNET ja PhosphoNET aktiivse värskendamise 2019. aastal, mistõttu värskemate teadusuuringute tulemused ei ole nendesse jõudnud.
- Kopenhaageni Ülikooli teadlaste välja töötatud andmebaas GPCRdb[146] keskendub G-valguga seotud retseptoritele (GPCR) ja nende ligandidele (nii looduslikele kui sünteetilistele). Proteoomi seisukohalt on märksõnadeks GPCR struktuuri eri tasemed ja viisid nende visualiseerimiseks, evolutsiooni käigus tekkinud erisused (fülogeneetilised puud), geneetiline variatiivsus, mutatsioonide analüüs jms.
Rohkem infot proteoomika ja farmakoloogia seostest ning asjakohaste infoallikate viiteid[147] leiab näiteks Rahvusvaheline Põhi- ja Kliinilise Farmakoloogia Liidu ning Briti Farmakoloogiaseltsi koostatud andmebaasi juhendis.[148] Eestikeelsetest materjalidest tutvustab andmebaase laiemalt (sh proteoomikaga seotud andmebaase) Tartu Ülikooli bioinformaatika professori Hedi Petersoni avalik inauguratsiooniloeng. Loengus antakse muuhulgas ülevaade ka genoomika ja proteoomika andmeanalüüsi aluspõhimõttetest (nt BLAST-algoritmi jaoks olulist PAM-maatriksist) ning bioinformaatika lühiajaloost.[149]
Remove ads
Viited
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads
