
Acide borique
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Cher Wikiwand IA, Faisons court en répondant simplement à ces questions clés :
Pouvez-vous énumérer les principaux faits et statistiques sur Acide borique?
Résumez cet article pour un enfant de 10 ans
L'acide borique, aussi appelé acide boracique ou acide orthoborique, est un composé chimique de formule brute H3BO3 ou structurelle B(OH)3, nommé autrefois sassoline en Italie centrale, où il jaillit à l'état naturel dans les fumerolles brûlantes et se dépose avec les autres vapeurs condensées dans les lagoni de Toscane[6]. Ce solide blanc, parfois légèrement coloré, cristallise dans un réseau triclinique. Il se présente sous forme d'un solide cristallisé en paillettes nacrées.
| Acide borique | |
 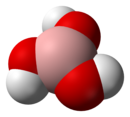 Représentations de la molécule d'acide borique |
|
| Identification | |
|---|---|
| Nom UICPA | acide borique borate d'hydrogène |
| Synonymes |
acide boracique |
| No CAS | 10043-35-3 |
| No ECHA | 100.030.114 |
| No CE | 233-139-2 |
| Code ATC | S02AA03 D08AD |
| PubChem | 7628 |
| ChEBI | 33118 |
| No E | E284 |
| SMILES | |
| InChI | |
| Apparence | cristaux incolores ou poudre blanche sans odeur[1] |
| Propriétés chimiques | |
| Formule | H3BO3 [Isomères] |
| Masse molaire[2] | 61,833 ± 0,008 g/mol H 4,89 %, B 17,48 %, O 77,63 %, |
| pKa | 9,28 à 24,85 °C pour B(OH)3 / B(OH)4−, puis 10,7 et 13,8 pour les deux derniers couples acide-base |
| Propriétés physiques | |
| T° fusion | transformation par transition d'ordre 2 entre 169 °C et 171 °C en acide métaborique HBO2, décomposition à 185 °C, formation de B2O3 à 300 °C |
| Solubilité | 47,2 g·l-1 (eau, 20 °C)[3] |
| Masse volumique | 1,435 g·cm-3 à 15 °C[4] |
| Pression de vapeur saturante | 2,7 mbar à 20 °C[3] |
| Thermochimie | |
| S0gaz, 1 bar | 295,23 J mol−1 K |
| S0solide | 88,7 J mol−1 K |
| ΔfH0gaz | -992,28 kJ mol−1 |
| ΔfH0solide | -1 093,99 kJ mol−1 |
| Cristallographie | |
| Système cristallin | Triclinique |
| Propriétés optiques | |
| Indice de réfraction | cristaux polyaxes, soit 1,337, 1,461 et 1,462 |
| Précautions | |
| SGH[3] | |
| H360FD H360FD : Peut nuire à la fertilité. Peut nuire au fœtus. |
|
| SIMDUT[5] | |
 D2A, D2A : Matière très toxique ayant d'autres effets toxiques Divulgation à 0,1 % selon les critères de classification |
|
| Peau | irritations possibles |
| Yeux | irritations possibles |
| Ingestion | Toxique. Vomissements et diarrhée à petites doses, fatal à hautes doses |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Assez peu soluble dans l'eau, c'est un acide faible. Il est souvent employé comme antiseptique bien que toxique, insecticide, absorbeur de neutrons dans les centrales nucléaires pour contrôler le taux de fission de l'uranium, et comme précurseur d'autres composés chimiques. Cet acide de Lewis tire son nom de l'un de ses composants, le bore, sa formule brute est H3BO3 ou en respectant mieux la structure à liaisons covalentes B(OH)3.
L'acide borique moléculaire peut provenir de la simple décomposition du minéral naturel nommée sassolite qui, décrit par sa formule B(OH)3, n'est qu'un assemblage de plans d'acide borique stabilisés par des liaisons hydrogène[7]. Il existe sous forme de cristaux incolores ou de poudre blanche se dissolvant dans l'eau.
