Loading AI tools
composé chimique De Wikipédia, l'encyclopédie libre
La proline (abréviations IUPAC-IUBMB : Pro et P) est un acide α-aminé dont l'énantiomère L est l'un des 22 acides aminés protéinogènes, encodé sur les ARN messagers par les codons CCU, CCC, CCA et CCG. C'est le seul acide aminé protéinogène ayant une amine secondaire et non primaire, ce qui lui confère une géométrie particulière tendant à interrompre les structures secondaires des protéines telles que les hélices α et les feuillets β.
| Proline | |
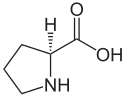 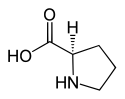 L ou S(–)-proline et D ou R(+)-proline |
|
| Identification | |
|---|---|
| Nom UICPA | acide pyrrolidine-2-carboxylique |
| Synonymes |
P, Pro |
| No CAS | (racémique) (L) ou S(–) (D) ou R(+) |
| No ECHA | 100.009.264 |
| No CE | 205-702-2 (L) |
| FEMA | 3319 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C5H9NO2 [Isomères] |
| Masse molaire[1] | 115,130 5 ± 0,005 4 g/mol C 52,16 %, H 7,88 %, N 12,17 %, O 27,79 %, |
| pKa | 1,95 - 10,64 |
| Propriétés biochimiques | |
| Codons | CCA, CCU, CCG, CCC |
| pH isoélectrique | 6,30[2] |
| Acide aminé essentiel | non |
| Occurrence chez les vertébrés | 5,0 %[3] |
| Précautions | |
| SIMDUT[4] | |
Produit non contrôlé |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La proline forme des résidus apolaires qui en polymérisant peuvent former divers types de protéines dans une famille dite des polyprolines.
La présence de nombreux résidus de proline peut être à l'origine d'une hélice à proline; c'est notamment le cas du collagène. Le cycle de la proline est presque plan. Cela peut être montré en considérant les angles de liaison dans ce cycle[5].
La proline intervient notamment dans la synthèse du collagène, qui possède la séquence (Gly–Pro–Hyp)n et la cicatrisation.
La proline est impliquée dans la bonne germination des graines, la floraison et d'autres phases de développement des plantes[6].
On a constaté des accumulations de proline chez de nombreuses d'espèces végétales quand elles étaient exposées à divers types de stress environnementaux, dont le stress hydrique chez la tomate et la betterave sucrière (sécheresse)[6],[7],[8].
Un nombre croisant de preuves plaident pour une corrélation positive entre ces accumulations et la gestion métabolique de ces stress par les plantes. Elle a un rôle d'osmolyte, mais elle est aussi un chélateur de métaux et a des propriétés antioxydantes: « Appliquée de manière exogène et à faibles doses, elle améliore la tolérance au stress chez les plantes », « la proline exogène atténue le stress salin en améliorant les activités antioxydantes, en réduisant l'absorption du sel tout en améliorant l'assimilation du potassium » chez la tomate, le concombre, les oignons[9],[10],[11].
Plusieurs auteurs ont aussi noté des effets indésirables à des doses plus élevées[6]. Une publication brésilienne (2019) a déterminé le juste dosage en proline des applications aux tomates cultivés en serre affectées par des températures élevées[12].
La proline contient dans sa molécule une fonction amine secondaire cyclique.
Un autre acide aminé, l'hydroxyproline, dérive de la proline par hydroxylation en 4.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.