| 2-Méthylpropane |
|
|
  |
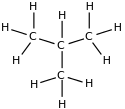
| Structure et représentations de l'isobutane |
| Identification |
| Nom UICPA
|
2-méthylpropane
|
| Synonymes
|
i-butane, triméthylméthane,
1,1-diméthyléthane, méthylpropane, réfrigérant R600a, Greenfreeze
|
| No CAS
|
75-28-5
|
| No ECHA
|
100.000.780 |
| No CE
|
200-857-2
|
| PubChem
|
6360
|
| SMILES
|
|
| InChI
|
InChI : vue 3D InChI =1S/C4H10/c1-4(2)3/h4H,1-3H3 |
| Apparence
|
gaz comprimé liquéfié incolore, d'odeur caractéristique[1]
|
| Propriétés chimiques |
| Formule
|
C4H10 [Isomères]
|
| Masse molaire[2]
|
58,122 2 ± 0,003 9 g/mol
C 82,66 %, H 17,34 %,
|
| Moment dipolaire
|
0,132 ± 0,002 D[3]
|
| Propriétés physiques |
| T° fusion
|
−159,42 °C[4]
|
| T° ébullition
|
−11,7 °C[4]
|
| Solubilité
|
48,9 mg l−1 (eau, 25 °C),
sol. dans l'éthanol, l'éther, le chloroforme[5]
|
| Masse volumique
|
2,506 kg m−3 (15 °C, 1 bar)[4]
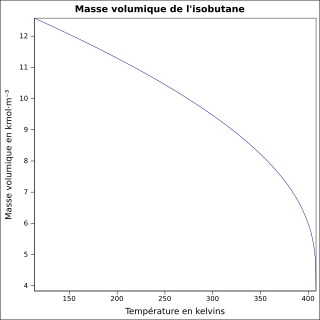
équation[6] : 
Masse volumique du liquide en kmol·m-3 et température en kelvins, de 113,54 à 408,14 K.
Valeurs calculées :
0,5523 g·cm-3 à 25 °C.
| T (K) |
T (°C) |
ρ (kmol·m-3) |
ρ (g·cm-3) |
|---|
| 113,54 |
−159,61 |
12,575 |
0,7309 |
| 133,18 |
−139,97 |
12,29913 |
0,71486 |
| 143 |
−130,15 |
12,15829 |
0,70668 |
| 152,82 |
−120,33 |
12,01528 |
0,69836 |
| 162,64 |
−110,51 |
11,86997 |
0,68992 |
| 172,46 |
−100,69 |
11,72221 |
0,68133 |
| 182,28 |
−90,87 |
11,57183 |
0,67259 |
| 192,1 |
−81,05 |
11,41864 |
0,66369 |
| 201,92 |
−71,23 |
11,26243 |
0,65461 |
| 211,74 |
−61,41 |
11,10297 |
0,64534 |
| 221,56 |
−51,59 |
10,93998 |
0,63586 |
| 231,38 |
−41,77 |
10,77317 |
0,62617 |
| 241,2 |
−31,95 |
10,60218 |
0,61623 |
| 251,02 |
−22,13 |
10,4266 |
0,60603 |
| 260,84 |
−12,31 |
10,24597 |
0,59553 |
|
| T (K) |
T (°C) |
ρ (kmol·m-3) |
ρ (g·cm-3) |
|---|
| 270,66 |
−2,49 |
10,05973 |
0,5847 |
| 280,48 |
7,33 |
9,86721 |
0,57351 |
| 290,3 |
17,15 |
9,6676 |
0,56191 |
| 300,12 |
26,97 |
9,45994 |
0,54984 |
| 309,94 |
36,79 |
9,24298 |
0,53723 |
| 319,76 |
46,61 |
9,01517 |
0,52399 |
| 329,58 |
56,43 |
8,77449 |
0,51 |
| 339,4 |
66,25 |
8,51819 |
0,4951 |
| 349,22 |
76,07 |
8,24246 |
0,47908 |
| 359,04 |
85,89 |
7,9417 |
0,4616 |
| 368,86 |
95,71 |
7,60708 |
0,44215 |
| 378,68 |
105,53 |
7,22331 |
0,41984 |
| 388,5 |
115,35 |
6,75934 |
0,39287 |
| 398,32 |
125,17 |
6,12967 |
0,35627 |
| 408,14 |
134,99 |
3,833 |
0,22279 |
|
|
| T° d'auto-inflammation
|
460 °C[4]
|
| Point d’éclair
|
−83 °C[4]
|
| Limites d’explosivité dans l’air
|
1,5 à 8,3 %vol
37 à 231 g m−3[4]
|
| Pression de vapeur saturante
|
52,132 kPa à −27,57 °C[5]
3,019 bar à 20 °C
4,1 bar à 30 °C
6,78 bar à 50 °C[4]
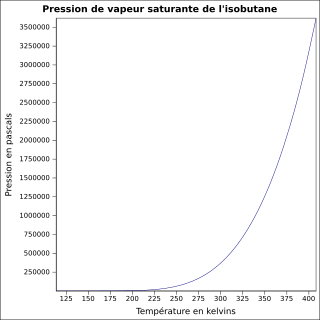
équation[6] : 
Pression en pascals et température en kelvins, de 113,54 à 408,14 K.
Valeurs calculées :
351 798,61 Pa à 25 °C.
| T (K) |
T (°C) |
P (Pa) |
|---|
| 113,54 |
−159,61 |
0,014 |
| 133,18 |
−139,97 |
1,29 |
| 143 |
−130,15 |
7,3 |
| 152,82 |
−120,33 |
31,85 |
| 162,64 |
−110,51 |
113,05 |
| 172,46 |
−100,69 |
339,06 |
| 182,28 |
−90,87 |
885,22 |
| 192,1 |
−81,05 |
2 059,47 |
| 201,92 |
−71,23 |
4 350,01 |
| 211,74 |
−61,41 |
8 467,8 |
| 221,56 |
−51,59 |
15 378,02 |
| 231,38 |
−41,77 |
26 316,72 |
| 241,2 |
−31,95 |
42 792,38 |
| 251,02 |
−22,13 |
66 574,43 |
| 260,84 |
−12,31 |
99 672,51 |
|
| T (K) |
T (°C) |
P (Pa) |
|---|
| 270,66 |
−2,49 |
144 311,04 |
| 280,48 |
7,33 |
202 903,24 |
| 290,3 |
17,15 |
278 028,2 |
| 300,12 |
26,97 |
372 413,61 |
| 309,94 |
36,79 |
488 925,77 |
| 319,76 |
46,61 |
630 567,58 |
| 329,58 |
56,43 |
800 484,82 |
| 339,4 |
66,25 |
1 001 980,23 |
| 349,22 |
76,07 |
1 238 535,09 |
| 359,04 |
85,89 |
1 513 837,46 |
| 368,86 |
95,71 |
1 831 816,73 |
| 378,68 |
105,53 |
2 196 683,82 |
| 388,5 |
115,35 |
2 612 976,69 |
| 398,32 |
125,17 |
3 085 611,2 |
| 408,14 |
134,99 |
3 619 900
|
|
 |
| Point critique
|
3 650 kPa[7], 134,65 °C[8]
|
| Thermochimie |
| S0liquide, 1 bar
|
200,79 J mol−1 K−1[9]
|
| ΔfH0gaz
|
−134,2 kJ mol−1[9]
|
| ΔfusH°
|
4,54 kJ mol−1 à −159,41 °C[9]
|
| ΔvapH°
|
19,99 kJ mol−1 à 25 °C
21,297 kJ mol−1 à −11,71 °C[9]
|
| Cp
|
96,65 J mol−1 K−1 (25 °C, gaz)
129,7 J mol−1 K−1 (−13,15 °C, liquide)[9]
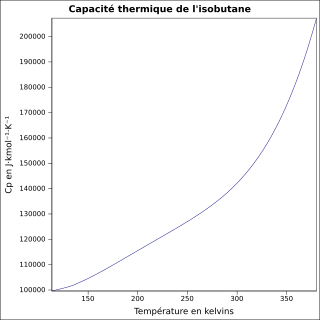
équation[6] : 
Capacité thermique du liquide en J·kmol-1·K-1 et température en kelvins, de 113,54 à 380 K.
Valeurs calculées :
141,432 J·mol-1·K-1 à 25 °C.
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 113,54 |
−159,61 |
99 610 |
1 714 |
| 131 |
−142,15 |
101 350 |
1 744 |
| 140 |
−133,15 |
102 739 |
1 768 |
| 149 |
−124,15 |
104 365 |
1 796 |
| 157 |
−116,15 |
105 959 |
1 823 |
| 166 |
−107,15 |
107 871 |
1 856 |
| 175 |
−98,15 |
109 864 |
1 890 |
| 184 |
−89,15 |
111 902 |
1 925 |
| 193 |
−80,15 |
113 958 |
1 961 |
| 202 |
−71,15 |
116 014 |
1 996 |
| 211 |
−62,15 |
118 061 |
2 031 |
| 220 |
−53,15 |
120 098 |
2 066 |
| 229 |
−44,15 |
122 136 |
2 101 |
| 237 |
−36,15 |
123 962 |
2 133 |
| 246 |
−27,15 |
126 058 |
2 169 |
|
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 255 |
−18,15 |
128 232 |
2 206 |
| 264 |
−9,15 |
130 530 |
2 246 |
| 273 |
−0,15 |
133 005 |
2 288 |
| 282 |
8,85 |
135 721 |
2 335 |
| 291 |
17,85 |
138 749 |
2 387 |
| 300 |
26,85 |
142 172 |
2 446 |
| 308 |
34,85 |
145 618 |
2 505 |
| 317 |
43,85 |
150 040 |
2 581 |
| 326 |
52,85 |
155 143 |
2 669 |
| 335 |
61,85 |
161 043 |
2 771 |
| 344 |
70,85 |
167 868 |
2 888 |
| 353 |
79,85 |
175 751 |
3 024 |
| 362 |
88,85 |
184 838 |
3 180 |
| 371 |
97,85 |
195 282 |
3 360 |
| 380 |
106,85 |
207 250 |
3 566 |
|
équation[10] : 
Capacité thermique du gaz en J·mol-1·K-1 et température en kelvins, de 200 à 1 500 K.
Valeurs calculées :
98,636 J·mol-1·K-1 à 25 °C.
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 200 |
−73,15 |
70 695 |
1 216 |
| 286 |
12,85 |
95 306 |
1 640 |
| 330 |
56,85 |
107 190 |
1 844 |
| 373 |
99,85 |
118 334 |
2 036 |
| 416 |
142,85 |
129 008 |
2 220 |
| 460 |
186,85 |
139 443 |
2 399 |
| 503 |
229,85 |
149 163 |
2 566 |
| 546 |
272,85 |
158 413 |
2 726 |
| 590 |
316,85 |
167 393 |
2 880 |
| 633 |
359,85 |
175 701 |
3 023 |
| 676 |
402,85 |
183 553 |
3 158 |
| 720 |
446,85 |
191 122 |
3 288 |
| 763 |
489,85 |
198 075 |
3 408 |
| 806 |
532,85 |
204 600 |
3 520 |
| 850 |
576,85 |
210 848 |
3 628 |
|
T
(K) |
T
(°C) |
Cp
 |
Cp
 |
|---|
| 893 |
619,85 |
216 549 |
3 726 |
| 936 |
662,85 |
221 867 |
3 817 |
| 980 |
706,85 |
226 931 |
3 904 |
| 1 023 |
749,85 |
231 531 |
3 984 |
| 1 066 |
792,85 |
235 807 |
4 057 |
| 1 110 |
836,85 |
239 872 |
4 127 |
| 1 153 |
879,85 |
243 566 |
4 191 |
| 1 196 |
922,85 |
247 011 |
4 250 |
| 1 240 |
966,85 |
250 309 |
4 307 |
| 1 283 |
1 009,85 |
253 340 |
4 359 |
| 1 326 |
1 052,85 |
256 213 |
4 408 |
| 1 370 |
1 096,85 |
259 024 |
4 457 |
| 1 413 |
1 139,85 |
261 681 |
4 502 |
| 1 456 |
1 182,85 |
264 285 |
4 547 |
| 1 500 |
1 226,85 |
266 936 |
4 593 |
|
|
| PCI
|
−2 869 kJ mol−1[9]
|
| Propriétés optiques |
| Indice de réfraction
|
 1,351 8[5] 1,351 8[5]
|
| Précautions |
| SGH[11],[12] |
  Danger H220 : Gaz extrêmement inflammable
Avec > 0,1 % de butadiène :
H220, H340 et H350H220 : Gaz extrêmement inflammable
H340 : Peut induire des anomalies génétiques (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger)
H350 : Peut provoquer le cancer (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger)
|
| SIMDUT[13] |
 
A, B1, A : Gaz comprimé
B1 : Gaz inflammable
Divulgation à 1,0 % selon les critères de classification
|
| NFPA 704 |
|
| Transport |
Code Kemler :23 : gaz inflammable Numéro ONU :1969 : ISOBUTANE Classe :2.1 Étiquette : 2.1 2.1 : Gaz inflammables (correspond aux groupes désignés par un F majuscule); |
| Écotoxicologie |
| LogP
|
2,8[1]
|
| Composés apparentés |
| Autres composés
|
butane
|
|
| Unités du SI et CNTP, sauf indication contraire. |
| modifier |