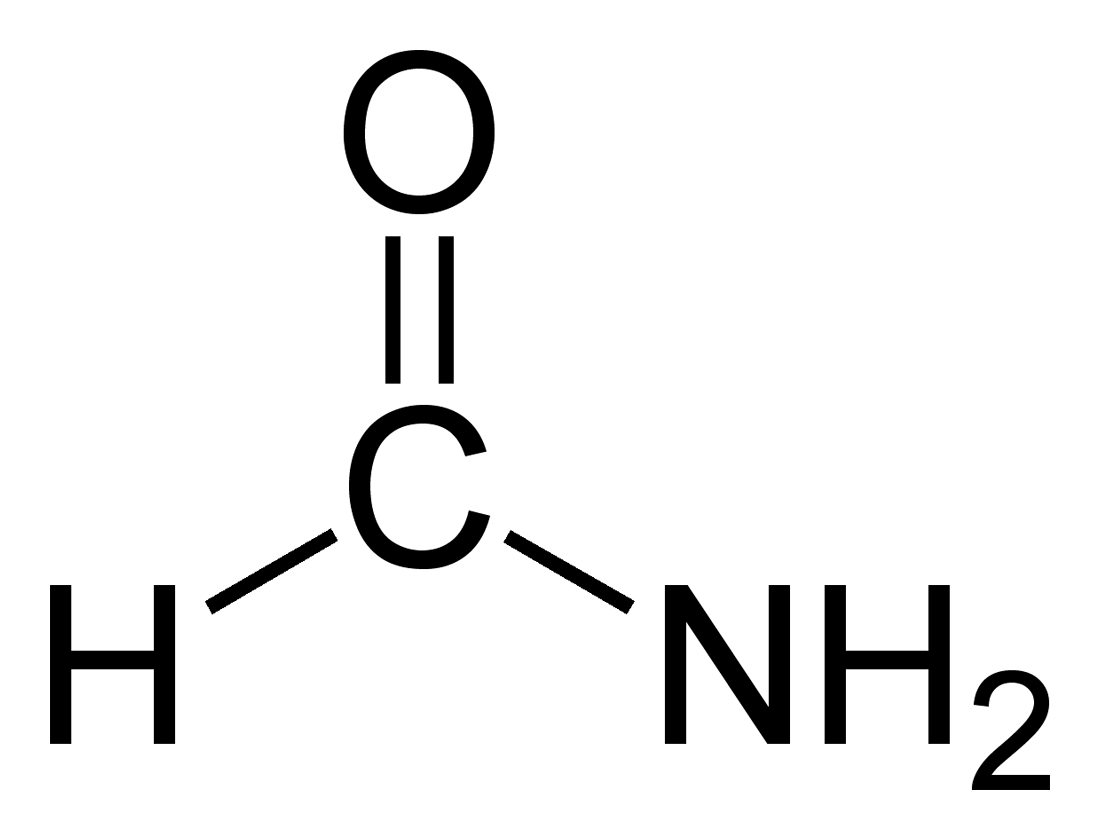
Formamida
composto químico From Wikipedia, the free encyclopedia
Remove ads
A formamida é unha amida derivada do ácido fórmico. É un líquido incoloro inmiscible en auga e cun cheiro parecido ao amoníaco. É a materia prima para a fabricación química de sulfamidas e outros fármacos, herbicidas e pesticidas, e na fabricación de ácido cianhídrico. Foi utilizado como suavizante para o papel e fibras. É un solvente para moitos compostos iónicos. Tamén foi utilizado como solvente para resinas e plastificantes.[4] Algúns astrobiólogos suxiren que pode ser unha alternativa á auga como solvente principal noutras posibles formas de vida no Universo.[5]
As formamidas son compostos do tipo RR′NCHO. Unha formamida importante é a dimetilformamida, (CH3)2NCHO.
Remove ads
Produción
Produción histórica
No pasado a formamida produciase tratando o ácido fórmico con amoníaco, o que produce formato de amonio, que á súa vez rende formamida ao quentalo:[6]
- HCOOH + NH3 → HCOO−
NH+
4 - HCOO−
NH+
4 → HCONH2 + H2O
A formamida tamén se xerou por aminólise de etil formato:[7]
- HCOOCH2CH3 + NH3 → HCONH2 + CH3CH2OH
Produción moderna
O proceso industrial actual para a fabricación de formamida consiste na carbonilación de amoníaco:[4]
- CO + NH3 → HCONH2
Un proceso alternativo en dúas etapas é a amoniólise de metil formato, o cal se forma a partir de monóxido de carbono e metanol:
- CO + CH3OH → HCOOCH3
- HCO2CH3 + NH3 → HCONH2 + CH3OH
Remove ads
Aplicacións
A formamida úsase na produción industrial de cianuro de hidróxeno. Tamén se usa como solvente para procesar varios polímeros como o poliacrilonitrilo.[8]
Reaccións
A formamida descomponse en monóxido de carbono e amoníaco cando se quenta por riba dos 100 °C.
- HCONH2 → CO + NH3
A reacción é lenta por debaixo dos 160 °C, pero acelera de aí en adiante. A temperaturas moi altas, os produtos de reacción cambian a cianuro de hidróxeno (HCN) e auga:
- HC(O)NH2 → HCN + H2O
O mesmo efecto ocorre en presenza de catalizadores de ácido sólido.[8]
Nicho ou aplicacións de laboratorio
A formamida é un constituínte de mesturas crioprotectoras de vitrificación usadas para a crioconservación de tecidos e órganos.
A formamida tamén se usa como estabilizador do ARN en electroforese en xel para desionizar o ARN. Na electroforese de capilaridade, utilízase para estabilizar febras monocatenarias de ADN desnaturalizado.
Outro uso é engadila en solución sol-xel para evitar o craqueo durante a sinterización.
A fomamida no seu estado puro foi utilizada como un solvente alternativo para a autoensamblaxe electrostática de nanopelículas de polímeros.[9]
A formamida úsase para preparar aminas primarias directamente e cetonas por medio de derivados N-formil, usando a reacción de Leuckart.
Remove ads
Bioquímica

As formamidas son intermediarios no ciclo da metanoxénese.
Química prebiótica
- Artigo principal: Química prebiótica baseada na formamida.
A formamida propúxose como solvente alternativo á auga, quizais pola súa capacidade de soportar a vida noutras partes do Universo con bioquímicas alternativas ás que se encontran actualmente na Terra. Fórma pola hidrólise do cianuro de hidróxeno. Ten un gran momento dipolar, e as súas propiedades de solvatación son similares ás da auga.[11]
A formamida pode converterse en trazas de guanina ao quentala en presenza de luz ultravioleta.[12]
Demostrouse que varias reaccións químicas prebióticas que producen derivados de aminoácidos poden ter lugar en formamida.[13]
Seguridade
Non se recomenda o contacto coa pel e os ollos. Cunha LD50 de gramos por kg, a formamida ten unha toxicidade aguda baixa. Tamén ten unha baixa mutaxenicidade.[8]
A formamida clasifícase como tóxica para a saúde reprodutora.[14]
Notas
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads