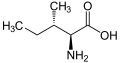
Isoleucina
composto químico From Wikipedia, the free encyclopedia
Remove ads
A isoleucina (abreviadamente Ile ou I)[1] é un α-aminoácido coa fórmula HO2CCH(NH2)CH(CH3)CH2CH3. É un aminoácido esencial, que os humanos non poden sintetizar, polo que debe estar incluído nos alimentos da nosa dieta. Os seus codóns son AUU, AUC e AUA.

Presenta como cadea lateral unha cadea hidrocarbonada alífática ramificada, polo que se clasifica como aminoácido hidrofóbico ou non polar. Xunto coa treonina, a isoleucina é un dos dous aminoácidos que presentan quiralidade na súa cadea lateral. Existen teoricamente catro estereoisómeros posibles da isoleucina, entre eles dous posibles diastereoisómeros da L-isoleucina. Pero na natureza existe só nunha única forma, o enantiómero ácido (2S,3S)-2-amino-3-metilpentanoico. O aminoácido leucina é tamén igual á isoleucina pero cos grupos -CH3 colocados no extremo da cadea.
Remove ads
Biosíntese
Como é un aminoácido esencial os animais non poden sintetizala, polo que debe ser tomada na dieta, xeralmente como compoñente das proteínas. Nas plantas e microorganismos, sintetízase en varios pasos a partir do ácido pirúvico e do alfa-cetoglutarato. Os encimas implicados nesta biosíntese son:[2]
- Acetolactato sintase (tamén chamada acetohidroxiácido sintase).
- Acetohidroxiácido isomeroredutase.
- Dihidroxiácido deshidratase.
- Valina-3-metil-2-oxovalerato transaminase ou valina aminotransferase.
Remove ads
Síntese
A isoleucina pode sintetizarse industrialmente nun proceso de múltiples fases a partir do 2-bromobutano e dietilmalonato.[3] A isoleucina sintética coñécese deste 1905.[4]
Catabolismo
A isoleucina é un aminoácido tanto glicoxénico coma cetoxénico. Despois de transaminarse co alfa-cetoglutarato o seu esqueleto carbonado pode converterse tanto en succinil-CoA coma en acetil-CoA. Cando se converte en succinil-CoA, este entra no ciclo do ácido cítrico para a súa conversión en oxalacetato para a gliconeoxénese (por tanto, é glicoxénico). Cando se converte en acetil-CoA, este pode entrar no ciclo do ácido cíclico ao condensarse co oxalacetato para formar citrato, pero tamén pode usarse para a síntese de ácidos graxos e corpos cetónicos (por tanto, é tamén cetoxénico).
A biotina, tamén denominada ás veces vitamina B7 é imprescindible para o catabolismo da isoleucina (e da leucina). Sen ela o organismo humano non podería degradar completamente a isoleucina e a leucina [5]. A carencia de biotina e a mala degradación da isoleucina pode levar a diversas complicacións fisiolóxicas (relacionadas co mantemento do músculo e a síntese proteica, e metabolismo lipídico) e a trastornos cognitivos orixinados por fallos nas vías metabólicas xerais e os efectos irritantes do hidroxiisovalerato, un subproduto da catabolización incompleta da isoleucina.
Fontes alimenticias
Aínda que este aminoácido non o poden producir os animais, pode almacenarse en grandes cantidades. Alimentos con gran contido de isoleucina son: ovos, proteína de soia, algas, pavo, polo, año, queixo, e peixe.[6]
Notas
Véxase tamén
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads