Timeline
Chat
Prospettiva
Indene
composto chimico Da Wikipedia, l'enciclopedia libera
Remove ads
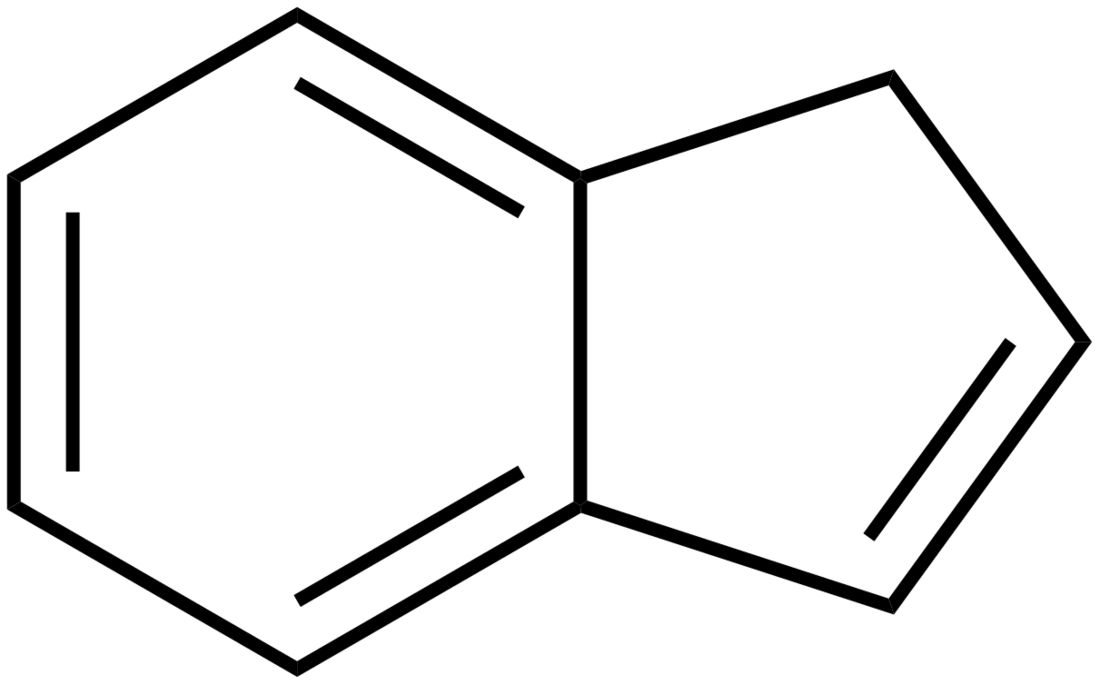
L'indene o 1H-indene è un idrocarburo aromatico biciclico avente formula molecolare C9H8. Esso è composto da un anello benzenico fuso con l'anello pentaatomico del ciclopentadiene, da cui l'altro nome tradizionale benzociclopentadiene.[2] L'indene ha un isomero meno stabile, l'isoindene, con il metilene in posizione 2 (2H-indene).[3]
Remove ads
Presenza in natura
L'indene si trova in natura in frazioni di catrame di carbone bollente intorno a 175-185 °C. Esso può essere ottenuto riscaldando questa frazione con sodio per precipitare il solido "sodio-indene." Questo passaggio sfrutta l'acidità debole dell'indene dimostrata dalla sua deprotonazione da parte del sodio metallico per dare il derivato indenilico. Il sodio-indene viene riconvertito in indene per distillazione in corrente di vapore della miscela.[4]
Remove ads
Proprietà e reattività
Riepilogo
Prospettiva
L'indene è un composto endotermico, ΔHƒ° = +110,6 kJ/mol.[5] In condizioni ambiente si presenta come un liquido incolore se puro, di odore aromatico e infiammabile; praticamente insolubile in acqua ma solubile nei solventi organici. Il principale uso industriale dell'indene è nella produzione di resine termoplastiche indene/benzofurano.[6]
L'indene può polimerizzare (sebbene meno facilmente del ciclopentadiene o dello stirene).[7] Per reazione con sodio in etanolo viene idrogenato ai carboni 2 e 3, dando l'indano C9H10.[8]
La sua ossidazione con acido dicromico porta all'acido omoftalico (acido o-carbossilfenilacetico). Condensa con ossalato di etile in presenza di etossido di sodio per formare l'estere indene-ossalico, e con aldeidi o chetoni in presenza di alcali per formare benzofulveni. Questi ultimi sono molto colorati.
Struttura e aromaticità
Nella molecola dell'indene l'anello benzenico è ovviamente aromatico (6 elettroni π), mentre l'altro, come accade per il ciclopentadiene, è solo potenzialmente tale: il C metilenico è ibridato sp3 e in tal modo impedisce la continuità di coniugazione nell'anello pentaatomico;[9] può divenire aromatico per semplice deprotonazione in ambiente sufficientemente basico a dare il suo anione (C9H7−), anione che è esattamente isoelettronico all'indolo, composto eterociclico aromatico.[10]
Per lo stesso motivo, l'indene è un idrocarburo relativamente acido (pKa ≈ 20),[11] sebbene parecchio meno del ciclopentadiene (pKa = 16),[12] di cui rappresenta il benzoderivato. Nell'anione che in tal modo si forma sono presenti 10 elettroni π, come nel naftalene, quindi con delocalizzazione più estesa che nell'idrocarburo neutro e maggiore stabilità. In conseguenza della sua maggiore acidità, per trattamento con reattivi organolitio, l'indene fornisce i corrispondenti composti litio-indenilici (una reazione di transmetallazione):
C9H8 + R-Li → LiC9H7 + R-H
Per la relativa acidità dei suoui idrogeni metilenici, l'indene è anche il precursore dell'anione indenile o indenuro (C9H7−), un ligando anionico correlato al ciclopentadienuro (Cp) e, come questo, usato in chimica organometallica, dando luogo a vari complessi metallici.[13]
Remove ads
Note
Voci correlate
Altri progetti
Collegamenti esterni
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads