Loading AI tools
ウィキペディアから
グルタミンシンテターゼまたはグルタミン合成酵素 (グルタミンごうせいこうそ、Glutamine synthetase、GS、 EC 6.3.1.2[3]) は、窒素の代謝に必須の役割を果たす酵素で、グルタミン酸とアンモニアの縮合によってグルタミンを合成する反応を触媒する。
| グルタミンシンテターゼ | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 ネズミチフス菌 Salmonella Typhimurium のグルタミンシンテターゼの2つのモノマーの間の活性部位。カチオン結合部位が黄色と橙色、ADPが桃色、ホスフィノスリシン (phosphinothricin) が青色で示されている[1]。 | |||||||||
| 識別子 | |||||||||
| EC番号 | 6.3.1.2 | ||||||||
| CAS登録番号 | 9023-70-5 | ||||||||
| 別名 | グルタミン合成酵素 (glutamine synthetase)、グルタミン酸-アンモニアリガーゼ (glutamate-ammonia ligase) | ||||||||
| データベース | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | metabolic pathway | ||||||||
| PRIAM | profile | ||||||||
| PDB構造 | RCSB PDB PDBj PDBe PDBsum | ||||||||
| 遺伝子オントロジー | AmiGO / QuickGO | ||||||||
| |||||||||
| グルタミンシンテターゼ 触媒ドメイン | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 ネズミチフス菌 Salmonella Typhimurium のグルタミンシンテターゼの12サブニット構造[2]。 | |||||||||||
| 識別子 | |||||||||||
| 略号 | Gln-synt_C | ||||||||||
| Pfam | PF00120 | ||||||||||
| Pfam clan | CL0286 | ||||||||||
| InterPro | IPR008146 | ||||||||||
| PROSITE | PDOC00162 | ||||||||||
| SCOP | 2gls | ||||||||||
| SUPERFAMILY | 2gls | ||||||||||
| |||||||||||
グルタミン酸 (Glutamate) + ATP + アンモニア (NH3) → グルタミン (Glutamine) + ADP + リン酸 (Pi)
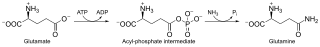
グルタミンシンテターゼ (GS) は硝酸イオンの還元、アミノ酸の分解、光呼吸によって生じたアンモニアを利用する[4]。グルタミンのアミド基が、グルタミンを経由するの代謝産物を合成する際の窒素源となる[5]。
アンモニウムイオンと水分子の競合、それらの結合親和性、アンモニウムイオンの濃度は、グルタミンの合成と加水分解に影響を与える。アンモニウムイオンがアシル-リン酸中間体を攻撃したときにはグルタミンが形成され、水分子が攻撃したときにはグルタミン酸が再形成される[6][7]。カチオンと負に帯電したポケットの間の静電的な力のため、アンモニウムイオンは水分子よりも強くGSへ結合する[4]。他の反応としては、アンモニウムイオン (NH4+) ではなくヒドロキシルアミン (NH2OH) がGSに結合し、γ-グルタミルヒドロキサム酸 (γ-glutamylhydroxamate) が生じる反応が考えられる[6][7]。

GSは、8、10、または12の同一のサブユニットから構成され、2層のリング構造が互いに向かい合って結合した形状をしている[6][8][9][10]。細菌のGSは十二量体であり、それぞれのモノマー間に計12個の活性部位が存在する[6]。各活性部位は、3つの異なる基質(ヌクレオチド、アンモニウムイオン、アミノ酸)の結合部位となる「トンネル」を形成している[4][6][10][11]。このトンネルは中央部がくびれた "bifunnel" 構造であり、bifunnelの頂部が外部への開口部となっており、そこにATPが結合する[4]。そして、グルタミン酸は底部に結合する[7]。bifunnelの中央部には、2価カチオン(マンガンイオンMn2+またはマグネシウムイオンMg2+)の結合部位が2つ存在する。1つはATPからグルタミン酸へのリン酸基の転移に関与しており、もう1つはGSの活性型構造を安定させてグルタミン酸の結合を助けている[6]。
GSの2層のリング間の結合は、水素結合と疎水的相互作用によって保たれている。各サブユニットのC末端領域 (helical thong) が、反対側のリングの向かい合ったサブユニットの疎水的領域に入り込み、GSの構造を安定化している。加えて、リングの中央部のチャネルは、リングの両側のサブユニットで形成された4枚の逆平行β-シート構造が6つ並ぶことで構成されている[6]。
GSは、グルタミン酸とアンモニアのATP依存的な縮合反応によるグルタミンの合成を触媒する[4]。ATPの加水分解は、協奏的な二段階反応の1段階目を駆動する[4][6][8]。ATPはグルタミン酸をリン酸化して、ADPとアシル-リン酸中間体であるγ-グルタミルリン酸を形成し、その後に中間体がアンモニアと反応して、グルタミンと無機リン酸が形成される。ADPと無機リン酸はアンモニアが結合してグルタミンが放出されるまで解離しない[6]。
まずATPは活性部位の頂部のカチオン結合部位の近傍に結合し、一方グルタミン酸は活性部位の底部のカチオン結合部位の近傍に結合する[5][7]。ADPの存在によってGSのコンフォメーションの遷移が引き起こされ、γ-グルタミルリン酸が安定化される。この中間体が存在しているときのみ、アンモニウムイオンはGSに強く結合する。結合部位は極性的で溶媒に露出しているため、結合するのはアンモニアよりもアンモニウムイオンである[7]。反応の2段階目では、アンモニウムイオンが脱プロトン化され、アンモニアが中間体を攻撃しグルタミンが形成される[12]。リン酸は活性部位の頂部を通って移動し、グルタミンは底部(2層のリングの間)を通って放出される[7][9]。

GSは主に脳、腎臓、肝臓に存在する[4][10]。脳のGSはグルタミン酸の代謝調節、アンモニアの解毒・同化、神経伝達物質によるシグナルの終結と再生に関与している[4][13]。GSは脳の中で、主にアストロサイトに見つかる[14]。アストロサイトは余剰のアンモニアとグルタミン酸を取り込み、神経を興奮毒性から保護する[13]。高アンモニア環境では、アストロサイトの腫脹が生じる[13][15][16]。ある研究では、アストロサイトの形態の変化によってグルタミン酸作動性領域の周辺でGSの発現が上昇し、高レベルのグルタミン酸とアンモニアを減少させる適応が起こることが示されている[13]。また他の研究では、アストロサイトの腫脹はグルタミンの蓄積によるものとされ、高アンモニアによる皮質組織の水分量の増加は、L-メチオニン-S-スルホキシイミンによってGSを阻害することで抑制された[15]。
GSは3つの異なるクラスに分類される[17][18][19]。
植物は2つ以上のGSIIを持っており、アイソザイムの1つは葉緑体へ移動する。他のものは細胞質に位置する。細胞質のGSの遺伝子の翻訳は5'UTRで調節されており、3'UTRは転写産物のターンオーバーに関与する[22]。
GSの3つのクラスは明らかに構造的関連性があるが、配列類似性はあまり高くない。
GSの調節は原核生物でのみ行われる[24]。GSは可逆的な共有結合修飾を受ける。12のサブユニットのチロシン残基に対し、二機能性の調節酵素であるアデニリルトランスフェラーゼ (adenylyl transferase、AT) によってアデニリル化、脱アデニリル化の双方が行われる[24]。アデニリル化は、タンパク質の側鎖にAMPを共有結合付加する翻訳後修飾である。アデニリル化にはATPを必要とし、GSの完全な阻害には12分子のATPが必要である。ATによる脱アデニリル化は、チロシン残基に結合したアデニリル基を加リン酸分解し、ADPとして解離させる。ATの活性は、ATに結合したPIIと呼ばれる44 kDaの三量体調節タンパク質の影響を受ける[24]。PIIもまたウリジリルトランスフェラーゼ (uridylyl transferase) による翻訳後修飾を受けるため、2状態が存在する。PIIがウリジリル化されていないときはPIIA型となり、AT:PIIA複合体はGSをアデニリル化し不活性化する。PIIがウリジリル化されているときはPIID型となり、AT:PIID複合体はGSを脱アデニリル化し活性化する[24]。AT:PIIA複合体とAT:PIID複合体は、α-ケトグルタル酸とグルタミンによって逆方向のアロステリックな調節を受ける。グルタミンはAT:PIIAを活性化してAT:PIIDを阻害し、アデニリル化によってGSを不活性化する。さらに、グルタミン酸はPIID型からPIIA型への変換を促進する。α-ケトグルタル酸の複合体への影響は、グルタミンの正反対である[24]。グラム陰性細菌の大部分では、GSはアデニリル化による修飾を受ける (一部のシアノバクテリアや緑藻は例外である)[25]。
GSの阻害は、大部分がアミノ酸の結合部位に集中している[6]。阻害剤としては、グルタミンの代謝の結果生じる、トリプトファン、ヒスチジン、カルバモイルリン酸、グルコサミン-6-リン酸、CTP、AMPがある[5][8][26]。また、アラニン、グリシンとセリンがGSのグルタミン酸結合部位に結合し、GDP、AMP、ADPがATP結合部位に結合する[6]。アラニン、グリシンとセリンはアデニリル化されていないGSのグルタミン酸結合部位に結合し、これら4つのアミノ酸は、それらに共通の「主鎖」の原子を利用して結合する[5]。グルタミン酸もグルタミンの代謝産物であり、グルタミン酸はGSの基質であるとともに阻害も行い、GSの調節因子として機能する。各阻害剤は酵素の活性を低下させ、グルタミンの代謝産物がすべての部位に結合すると、GSの活性はほぼ完全に阻害される[8]。阻害を行う入力シグナルが多数存在することで、体内の窒素レベルに応じたGSの繊細な調節が可能となっている。フィードバック調節には脳と他の組織で差異があり、脳以外のGSは、グルタミンやその誘導体によってフィードバック阻害を受けるが、脳のGSは阻害されない[6]。

他の阻害剤としては、次のようなものがある。
今日では多くの合成阻害剤が利用可能である[6]。
大腸菌を用いた研究によって、GSは遺伝子発現も調節されていることが明らかにされた。GSのサブユニットをコードする遺伝子はglnAである。glnAの転写はエンハンサー領域に結合する特異的転写因子NRI (NtrC) に依存し、NRIがリン酸化型のとき転写は活性化される。NRIのリン酸化は、プロテインキナーゼであるNRII (NtrB) によって触媒される。NRIIがPIIAと複合体を形成しているときはホスファターゼとして機能し、NRIは脱リン酸化されてglnAの転写は止まる[24]。
シアノバクテリアには全く異なる調節機構が存在する[27]。上述のNtrC-NtrB二成分制御系の代わりに[28][29]、シアノバクテリアは転写調節因子NtcAを持っている。NtcAはこのクレードのみに存在し、GSや窒素代謝に関与する一群の遺伝子の発現を調節する[30][31]。さらに、シアノバクテリアのGSはフィードバック阻害の感受性を向上させるための共有結合修飾が行われない[29]。代わりに、シアノバクテリアのGSはGS不活性化因子 (GS inactivation factor、IF) と名付けられた低分子量タンパク質によって阻害され、IFの転写はNtcAによって負の制御を受けている[32][33]。これらの不活性化因子はさらにノンコーディングRNAによって調節されている。低分子RNAであるNsiR4はIF7 (gifA) のmRNAの5'UTRと相互作用し、発現を低下させる。NsiR4の発現はNtcAによって正の制御を受けている[34]。加えて、IF17の発現はグルタミンが結合するリボスイッチによって制御されている[35]。
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.