トップQs
タイムライン
チャット
視点
食作用
ウィキペディアから
Remove ads
食作用(しょくさよう、英: phagocytosis[注釈 1]、ファゴサイトーシス)または貪食(どんしょく)は、細胞がその細胞膜を使って大きな粒子(0.5 μm以上)を取り込み、ファゴソーム(食胞)と呼ばれる内部区画を形成するプロセスである。これはエンドサイトーシスの一種である。食作用を行う細胞を食細胞(ファゴサイト)と呼ぶ。



多細胞生物の免疫系では、食作用は病原体や細胞の残骸を異物として除去するための主要な機構である。摂取された物質は、ファゴソーム内で消化される。細菌、ウイルス、死んだ組織細胞、寄生虫、異常な代謝産物、小さな鉱物粒子などが、貪食される可能性のある物質の例である。原生動物の中には、食作用を利用して栄養素を摂取するものがある。
Remove ads
歴史
食作用は、カナダの医師ウィリアム・オスラーが最初に指摘し(1876年)[1]、その後、イリヤ・メチニコフが研究し命名した(1880年と1883年)[2]。
免疫系での食作用
要約
視点
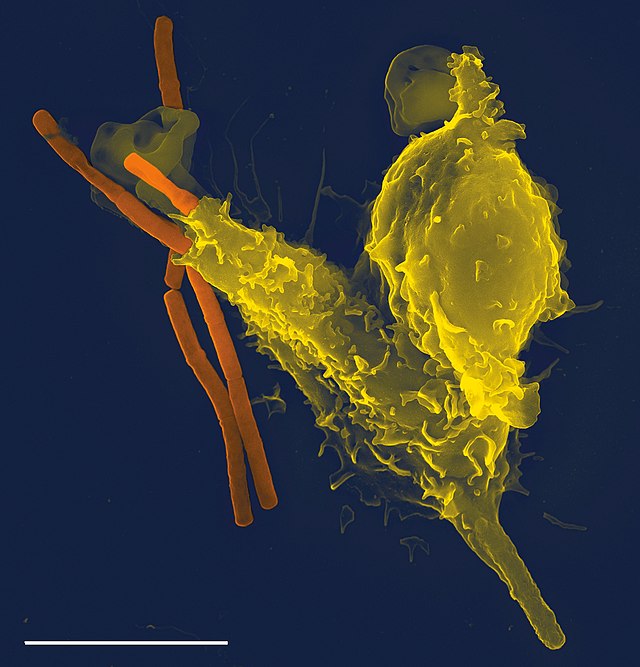
→詳細は「食細胞」を参照
食作用は、自然免疫防御の主要な機構の一つである。これは、感染に応答する最初のプロセスの1つであり、適応免疫応答の開始ブランチの1つでもある。ほとんどの細胞は食作用を行うことができ、一部の細胞は主な機能の一部として食作用を実行する。これらは「プロフェッショナルの食細胞」(professional phagocytes)と呼ばれている。食作用は進化という観点から見ると古く、無脊椎動物にも存在している[3]。
プロフェッショナルの食細胞
好中球、マクロファージ、単球、樹状細胞、破骨細胞、および好酸球は、プロフェッショナルの食細胞として分類される[2]。最初の3つは、ほとんどの感染症に対する免疫応答に最も大きな役割を果たす[3]。
好中球の役割は、血流をパトロールし、感染の場合にのみ大変な数で組織に急速に移動することである[3]。そこでは食作用による直接的な殺傷効果がある。摂取後の好中球は、病原体を細胞内で効率的に殺滅する。好中球は、主にFcγ受容体と補体受容体1および3を介して貪食する。好中球の殺滅効果は、あらかじめ形成された顆粒に存在する分子のたくさんのレパートリーによるものである。この顆粒に用意されている酵素や他の分子は、コラゲナーゼ、ゼラチナーゼ、またはセリンプロテアーゼなどのプロテアーゼ、ミエロペルオキシダーゼ、ラクトフェリン、および抗生物質タンパク質である。これらのファゴソームへの脱顆粒は、高い活性酸素種の産生(呼吸性バースト)を伴い、非常に高い殺菌力がある[4]。
単球やそれが成熟したマクロファージは、血液循環から離れて組織内を移動する。そこでは、これらは常在細胞となり、静止した防壁を形成する[3]。マクロファージは、マンノース受容体、スカベンジャー受容体、Fcγ受容体、補体受容体1、3、4によって食作用を開始する。マクロファージは長寿命で、新たなリソソームを形成することで食作用を継続することができる[3][5]。
また、樹状細胞も組織内に存在し、食作用によって病原体を摂取する。それらの役割は、微生物を殺したり除去することではなく、適応免疫系の細胞に抗原提示するために微生物を分解することである[3]。
食作用を誘発する受容体
食作用のための受容体は、認識される分子によって2つのカテゴリーに分類される。1つ目のオプソニン受容体はオプソニンに依存している[6]。これらの中には、結合したIgG抗体のFc部分を認識する受容体や、細胞や血漿由来の他のオプソニンを認識する沈着した補体や受容体がある。2つ目の非オプソニン受容体には、レクチン様受容体、デクチン受容体、スカベンジャー受容体がある。一部の食細胞経路は、病原体関連分子パターン(PAMPS)への付着によって活性化されたパターン認識受容体(PRR)からの第2のシグナルを必要とし、これによってNF-κBが活性化される[2]。
Fcγ受容体
Fcγ受容体は、IgGでコーティングされた標的を認識する。主に認識される部分はFcフラグメントである。受容体の分子は、細胞内ITAMドメインを持っているか、ITAM含有アダプター分子と結合している。ITAMドメインは、食細胞の表面から核にシグナルを伝達する。たとえば、ヒトマクロファージの活性化受容体には、FcγRI、FcγRIIA、FcγRIIIがある[5]。Fcγ受容体を介した食作用では、「食作用カップ」と呼ばれる細胞の突起が形成され、好中球の酸化的バーストを活性化する[4]。
補体受容体
これらの受容体は、血漿補体からC3b、C4b、およびC3biでコーティングされた標的を認識する。受容体の細胞外ドメインには、レクチン様補体結合ドメインが含まれる。補体受容体による認識だけでは、付加的なシグナルなしで内在化を起こせない。マクロファージでは、CR1、CR3、CR4が標的の認識を担っている。補体でコーティングされた標的は、突起なしで、食細胞膜に「沈み込む」ことで内在化される[5]。
マンノース受容体
マンノースおよびフコースなどの病原体に関連する糖類は、マンノース受容体によって認識される。8つのレクチン様ドメインが受容体の細胞外部分を形成する。マンノース受容体を介した摂取は、Fcγ受容体または補体受容体を介した食作用とは分子メカニズムが異なる[5]。
ファゴソームの分解
物質の飲み込みはアクチン-ミオシン収縮系によって促進される。物質の食作用によってファゴソーム(phagosome、食胞)と呼ばれる細胞小器官が形成される。その後、これは食細胞の中心体に向かって移動し、リソソーム(lysosome、水解小体)と融合してファゴリソソームを形成し分解に至る。ファゴリソソームは次第に酸性化され、分解酵素が活性化する[2][7]。
分解は、酸素依存性または酸素非依存性の2種類がある。
- 酸素依存性分解は、NADPHと活性酸素種の生成に依存する。過酸化水素とミエロペルオキシダーゼがハロゲン化反応を活性化させ、次亜塩素酸塩の生成および細菌の破壊をもたらす[8]。
- 酸素非依存性分解は、リゾチームなどの酵素やディフェンシンなどのカチオン性タンパク質を含む顆粒の放出に依存する。これらの顆粒には他の抗菌ペプチドも存在しており、ラクトフェリンは鉄を補足して細菌にとって好ましくない増殖条件を作り出す。また、ヒアルロニダーゼ、リパーゼ、コラゲナーゼ、エラスターゼ、リボヌクレアーゼ、デオキシリボヌクレアーゼなどの他の酵素も、感染の拡大を妨げ、細胞死につながる必須の微生物生体分子の分解に重要な役割を果たす[4][5]。
白血球は、食作用の際にシアン化水素を生成し、いくつかの他の毒性化学物質を生成することで細菌、真菌、他の病原体を殺滅することができる[9][10][11]。
梅毒トレポネーマ(Treponema pallidum)、大腸菌(Escherichia coli)、黄色ブドウ球菌(Staphylococcus aureus)などの一部の細菌は、いくつかの機構によって食作用を回避することができる[要出典]。
獲得免疫の誘導
→この詳細な機構については「抗原提示細胞」を参照
また、異物の分解産物の一部は細胞膜表面に提示され、これをリンパ球(T細胞)が認識する。このことによりT細胞の分化が生じ、抗原に特異的な免疫である獲得免疫(細胞性免疫あるいは液性免疫)が誘導される[要出典]。
Remove ads
アポトーシスでの食作用
→詳細は「アポトーシス」および「エフェロサイトーシス」を参照
死につつある細胞は、アポトーシスに続いて、エフェロサイトーシスと呼ばれるプロセスで、マクロファージによって周囲の組織に取り込まれる必要がある。アポトーシス細胞の特徴の一つは、カルレティキュリン、ホスファチジルセリン(細胞膜内層から)、アネキシンA1、酸化LDL、変化した糖鎖など、さまざまな細胞内分子が細胞表面に提示されることである[12]。これらの分子は、ホスファチジルセリン受容体のようなマクロファージの細胞表面にある受容体、またはトロンボスポンジン1、GAS6、MFGE8のような可溶性(浮遊)受容体によって認識され、CD36やαVβ3インテグリンのようなマクロファージ上の他の受容体と結合する。アポトーシス細胞のクリアランスの障害は、通常、マクロファージの障害食作用と関連している。アポトーシス細胞の残骸が蓄積すると、しばしば自己免疫疾患を引き起こす。したがって、食作用を薬理学的に増強することは、ある種の自己免疫疾患の治療において医学的な可能性を秘めている[13][14][15][16]。

原生生物での食作用
多くの原生生物では、食作用は栄養の一部または全部を提供する摂食手段として使用される。これは貪食栄養と呼ばれ、吸収によって起こる浸透圧栄養とは区別される[要出典]。
- アメーバなどでは、食細胞と同様に、標的物体を仮足で囲むことによって食作用が起こる。アメーボゾアの一種であるヒトの赤痢アメーバは赤血球を貪食することがある。
- 繊毛虫では細胞内の細胞口と呼ばれる溝または窪みで食作用が起こる [17]。
免疫細胞の場合と同様に、得られたファゴソームは消化酵素を含むリソソームと融合して、ファゴリソソームを形成する可能性がある。次に、食物粒子が消化され、放出された栄養素は、他の代謝プロセスで使用するために細胞質ゾルに拡散または輸送される [18]。
参照項目
脚注
外部リンク
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads
