
Diboraan
chemische stof / Uit Wikipedia, de vrije encyclopedia
Diboraan is het eenvoudigste, min of meer stabiele hydride van boor. Het is het dimeer van monoboraan (BH3), dat niet stabiel is en dimeriseert tot diboraan. Diboraan is het molecule waarvoor het later breder toepasbare concept van de 3-centra-2-elektronbinding is ontwikkeld, waarbij twee waterstofatomen voorkomen als een brug tussen de booratomen.
Snelle feiten Structuurformule en molecuulmodel, Algemeen ...
| Diboraan | |||||
|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | |||||
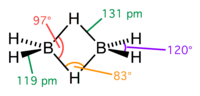 | |||||
Structuurformule van diboraan | |||||
| Algemeen | |||||
| Molecuulformule | B2H6 | ||||
| IUPAC-naam | diboraan | ||||
| Andere namen | boorethaan, boorhydride | ||||
| Molmassa | 27,7 g/mol | ||||
| CAS-nummer | 19287-45-7 | ||||
| EG-nummer | 242-940-6 | ||||
| Wikidata | Q407684 | ||||
| Vergelijkbaar met | boraan | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H330 - H220 - H280 | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P260 - P210 - P304+P340 - P315 - P377 - P381 - P405 - P403 | ||||
| VN-nummer | 1911 | ||||
| Fysische eigenschappen | |||||
| Aggregatietoestand | gasvormig | ||||
| Kleur | kleurloos | ||||
| Dichtheid | (vloeistof bij kookpunt) 0,437 g/cm³ | ||||
| Smeltpunt | −165 °C | ||||
| Kookpunt | −92 °C | ||||
| Zelfontbrandings- temperatuur | 40-50 °C | ||||
| Goed oplosbaar in | THF | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Sluiten
Er is maar één geschikt oplosmiddel voor diboraan bekend, namelijk tetrahydrofuraan (THF). In andere oplosmiddelen is het ofwel onvoldoende oplosbaar, ofwel reageert diboraan ermee. Diboraan reageert ook met THF, zij het langzaam en de oplossing kan gestabiliseerd worden door er een sulfide aan toe te voegen zoals dimethylsulfide.[1]


