Anionorodnik ponadtlenkowy
Z Wikipedii, wolnej encyclopedia
Anionorodnik ponadtlenkowy (O2•−) – jedna z reaktywnych form tlenu (RFT). Powstaje w wyniku redukcji jednoelektronowej tlenu cząsteczkowego, jako uboczny produkt utleniania tkankowego w mitochondriach (reakcje enzymatyczne zachodzące w łańcuchu oddechowym katalizowane przez różne oksydoreduktazy) lub szeregu innych reakcji redoks.
| |||||
| Ogólne informacje | |||||
| Wzór sumaryczny |
O2•− | ||||
|---|---|---|---|---|---|
| Masa molowa |
32,00 g/mol | ||||
| Identyfikacja | |||||
| Numer CAS | |||||
| PubChem | |||||
| |||||
Wiele związków występujących w formie zredukowanej (RH2) reagując z tlenem ulega jednoelektronowemu utlenieniu. Efektem takiego działania jest powstanie anionorodnika ponadtlenkowego O2•− i wolnego rodnika reagującego związku:
- RH2 + O2 → RH• + H+ + O2•−
Reakcje tego typu w komórkach najczęściej prowadzą do powstania anionorodnika ponadtlenkowego i w efekcie odpowiadają za rozwój wielu innych zdarzeń o charakterze wolnorodnikowym. Zredukowane związki głównie biorące udział w tego typu reakcjach zestawiono w tabeli poniżej[1].
| Związki w formie zredukowanej |
|---|
| Ryboflawina |
| Nukleotydy flawinowe (FMNH2, FADH2) |
| Katecholaminy (adrenalina, dopamina, DOPA) |
| Cysteina |
| Glutation |
| Glukoza |
| Sapropteryna |
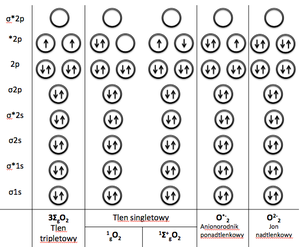
Cząsteczka tlenu O2 w warunkach normalnych występuje w stanie tripletowym (schemat 1). Takie rozmieszczenie elektronów powoduje, że jest ona stosunkowo mało reaktywna. Anionorodnik ponadtlenkowy ma dodatkowy niesparowany elektron obsadzony na orbitalu *2p, który nadaje mu cechę wolnego rodnika. Warto zwrócić uwagę, iż takie rozmieszczenie elektronów w anionorodniku czyni go paramagnetykiem. Do pełnej redukcji cząsteczki tlenu O2 konieczne jest przyłączenie 4 elektronów oraz 4 protonów H+. Schemat 2 przedstawia kolejne etapy redukcji cząsteczki tlenu.
- Schemat 1. Rozkład elektronów na orbitalach molekularnych tlenu
- Schemat 2. Wieloetapowy schemat redukcji tlenu cząsteczkowego