Лучшие вопросы
Таймлайн
Чат
Перспективы
Рецептор, активируемый пероксисомным пролифератором альфа
Из Википедии, свободной энциклопедии
Remove ads
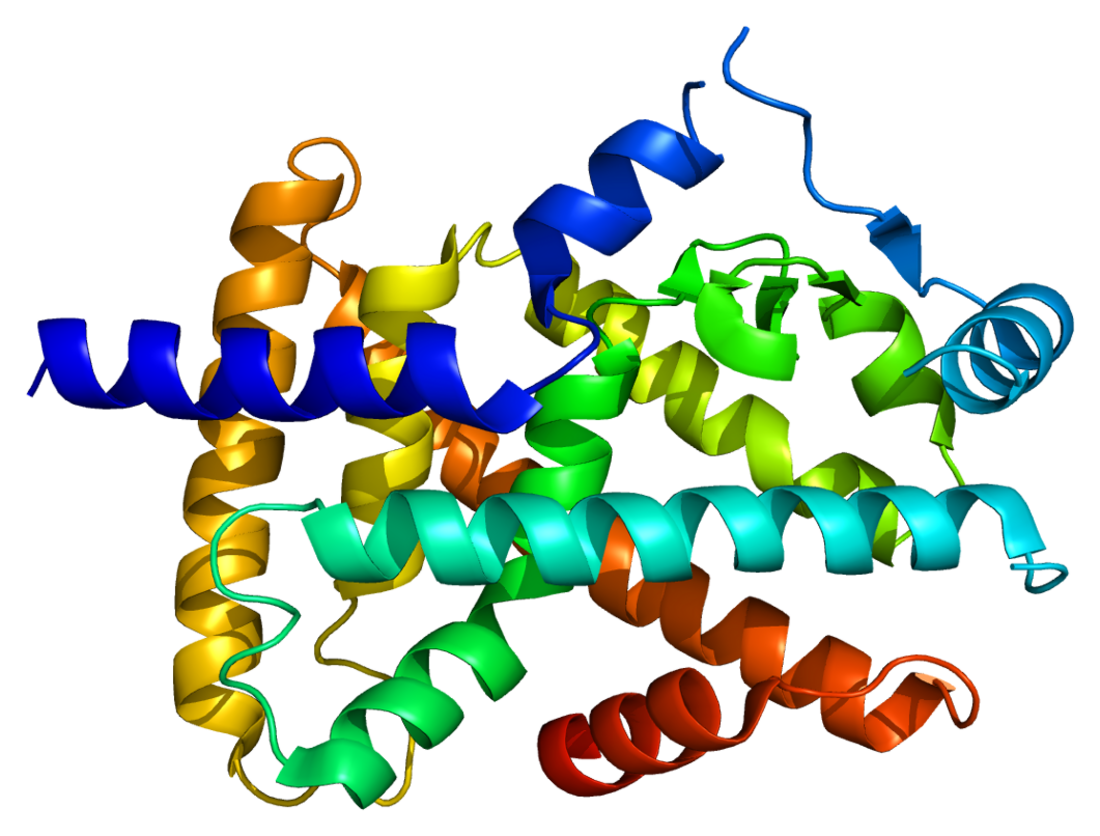
Рецептор, активируемый пероксисомным пролифератором альфа (англ. Peroxisome proliferator-activated receptor alpha, сокр. PPAR-α), также известный как NR1C1 (подсемейство ядерных рецепторов 1, группа C, тип 1) представляет собой белок — ядерный рецептор, функционирующий как транскрипционный фактор, который у человека кодируется геном PPARA, локализованный на длинном плече (q-плече) 22-й хромосомы[5]. Вместе с дельта-рецептором, и гамма-рецептором, активируемые пероксисомным пролифератором, PPAR-альфа является частью подсемейства рецепторов, активируемых пероксисомным пролифератором. Это был первый член семейства PPAR, клонированный в 1990 году Стивеном Грином, и он был идентифицирован как ядерный рецептор разнообразного класса гепатоканцерогенов грызунов, вызывающих пролиферацию пероксисом[6].
Полипептидная цепь белка включает в себя 468 аминокислот, а молекулярная масса составляет — 52225 Да[7].
Remove ads
Экспрессия
PPAR-α в первую очередь активируется посредством связывания лиганда. Эндогенные лиганды включают жирные кислоты, такие как арахидоновая кислота (С20), а также другие полиненасыщенные жирные кислоты и различные соединения, производные жирных кислот, такие как некоторые члены семейства 15-гидроксиэйкозатетраеновой кислоты (15-ГЭТЕ) метаболитов арахидоновой кислоты, например, 15(S)-ГЭТЕ, 15(R)-ГЭТЕ и 15(S)-ГПЭТЕ и 13-гидроксиоктадекадиеновая кислота, метаболит линолевой кислоты. Синтетические лиганды включают фибраты, которые используются для лечения гиперлипидемии, а также разнообразный набор инсектицидов, гербицидов, пластификаторов и органических растворителей, которые вместе называются пролифераторами пероксисом.
Remove ads
Выполняемые функции
PPAR-α — транскрипционный фактор, регулируемый свободными жирными кислотами, и является одним из основных регуляторов липидного обмена в печени[8]. PPAR-альфа активируется в условиях энергетического голодания и необходим для процесса кетогенеза, ключевого адаптивного ответа на длительное голодание[9][10]. Активация PPAR-альфа способствует поглощению, утилизации и катаболизму жирных кислот путём регуляции генов, участвующих в транспорте жирных кислот, связывании и активации жирных кислот, а также в пероксисомальном и митохондриальном β-окислении жирных кислот[11]. Активации окисления жирных кислот способствует повышенная экспрессия CPT1 (который доставляет длинноцепочечные липиды в митохондрии) под действием PPAR-α[12]. PPAR-α также подавляет гликолиз, одновременно способствуя глюконеогенезу и синтезу гликогена в печени[8].
В макрофагах PPAR-α подавляет поглощение гликированного липопротеина низкой плотности (холестерина ЛПНП), препятствует образованию пенистых клеток (атеросклероз) и ингибирует провоспалительные цитокины[12].

Remove ads
Распределение по тканям
Экспрессия PPAR-α наиболее высока в тканях, которые быстро окисляют жирные кислоты. У грызунов самые высокие уровни экспрессии мРНК PPAR-альфа обнаружены в печени и бурой жировой ткани, затем в сердце и почках[13]. Более низкие уровни экспрессии PPAR-альфа обнаружены в тонком и толстом кишечнике, скелетных мышцах и надпочечниках. У человека PPAR-альфа экспрессируется более равномерно в различных тканях, с высокой экспрессией в печени, кишечнике, сердце и почках.
Нокаутные исследования
Исследования, проведенные на мышах, лишённых функциональных PPAR-альфа, показывают, что PPAR-α необходимы для индукции пролиферации пероксисом под действием различных синтетических соединений, называемых пероксисомными пролифераторами[14]. У мышей, лишённых PPAR-альфа, также нарушается реакция на голодание, характеризующаяся серьёзными метаболическими нарушениями, включая низкий уровень кетоновых тел в плазме, гипогликемию и жировую дистрофию печени[9].
Remove ads
Фармакология
Суммиров вкратце
Перспектива
PPAR-α является фармацевтической мишенью фибратов, класса препаратов, используемых для лечения дислипидемии. Фибраты эффективно снижают уровень триацилглицеридов в сыворотке крови и повышают уровень холестерина ЛПВП («хорошего холестерина»)[15]. Хотя клиническая польза от лечения фибратами была отмечена, общие результаты неоднозначны и заставляют сомневаться в широком применении фибратов для лечения ишемической болезни сердца, в отличие от статинов. Агонисты PPAR-α могут иметь терапевтическое значение для лечения неалкогольной жировой болезни печени. PPAR-альфа также может быть местом действия некоторых противосудорожных препаратов[16][17].
Эндогенное соединение, 7(S)-гидроксидокозагексаеновая кислота (7(S)-HDHA, которая является докозаноидным производным омега-3 жирной кислоты DHA, была выделена в качестве эндогенного высокоаффинного лиганда для PPAR-альфа в мозге крыс и мышей. Энантиомер 7(S) связывался с PPAR-альфа с микромолярной аффинностью, в 10 раз более высокой по сравнению с энантиомером (R), и мог вызывать дендритную активацию[18]. Предыдущие доказательства функции этого соединения были умозрительными, основанными на структуре и изучении химического синтеза[19].
Как диеты с высоким содержанием сахара, так и диеты с низким содержанием белка повышают уровень циркулирующего в печени эндокринного FGF21 у людей посредством PPAR-α, хотя этот эффект может сопровождаться FGF21-резистентностью[20].
Remove ads
Гены-мишени
PPAR-α регулирует биологические процессы, изменяя экспрессию большого количества генов-мишеней. Соответственно, функциональная роль PPAR-альфа напрямую связана с биологической функцией его генов-мишеней. Исследования по профилю экспрессии генов показали, что число генов-мишеней PPAR-альфа исчисляется сотнями[11]. Классические гены-мишени PPAR-альфа включают PDK4, ACOX1 и CPT1. Анализ экспрессии генов с низкой и высокой пропускной способностью позволил создать всеобъемлющие карты, иллюстрирующие роль PPAR-альфа как главного регулятора липидного обмена через регуляцию множества генов, вовлечённых в различные аспекты липидного обмена. Эти карты, построенные для печени мыши и человека, ставят PPAR-альфа в центр регуляторного узла, влияющего на поглощение и внутриклеточное связывание жирных кислот, митохондриальное β-окисление и пероксисомальное окисление жирных кислот, кетогенез, обмен триацилглицеридов, глюконеогенез и синтез/секрецию желчи.
Remove ads
Взаимодействия
Было показано, что PPAR-α взаимодействует с:
См. также
Примечания
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads