Amonijum hlorid je neorgansko hemijsko jedinjenje, koje se ubraja u najznačajnije soli amonijaka. Njegova molekulska formula je NH4Cl. Nastaje usled mešanja hlorovodonične kiseline i amonijaka:
- HCl + NH3 → NH4Cl
Kratke činjenice Identifikacija, Svojstva ...
| Amonijum hlorid |
|---|
 |
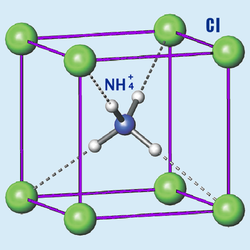 |
| IUPAC ime |
|
| Drugi nazivi |
nišador |
| Identifikacija |
| CAS registarski broj |
12125-02-9 Y |
| ChemSpider[1] |
23807 |
| UNII |
01Q9PC255D Y |
| EINECS broj |
235-186-4 |
| RTECS registarski broj toksičnosti |
BP4550000 |
| Jmol-3D slike |
Slika 1 |
|
|
| Svojstva |
| Molekulska formula |
NH4Cl |
| Molarna masa |
53,491 g/mol |
| Agregatno stanje |
Bela čvrsta supstanca
higroskopna |
| Miris |
bez mirisa |
| Gustina |
1,5274 g/cm3 |
| Tačka topljenja |
338 °C (razlaže se) |
| Rastvorljivost u vodi |
29,7 g/100 mL (0 °C)
37,2 g/100 mL (20 °C)
77,3 g/100 mL (100 °C) |
| Rastvorljivost u alkohol |
0,6 g/100 mL (19 °C) |
| pKa |
9.245 |
| Indeks prelamanja (nD) |
1,642 |
| Termohemija |
Standardna entalpija stvaranja jedinjenja ΔfHo298 |
−314.55 kJ/mol[2] |
Standardna molarna entropija So298 |
94.85 J K−1 mol−1[2] |
| Opasnost |
| Podaci o bezbednosti prilikom rukovanja (MSDS) |
ICSC 1051 |
| EU-klasifikacija |
Škodljiv (Xn)
Iritant (Xi) |
| EU-indeks |
017-014-00-8 |
| NFPA 704 |
|
| R-oznake |
R22, R36 |
| S-oznake |
S2, S22 |
| Tačka paljenja |
Ne gori |
| LD50 |
1650 mg/kg, oralno (pacov) |
| Srodna jedinjenja |
| Drugi anjoni |
Amonijum-fluorid
amonijum-bromid
amonijum-jodid |
| Drugi katjoni |
Natrijum-hlorid
kalijum-hlorid
hidroksilamonijum-hlorid |
|
Y (šta je ovo?)
(verifikuj)
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala |
| Infobox references |
Zatvori
Drugi način za dobijanje amonijum hlorida je:
(NH4)2SO4 + 2NaCl → 2NH4Cl + Na2SO4
Pod normalnim uslovima amonijum hlorida predstavlja beli prah ili bezbojhno kristalno čvrsto telo. Veoma se dobro rastvara u vodi (na sobnoj temperaturi 37 g na 100 g H2O). Ukoliko se podgreje do 335 °C sublimuje delimičnom disocijacijom na hlorovodonik i amonijak. Na temperaturi preko 350 °C disocijacija je stoprocentna.
Temperatura topljenja mu je 338 °C, a temperatura ključanja 520 °C
Amonijum hlorid koristi kao elektrolit u baterijama. Koristi se i kao lek za kašalj, sastojak šampona, dodatak stočnoj hrani ...
Amonijum hlorid je najstarija poznata so amonijaka.
Njegova molekulska masa je 53.4913 u



