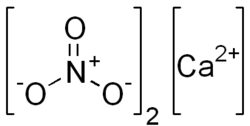
Kalcijum nitrat
From Wikipedia, the free encyclopedia
Remove ads
Kalcijum nitrat (Norveška šalitra), je neorgansko jedinjenje sa formulom Ca(NO3)2.[4][5] Ova bezbojna so apsorbuje vlagu iz vazduha i obično se nalazi u obliku tetrahidrata.
On se uglavnom koristi kao komponenta đubriva mada ima i druge primene. Nitrokalcit je ime minerala koji je po sastavu hidratisani kalcijum nitrat. On se formira kao eflorescens na mestima gde je stajsko đubrivo u kontaktu sa betonom u suvoj sredini. Niz srodnih soli je poznat, među kojima su kalcijum amonijum nitrat dekahidrat i kalcijum kalijum nitrat dekahidrat.[6]
Remove ads
Proizvodnja i reaktivnost
Kalcijum nitrat je bio prvo sintetičko azotno đubrivo. Proizvodnja je počela u Notodenu u Norveškoj 1905. Najveći deo svetske proizvodnje kalcijum nitrata u današnje vreme dolazi iz Porsgruna, Norveška.
On je proizvodi tretiranjem krečnjaka sa azotnom kiselinom, čemu sledi neutralizacija amonijakom:
- CaCO3 + 2 HNO3 → Ca(NO3)2 + CO2 + H2O
On je takođe nuzprodukt nitrofosfatnog procesa za ekstrakciju kalcijum fosfata:
- Ca3(PO4)2 + 6 HNO3 + 12 H2O → 2 H3PO4 + 3 Ca(NO3)2 + 12 H2O
On se može pripremiti iz vodenog rastvora amonijum nitrata, i kalcijum hidroksida:
- 2 NH4NO3 + Ca(OH)2 → Ca(NO3)2 + 2 NH4OH
Poput srodnih zemnoalkalnih metalnih nitrata (kao i LiNO3), kalcijum nitrat se razlaže nakon zagrevanja uz oslobađanje azot dioksida:[6]
- 2 Ca(NO3)2 → 2 CaO + 4 NO2 + O2 ΔH = 369 kJ/mol
Remove ads
Reference
Vanjske veze
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads