Loading AI tools
จากวิกิพีเดีย สารานุกรมเสรี
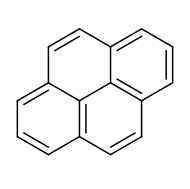
ไพรีน (อังกฤษ: pyrene) เป็นสารประกอบโพลีไซคลิกอะโรมาติกไฮโดรคาร์บอน (PAH) ที่มีวงเบนซีนเชื่อมติดกัน 4 วง เป็นวงแบน ลักษณะเป็นของแข็งไม่มีสี เกิดจากเผาไหม้ไม่สมบูรณ์ของสารประกอบอินทรีย์
 | |
 | |
 | |
| ชื่อ | |
|---|---|
| Preferred IUPAC name
Pyrene[1] | |
| ชื่ออื่น
Benzo[def]phenanthrene | |
| เลขทะเบียน | |
3D model (JSmol) |
|
Beilstein Reference |
1307225 |
| ChEBI | |
| ChEMBL | |
| เคมสไปเดอร์ | |
| ECHA InfoCard | 100.004.481 |
Gmelin Reference |
84203 |
| KEGG | |
ผับเคม CID |
|
| RTECS number |
|
| UNII | |
CompTox Dashboard (EPA) |
|
InChI
| |
SMILES
| |
| คุณสมบัติ | |
| C16H10 | |
| มวลโมเลกุล | 202.256 g·mol−1 |
| ลักษณะทางกายภาพ | ของแข็งไม่มีสี
(yellow impurities are often found at trace levels in many samples). |
| ความหนาแน่น | 1.271 g/cm3[2] |
| จุดหลอมเหลว | 150.62 องศาเซลเซียส (303.12 องศาฟาเรนไฮต์; 423.77 เคลวิน)[2] |
| จุดเดือด | 394 องศาเซลเซียส (741 องศาฟาเรนไฮต์; 667 เคลวิน)[2] |
| 0.049 mg/L (0 °C) 0.139 mg/L (25 °C) 2.31 mg/L (75 °C)[3] | |
| log P | 5.08[4] |
| Band gap | 2.02 eV[5] |
Magnetic susceptibility (χ) |
-147·10−6 cm3/mol[6] |
| โครงสร้าง[7] | |
| โมโนคลินิก | |
Space group |
P21/a |
Lattice constant |
a = 13.64 Å, b = 9.25 Å, c = 8.47 Å α = 90°, β = 100.28°, γ = 90° |
หน่วยสูตร (Z) |
4 |
| อุณหเคมี[8] | |
ความจุความร้อน (C)
|
229.7 J/(K·mol) |
Std molar entropy (S⦵298) |
224.9 J·mol−1·K−1 |
Std enthalpy of formation (ΔfH⦵298) |
125.5 kJ·mol−1 |
ความร้อนแฝงของการหลอมเหลว (ΔfH⦵fus)
|
17.36 kJ·mol−1 |
| ความอันตราย | |
| อาชีวอนามัยและความปลอดภัย (OHS/OSH): | |
อันตรายหลัก |
ระคายเคือง |
| GHS labelling:[9] | |
Pictograms |
  |
Signal word |
เตือน |
Hazard statements |
H315, H319, H335, H410 |
Precautionary statements |
P261, P264, P271, P273, P280, P302+P352, P304+P340, P305+P351+P338, P312, P321, P332+P313, P337+P313, P362, P391, P403+P233, P405, P501 |
| NFPA 704 (fire diamond) | |
| จุดวาบไฟ | ไม่ติดไฟ |
| สารประกอบอื่นที่เกี่ยวข้องกัน | |
PAHsที่เกี่ยวข้อง |
เบนโซไพรีน |
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |
ไพรีนพบครั้งแรกในน้ำมันดินถ่านหินโดยพบได้ถึง 2% มีโครงสร้างแบบเรโซแนนซ์ที่เสถียรกว่าสาร PAHs ตัวอื่นที่เป็นไอโซเมอร์ของฟลูโอแรนทีนเหมือนกัน เกิดขึ้นได้มากจากสภาพการเผาไหม้ ตัวอย่างเช่นเกิดจากการใช้รถยนต์ประมาณ 1 ไมโครกรัม/ กิโลเมตร [10]
การเกิดปฏิกิริยาออกซิเดชันกับโครเมตได้ perinaphthenone และ 1 ,4,5,8 - tetracarboxylic acid โดยผ่านลำดับของปฏิกิริยาไฮโดรจีเนชันและมีความไวต่อปฏิกิริยา halogenation, ปฏิกิริยาการเติมของ Diels-Alder และปฏิกิริยาไนเตรชันที่มีความจำเพาะที่แตกต่างกัน[10]
ไพรีนและอนุพันธ์มีการใช้ในการผลิตสีย้อมเชิงพาณิชย์เช่น pyranine และ naphthalene - 1 ,4,5,8 - tetracarboxylic acid อนุพันธ์ของไพรีนยังเป็นโมเลกุลที่มีคุณค่าสำหรับใช้เป็นโพรบเรืองแสงในกล้อง fluorescence spectroscopy ซึ่งให้ควอนตัมมากและอายุการใช้งานนาน (0.65 และ 410 nanosecond ตามลำดับในเอทานอลที่ 293K) การปล่อยสเปกตรัมมีความไวสูงต่อตัวทำละลายมีขั้วได้ ดังนั้นไพรีนถูกนำมาใช้เป็นโพรบเพื่อตรวจสอบสภาพแวดล้อมที่มีตัวทำละลาย การปล่อยสเปกตรัมจะมีความเข้มต่างไปขึ้นกับการทำปฏิกิริยากับตัวทำละลาย

แม้ว่าจะไม่เป็นปัญหามากเท่าเบนโซไพรีน แต่จากการศึกษาในสัตว์พบว่าไพรีนเป็นพิษต่อตับและไต
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.