热门问题
时间线
聊天
视角
組織蛋白
来自维基百科,自由的百科全书
Remove ads
組織蛋白(英語:histone,或稱組織蛋白)是真核生物體細胞染色質與原核細胞中的鹼性蛋白質,和DNA共同組成核小體結構[1][2][3]。它們是染色質的主要蛋白質體分,作為DNA纏繞的線軸,並在基因調控中發揮作用,但是原核細胞組織蛋白對基因調控的作用非常微弱[3]。沒有組織蛋白,染色體中未纏繞的DNA將非常長(人類DNA中的長寬比超過1000萬比1)。例如,每個人類二倍體細胞(含有23對染色體)具有約1.8米長的DNA,但是在組織蛋白上纏繞它具有大約90微米(0.09毫米)的染色質,當在有絲分裂期間複製和濃縮時,其導致約120微米的染色體[4]。
Remove ads
分類和組織蛋白變體
存在五個主要的組織蛋白家族: H1/H5,H2A,H2B,H3和H4[2][5][6][7]。組織蛋白H2A,H2B,H3和H4被稱為核心組織蛋白(Core Histone),而組織蛋白H1/H5被稱為連接組織蛋白(Linker Histone)。
在H2A、H2B、H3及H4這四種組織蛋白中的其中兩種稱為「核心組織蛋白」,並且集合成為八聚體的核小體核心顆粒。這種集合是將DNA的146對鹼基對以1.65左手超螺旋形圍在這個蛋白質線軸。連接組織蛋白H1將核小體核心顆粒與DNA的進入位點及E位點結合,因而可以將DNA緊扣在位,並且能容許形成更高層次的結構。最基本的形狀為一個10納米的纖維或一連串的珠子。這涉及將在每一個核小體之間約50對的DNA鹼基對圍在這些核小體上,這些DNA又稱為連接DNA。較高層次的結構包括有30及100納米的纖維,是在一般細胞內的結構。在減數分裂中,透過核小體與其他蛋白質的相互作用,合成染色體。合成的組織蛋白與DNA稱為染色質。
核心組織蛋白是高度保守的蛋白質,意即組織蛋白在胺基酸序列中有著非常小的改變。連接組織蛋白通常有著多於一種的形狀,對比核心組織蛋白是保守程度較低的。
在主要的組織蛋白類別中,亦存在一些異構物。它們有著相同的胺基酸序列及相似的核心結構,但卻有著不同的特徵。這些不同的組織蛋白通常帶著染色質的特別功能,就如與H3相似的CenpA是唯一的組織蛋白與染色體的著絲點聯合;H2A的異構物H2A.Z是與活性轉錄基因聯合與涉及在異染色體的形成;另一個H2A異構物H2A.X以雙鏈斷裂與DNA結合,並進行DNA修復。
Remove ads
組織蛋白H1有著一個中央球狀結構域及長的C與N端尾巴,能將小珠子串結構圍成30納米大小的螺線管結構。對比其他種類的組織蛋白,H1的數量只為其他的一半。這是因為它不是構成核小體部份,而只是將DNA及核小體緊扣在一起。H1亦有著它的異構物,稱為組織蛋白H5。
與組織蛋白H2A及H2B類似,組織蛋白H3有著一個主要的球狀結構域與長的N端尾巴,是組成小珠子串結構內的核小體的重要原素。它的N端尾巴從球狀核小體核心伸出,能進行多種影響細胞運作的表觀遺傳修飾。這些修飾包括將甲基及乙醯基共價附著於離胺酸或精胺酸,及絲胺酸或羥丁胺酸的磷酸化。離胺酸9的甲基化涉及基因沉默及在DNA內形成相對較不活躍的異染色質。組織蛋白H3的乙醯基化會在組織蛋白尾巴內不同的離胺酸位置出現,並且由組織蛋白乙醯轉移酶(HAT)所催化。離胺酸14的乙醯基化在基因中很普遍,亦會轉錄成為核糖核酸(RNA)。
以下是人類組織蛋白的列表:
Remove ads
結構
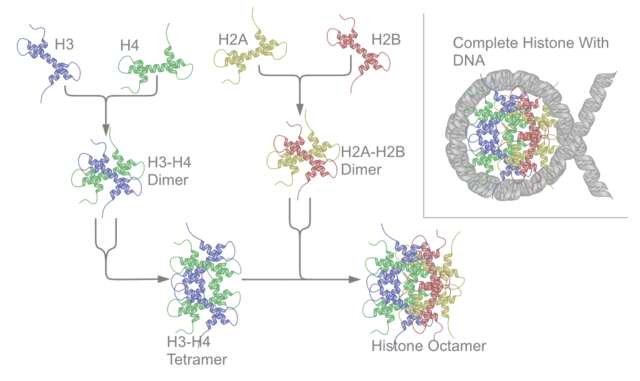
核小體核心顆粒是由兩個H2A-H2B二聚物及兩個H3-H4二聚物結合而成,形成兩半接近對稱的蛋白質三級結構(2階旋轉對稱,即1個高分子是另一個的鏡像)。H2A-H2B及H3-H4二聚物本身亦呈現偽雙向對稱。
這四個核心組織蛋白(H2A、H2B、H3及H4)是在結構上相似及在進化中高度保存的,所有均有著一個「螺旋纏繞螺旋纏繞螺旋」的形狀,可以容許簡單的二聚化。它們在胺基酸結構上都有著一條長的尾巴,讓轉錄後修飾的進行。
總括來說,組織蛋白與DNA有著五種的相互作用:
- H2B、H3及H4的α螺旋兩極積聚正電,能與DNA的帶有負電荷的磷酸鹽分子團產生相互作用。
- 在DNA骨幹與胺基之間的氫鍵對組織蛋白的主鏈。
- 組織蛋白與DNA的去氧核糖的非極性相互作用。
- 鹼性胺基酸(如離胺酸及精胺酸)旁鏈與DNA磷酸氧旁鏈之間的鹽連及氫鍵。
- H3及H2B的N端尾巴的非特定副槽面插入至DNA分子的兩個副槽面。
組織蛋白最重要的基本性質,除了是協助與DNA的相互作用外,就是它的水溶性。
組織蛋白的轉譯後修飾會先在它的N端尾巴開始,再而在其球狀結構域進行。這種修飾包括有甲基化、瓜胺酸化、乙醯化、磷酸化、小泛素相關修飾化、泛素化及二磷酸腺苷核醣基化。這些影響著組織蛋白在基因調控的功能。
一般來說,活性的基因較少與組織蛋白聯繫,但非活性的基因會在間期中與組織蛋白聯合。組織蛋白的結構在進化上保存,這是因為任何有害的突變會造成嚴重的不適應性。
Remove ads
歷史
於1884年,艾布瑞契·科塞爾首先發現組織蛋白。直至1990年代早期,組織蛋白才被更多認識,並非純粹細胞核的惰性填充料,這部分基於馬克·普塔什尼(Mark Ptashne)等人的模型,他們認為轉錄是被蛋白質-DNA和蛋白質-蛋白質相互作用在很大程度上被活化裸DNA模板,就像細菌一樣。及後它的調控功能才被發現。
在1980年代,Yahli Lorch和羅傑·科恩伯格(Roger Kornberg)[8]表明,核心啟動子上的核小體體外阻止了轉錄的啟動,麥可·格倫斯坦(Michael Grunstein)[9]證明組織蛋白在體內抑制轉錄,導致核小體為 一般基因阻遏物。
功能
組織蛋白作為DNA纏繞的線軸。這使得能夠在細胞核內將真核細胞的大型的基因組所必需的壓實物:壓實的分子比未壓實的分子短40,000倍。
組織蛋白進行轉譯後修飾,以更改它與DNA及其他核蛋白的相互作用。組織蛋白H3及H4有著核小體伸出的長尾巴,能夠在不同的地方進行共價修飾。這種修飾包括有甲基化、瓜氨化、乙醯基化、磷酸化、小泛素相關修飾化、泛素化及二磷酸腺苷核醣基化。組織蛋白核心(即H2A及H3)亦可以作出修飾。修飾的組合可以組成編碼,成為組織蛋白編碼。組織蛋白修飾在不同的生物過程起著作用,包括基因表觀調控、DNA修復、有絲分裂及減數分裂 [10]。
組織蛋白修飾的命名是:
舉例來說,H3K4Me就代表組織蛋白H3從N端開始起計第4個離胺酸的甲基化。
參考文獻
參見
外部連結
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads


