From Wikipedia, the free encyclopedia
Amiloidi (lat. amilum od grč. ἄμυλον amilon = škrob) su agregati protein okarakteriziran vlaknastom morfologijom od 7–13 nm u prečniku, β- lista sekundarne strukture (poznata kao kros-β) i sposobnošću prijema obojenja određenim bojama, kao što je kongo crvena.[1] U ljudskom tijelu, amiloidi su povezani s razvojem različitih bolesti.
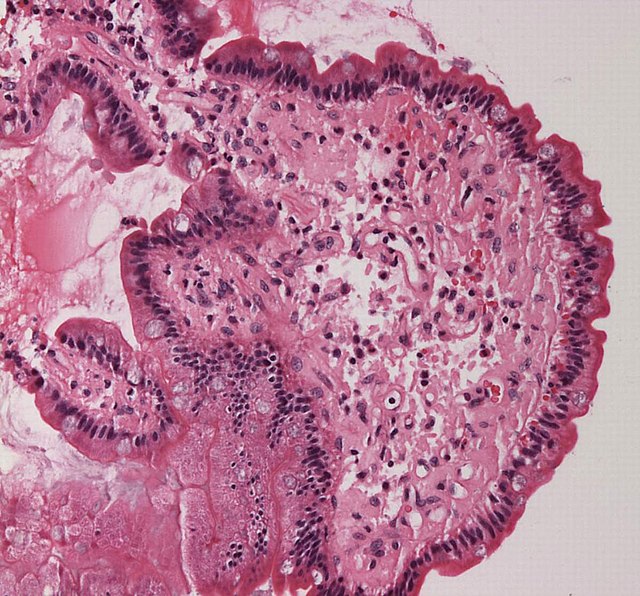
Patogeni amiloidi nastaju kada prethodno zdravi proteini izgube svoju normalnu strukturu i fiziološku funkciju (pogrešno savijanje proteina) i formiraju vlaknaste naslage u plakovima oko ćelija koje mogu poremetiti zdravu funkciju tkiva i organa. Takvi amiloidi su povezani (ali ne nužno kao uzrok) više od 50[2][3] ljudskih bolesti, poznatih kao amiloidoze, i mogu imati ulogu u nekim neurodegenerativnim poremećajima.[2][4] Neke od ovih bolesti su uglavnom sporadične, a samo je nekoliko porodičnih slučajeva. Drugi su samo neporodični. Neki su jatrogeni jer proizlaze iz liječenja. Prioni su infektivni oblici amiloida koji mogu djelovati kao šablon za pretvaranje drugih neinfektivnih oblika.[5] Amiloidi mogu imati i normalne biološke funkcije; naprimjer, u formiranju fimbrije u nekim rodovima bakterija, prijenos epigenetičkih osobina u gljivama, kao i taloženje pigmenta i oslobađanje hormona kod ljudi.
Poznato je da amiloidi nastaju iz mnogih različitih proteina.[2][6] Ovi polipeptidni lanci općenito formiraju strukture β-lista koje se agregiraju u duga vlakna; međutim, identični polipeptidi se mogu sklopiti u više različitih amiloidnih konformacija. Raznolikost konformacija je možda dovela do različitih oblika prionskih bolesti.[7]
Naziv amiloid dolazi od rane pogrešne identifikacije supstance koju je postavio Rudolf Virchow kao škrob, baziran na tehnikama bojenja sirovim jodom. Naučna zajednica je neko vrijeme raspravljala o tome da li su amiloidne naslage masne ili ugljikohidratne naslage dok se konačno nije otkrilo (1859.) da su to, u stvari, naslage albumoidnog proteinskog materijala.[8]
Do danas je pronađeno 37 ljudskih proteina koji da formiraju patološke promjene amiloida koji su povezani s dobro definiranim bolestima.[2] Međunarodno društvo za amiloidozu klasificira amiloidna vlakna i s njima povezane bolesti zasnovane na pridruženim proteinima (na primjer ATTR je grupa bolesti i pridruženih fibrila koje tvori transtiretin).[3](tabela ispod)
| Protein | Bolest | Zvanična skraćenica |
|---|---|---|
| β Amiloid-peptid (Aβ) od prekursora amiloidnog proteina[13][14][15][16] | Alzheimerove bolesti, Nasljedno cerebralno krvarenje s amiloidozom | Aβ |
| α-Sinuklein[14] | Parkinsonova bolest, Demencija Parkinsonove bolesti, Demencija sa Lewyjevim tijelima, Multipla sistemska atrofija | AαSyn |
| PrPSc[17] | Transmisivna spongiformna encefalopatija (npr. Fatalna porodična nesanica, Gerstmann-Sträussler-Scheinkerova bolest, Creutzfeldt-Jacobova bolest, APrPn | |
| Mikrotubulama pridruženi protein tau | Različiti oblici tauopatija (npr. Pickova bolest, Progresivna suprajedarna paraliza, Kortikobazalna degeneracija, Frontotemporalna demencija sa parkinsonizmom povezanim sa hromosomom 17 Argirofilna zrnasta bolest) | ATau |
| Huntingtinski egzon 1[18][19] | Huntingtonova bolest | Nema |
| peptid ABri | Porodična britanska demencija | ABri |
| Peptid ADan | Porodična danska demencija | ADan |
| Fragmenti imunoglobulinskog lahkog lanca[20] | Amiloidoza lahkog lanca | AL |
| Fragmenti Amiloidoza teškog lanca[20] | Amiloidoza teškog lanca | AH |
| Punodužinski N-terminalni fragmenat proteina amiloida A u serumu | Amiloidoza AA | AA |
| Transtiretin | Senilna sistemska amiloidoza, Porodična amiloidna polineuropatija, Porodična amiloidna kardiomiopatija, Leptomeningealna amiloidoza | ATTR |
| Beta-2 mikroglobulin | Amiloidoza povezana s dijalizom, Porodična nasljedna visceralna amiloidoza | Aβ2M |
| N-terminalni fragmenti apoliproteina A | Amiloidoza ApoAI | AApoAI |
| C-terminalno produženi apolipoprotein AII | Amiloidoza ApoAII | AApoAII |
| N-terminalni fragmenti apolipoproteina AIV | Amiloidoza ApoAIV | AApoAIV |
| Apolipoprotein C-II | Amiloidoza ApoCII | AApoCII |
| Apolipoprotein C-III | Amiloidoza ApoCIII | AApoCIII |
| Fragmenti gelsolina | Porodična amiloidoza Finskog tipa | AGel |
| Lizozim | Nasljedna neneuropatska sistemska amiloidoza | ALys |
| Fragmenti fibrinogenog alfa lanca | Fibrinogena amiloidozas | AFib |
| N-terminalno skraćeni cistatin C | Nasljedno cerebralno krvarenje s amiloidozom islandskog tipa | ACys |
| IAPP (Amilin)[21][22] | Šećerna bolest tip 2, Insulinom | AIAPP |
| Kalcitonin[20] | Sržni karcinom štitnjače | ACal |
| Pretkomorni natriuretički faktor | Srčane aritmije, Izolirana pretkomorska amiloidoza | AANF |
| Prolaktin | Hipofizni prolaktinom | APro |
| Insulin | Injekcijski-lokalizirana amiloidoza | AIns |
| Laktadherin / Medin | Aortna medijalna amiloidoza | AMed |
| Laktotransferin / Laktoferin | Želatinozna kapljičasta rožnjačna distrofija | ALac |
| Odontogeni ameloblastno pridružrni protein | Kalcificirajući epitelni odontogeni tumori | AOAAP |
| Plućni surfaktantno pridruženi protein C (SP-C) | Plućna alveolska proteinoza | ASPC |
| Leukocitni ćelijsko-izvedeni hemotaksin-2 (LECT-2) | Amiloidoza Bubrežna amiloidoza LECT2 | ALECT2 |
| Galektin-7 | Lišajska amiloidoza, Makulska amiloidoza | AGal7 |
| Korneodezmozin | Tjemenski hypotrichosis simplex | ACor |
| C-terminalni fragmenti TGFBI/keratoepitelina | Distrofija rožnjačne rešetke tip I, distrofija rožnjačne rešetke tip 3A, distrofija rožnjačne rešetke Avellino tip | AKer |
| Semenogelin-1 (SGI) | Amiloidoza sjemenskih vezikula | ASem1 |
| Proteinj S100A8/A9 | Rak prostate | Nema |
| Enfuvirtid | Injekcijski-lokalizirana amiloidoza | AEnf |

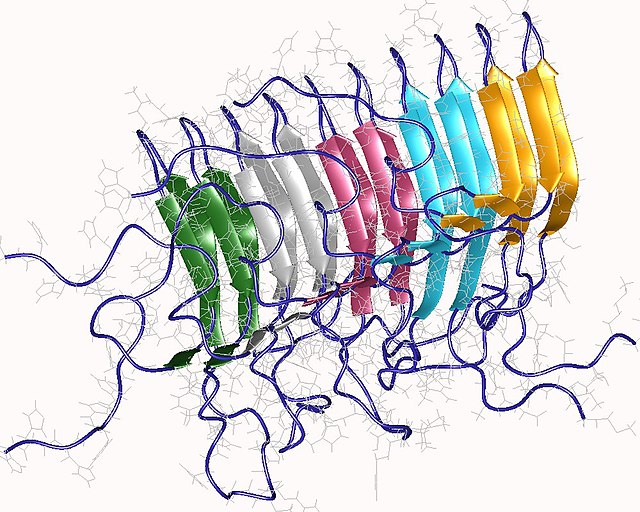
Amiloidi su formirani od dugih nerazgranatih vlakana koja se odlikuju proširenom sekundarnom strukturom beta-lista u kojoj su raspoređeni pojedinačni beta-lanci (β-nizovi) (obojene strelice na susjednoj slici) u orijentaciji okomitoj na dugu os vlakna. Takva struktura je poznata kao kros-β struktura. Svako pojedinačno vlakno može biti široko 7-13 nanometara i dugo nekoliko mikrometara.[2][7] Glavna obilježja prepoznata iz ugla različitih disciplina za klasifikaciju proteinskih agregata kao amiloida je prisustvo vlaknaste morfologije očekivanog prečnika, detektiranog pomoću transmisijske elektronske mikroskopije (TEM) ili mikroskopije atomske sile (AFM), prisutnost unakrsne β-sekundarne strukture, određene pomoću kružnog dihronizma, FTIR, nuklearne magnetne rezonance u čvrstom stanju (ssNMR), rendgenske kristalografije ili difrakcijom rendgenskih vlakana (često se smatra testom "zlatnog standarda" da bi se utvrdilo sadrži li struktura unakrsna β-vlakna) i sposobnost bojenja specifičnim bojama, kao što je [ [Kongo crvena]], tioflavin T ili tioflavin S.[2]
Termin "kros-β" (unakrska β) zasnovan je na posmatranju dva skupa difrakcijskih linija, jedne uzdužne i jedne poprečne, koje formiraju karakterističan "križni" obrazac.[24] Postoje dva karakteristična difrakcijska signala rasijanja, proizvedena na 4,7 i 10 Å (0,47 nm i 1,0 nm), koji odgovaraju međulančanim razmacima i udaljenostima slaganja u beta-listovima. "Stopovi" beta-lista su kratki i prelaze širinu amiloidnog fibrila; dužina amiloidnog fibrila je izgrađena od poređanih β-lanaca. Unakrsni β-obrazac smatra se dijagnostičkim obilježjem strukture amiloida.[1][7]
Amiloidna vlakna se uglavnom sastoje od 1-8 protofilamenata (jedan protofilament koji također odgovara vlknu prikazan je na slici), svaki promjera 2-7 nm, koji međusobno djeluju bočno, kao ravne trake koje održavaju visinu od 2-7 nm (jednog protofilamenta) i široki su do 30 nm; češće se protofilamenti uvijaju jedan oko drugog i formiraju tipski 7-13 nm široke fibrile.[2] Svaki protofilament ima tipsku unakrsnu β-strukturu i može biti formiran od 1-6 β-listova (šest je prikazano na slici) naslagane jedna na drugu. Svaka pojedinačna proteinska molekula može doprinijeti jednom do nekoliko β-lanaca u svakom protofilamentu i lanci mogu biti raspoređeni u antiparalelne β-listove, ali češće u paralelne β-listove. Samo dio polipeptidnog lanca nalazi se u β-lančanoj konformaciji u vlaknima, ostatak tvori strukturirane ili nestrukturirane petlje ili repove.
Dugo je znanje o strukturi amiloidnih vlakana na atomskom nivou bilo ograničeno činjenicom da su neprikladna za najtradicionalnije metode za proučavanje proteinskih struktura. Posljednjih godina zabilježen je napredak u eksperimentalnim metodima, uključujući spektroskopiju NMR u čvrstom stanju i krioelektronsku mikroskopiju. U kombinaciji, ovi metodi dali su 3D atomske strukture amiloidnih fibrila formiranih od amiloidnih β peptida, α-sinukleina, tau i FUS-proteina, povezanih s različitim neurodegenerativnim bolestima..[25][26]


Amiloid se formira polimerizacijom stotina do hiljada monomernih peptida ili dugovlaknastih proteina. Formiranje amiloida uključuje fazu zaostajanja (zvanu nukleacijska faza), eksponencijalnu fazu (zvanu 'faza rasta) i fazu platoa (zvana faza zasićenja), kao što je prikazano na slici.[27][28][29][30] Zaista, kada je količina fibrila prikazana u zavisnosti od vremena, vidi se sigmoidni vremenski tok koji odražava tri različite faze.
U najjednostavnijem modelu „jezgarne polimerizacije “ (označeno crvenim strelicama na donjoj slici), pojedinačni rasklopljeni ili djelomično rasklopljeni polipeptidni lanci (monomeri) pretvaraju se u jezgro (monomer no ili oligomerno) preko termodinamički nepovoljnog procesa koji se javlja u ranoj fazi kašnjenja.[29] Fibrili rastu naknadno iz ovih jezgara dodavanjem monomera u eksponencijalnoj fazi.[29]
Drugačiji model, zvani jezgarna konformacijska konverzija označen je plavim strelicama na donjoj slici, uveden je kasnije, kako bi se uklopio u neka eksperimentalna zapažanja: često je otkriveno da se monomere brzo pretvaraju u pogrešno savijene i visoko neorganizirane oligomere različite od jezgara.[31] Tek kasnije, ovi agregati će se strukturno reorganizirati u jezgra, na kojima će se drugi neorganizirani oligomeri dodavati i reorganizirati putem šablonskog ili induciranog mehanizma (ovaj model nukleirane konformacijske konverzije), formirajući fibrile na kraju.[31]
Normalno savijeni proteini moraju se djelomično odmotati prije nego što se agregacija može dogoditi kroz jedan od ovih mehanizama.[32] U nekim slučajevima, međutim, presavijeni proteini se mogu agregirati bez prelaska glavne energetske barijere za odvijanje, naseljavanjem konformacija sličnih nativnim kao posljedica termalnih fluktuacija, oslobađanja liganda ili lokalnog odvijanja koje se događa u određenim okolnostima.[32] U ovim nativnim konformacijama, segmenti koji su normalno ukopani ili strukturirani u potpuno presavijeni i koji imaju veliku sklonost agregatima postaju izloženi rastvaraču ili fleksibilni, omogućavajući formiranje nativnih agregata , koji se kasnije pretvaraju u jezgra i fibrile. Ovaj proces se naziva nativnolika agregacija (zelene strelice na slici) i sličan je modelu nukleirane konformacijske konverzije.
Noviji, moderan i temeljiti model formiranja amiloidnih fibrila uključuje intervenciju sekundarnih događaja, kao što je fragmentacija, u kojoj se vlakna lome na dva ili više kraćih fibrila, i sekundarna nukleacij, u kojoj se površine fibrila kataliziraju stvaranjem novih jezgara.[30] Oba sekundarna događaja povećavaju broj krajeva fibrila koje mogu regrutirati nove monomere ili oligomere, pa se ubrzava stvaranje vlakana, putem mehanizma pozitivne povratne sprege. Ovi događaji doprinose dobro poznatim koracima primarne nukleacije (formiranje jezgra od monomera putem jednog od gore opisanih modela), elongacije fibrila (dodavanje monomera ili oligomera na rastuće krajeve fibrila) i disocijacije (suprotan proces).
Takav novi model opisan je na slici desno i uključuje korištenje master jednadžbe koja uključuje sve korake formiranja amiloidnih fibrila, tj. primarnu nukleaciju, elongaciju fibrila, sekundarnu nukleaciju i fragmentaciju fibrila.[30][33] Konstate stopae različitih koraka mogu se odrediti globalnim prilagođavanjem broja agregacija (naprimjer emisije fluorescencije tioflavina (ThT) umjesto vremena) snimljenih pri različitim koncentracijama proteina.[30] Pristup opće glavne jednadžbe formiranju amiloidnih fibrila sa sekundarnim putevima razvili su Knowles, Vendruscolo, Cohen, Michaels sa suradnicima i odredili vrijeme evolucije koncentracije dužine vlakana (ovdje predstavlja broj monomera u agregatu).[33] gdje označava Kroneckerov delta. Fizička interpretacija različitih pojmova u gornjoj glavnoj jednadžbi je direktna: pojmovi u prvom redu opisuju rast fibrila dodavanjem monomera sa konstantom brzine (elongacija). Termini u drugom redu opisuju disocijaciju monomera, tj. inverzni proces elongacije. je konstantna brzina disocijacije monomera. Termini u trećem redu opisuju efekt fragmentacije, za koju se pretpostavlja da se javlja homogeno duž fibrila sa konstantnom brzinom . . Konačno, termini u posljednjem redu opisuju primarnu i sekundarnu nukleaciju. Brzina sekundarne nukleacije proporcionalna je masi agregata, definiranoj kao .
Prateći ovaj analitički pristup, postalo je očigledno da faza kašnjenja ne odgovara nužno samo formiranju jezgra, već je rezultat kombinacije različitih koraka. Slično, eksponencijalna faza nije samo elongacija fibrila, već je rezultat kombinacije različitih koraka, uključujući primarnu nukleaciju, elongaciju fibrila, ali i sekundarne događaje. Značajna količina vlakana koja nastaje kao rezultat primarne nukleacije i izduženja fibrila može se formirati tokom lag-faze, a sekundarni koraci, a ne samo elongacija fibrila, mogu biti dominantni procesi koji doprinose rastu fibrila tokom eksponencijalne faze. Sa ovim novim modelom, svi uznemirujući agensi formiranja amiloidnih fibrila, kao što su navodni lijekovi, metaboliti, mutacije, molekulski pratitelji, itd., mogu se pripisati određenom koraku formiranja fibrila.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.