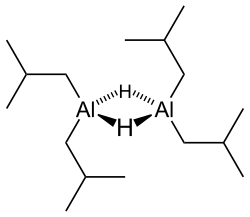
Diisobutylaluminiumhydrid
chemická sloučenina From Wikipedia, the free encyclopedia
Remove ads
Diisobutylaluminiumhydrid (zkráceně DIBALH, DIBAL, DIBAL-H nebo DIBAH) je organická sloučenina se vzorcem (i-Bu2AlH)2, lde i-Bu je isobutyl (-CH2CH(CH3)2). Používá se například jako kokatalyzátor polymerizace alkenů.[1]
Remove ads
Vlastnosti
Podobně jako u většiny organických sloučenin hliníku je struktura této pravděpodobně složitější než napovídá stechiometrický vzorec. Několika metodami bylo zjištěno, že sloučenina vytváří dimer a trimer, obsahující tetraedrická hliníková centra a hydridové můstkové ligandy.[2]
Hydridové ionty jsou malé a navázané na sloučeniny hliníku také silně zásadité, což za přítomnosti alkylových skupin způsobuje tvorbu můstků.
Remove ads
Příprava
DIBAL lze připravit zahříváním triisobutylhliníku (který se také vyskytuje jako dimer), čímž se vyvolá beta-hydridová eliminace:[3]
- (i-Bu3Al)2 → (i-Bu2AlH)2 + 2 (CH3)2C=CH2
I když může DIBAL být prodáván jako bezbarvá kapalina, tak se častěji dodává jako roztok v organickém rozpouštědlu, například toluenu nebo hexanu.
Použití
DIBAL se používá v mnoha redukcích, například při přeměnách karboxylových kyselin, nitrilů a dalších jejich derivátů na aldehydy. DIBAL účinně redukuje α-β nenasycené estery na allylalkoholy.[4] Hydrid lithnohlinitý (LiAlH4) oproti tomu redukuje estery a acylchloridy na primární alkoholy a nitrily na primární aminy. DIBAL reaguje rychleji se sloučeninami bohatými na elektrony, je tak elektrofilním redukčním činidlem, zatímco LiAlH4 je spíše nukleofilem.
Přestože DIBAL dobře redukuje nitrily na aldehydy, tak redukce esterů se stejnými funkčními skupinami sice vypadají, že by také měly probíhat dobře, ovšem často vedou ke směsím alkoholů a aldehydů; tomu se lze vyhnout opatrným řízením podmínek reakce.[5]
Bezpečnost
DIBAL, jako i většina organohlinitých sloučenin, nebezpečně reaguje se vzduchem a vodou, kdy může i dojít k výbuchu.
Odkazy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads