Top-Fragen
Zeitleiste
Chat
Kontext
Bariumcarbonat
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Remove ads
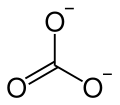
Bariumcarbonat ist das Carbonat des Erdalkalimetalls Barium. Es besitzt die Formel BaCO3 und kommt in der Natur als Mineral Witherit vor.
Es wird als Bestandteil von Rattengift sowie als Komponente von Zement und Backsteinen verwendet.
Remove ads
Eigenschaften

Das farblose Salz Bariumcarbonat zersetzt sich bei atmosphärischem Druck bei Temperaturen ab 1300 °C zu Bariumoxid und Kohlenstoffdioxid:[2]
Es kristallisiert orthorhombisch, Raumgruppe Pmcn (Raumgruppen-Nr. 62, Stellung 5) mit den Gitterparametern a = 5,313 Å, b = 8,896 Å und c =6,428 Å.[5] Es sind auch Hochtemperaturformen mit den Raumgruppen R3m (Nr. 166) und Fm3m (Nr. 225) bekannt.[6]
Remove ads
Herstellung
Zusammenfassung
Kontext
Bariumcarbonat wird industriell durch die Reaktion von Bariumsulfid mit Kohlenstoffdioxid oder auch Natriumcarbonat bei 40–90 °C hergestellt:[7]
Es kann auch durch Einleiten von Kohlenstoffdioxid in eine Aufschlämmung aus Bariumhydroxid in Wasser dargestellt werden:[8]
Remove ads
Verwendung
Bariumcarbonat wird beispielsweise als Rohstoff für die Herstellung von Wirtschaftsglas und optischem Glas benutzt. Zudem ist es das Endprodukt beim Nachweis von Kohlenstoffdioxid mit Barytwasser. Dieser Nachweis ist nur möglich, weil Bariumcarbonat in Wasser schwer löslich ist. In geringen Mengen wird es in der Fahrzeugindustrie für Speicherkatalysatoren eingesetzt.
Sicherheitshinweise
Bariumcarbonat ist gesundheitsschädlich.[9] Es wirkt reizend auf Schleimhäute, führt zu Funktionsstörungen im zentralen und peripheren Nervensystem, Muskellähmung, gastrointestinalen Beschwerden sowie Herz-Kreislauf- und Lungenfunktionsstörungen.
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads