Najlepsze pytania
Chronologia
Czat
Perspektywa
Eten
związek chemiczny Z Wikipedii, wolnej encyklopedii
Remove ads
Eten, etylen, C2H4 – organiczny związek chemiczny, najprostszy możliwy alken (węglowodór nienasycony).

Remove ads
Właściwości
Eten jest gazem bezbarwnym, o słodkawym zapachu. Jest substancją łatwopalną. Rozpuszcza się bardzo dobrze w rozpuszczalnikach niepolarnych np. arenach i alkanach.
Budowa
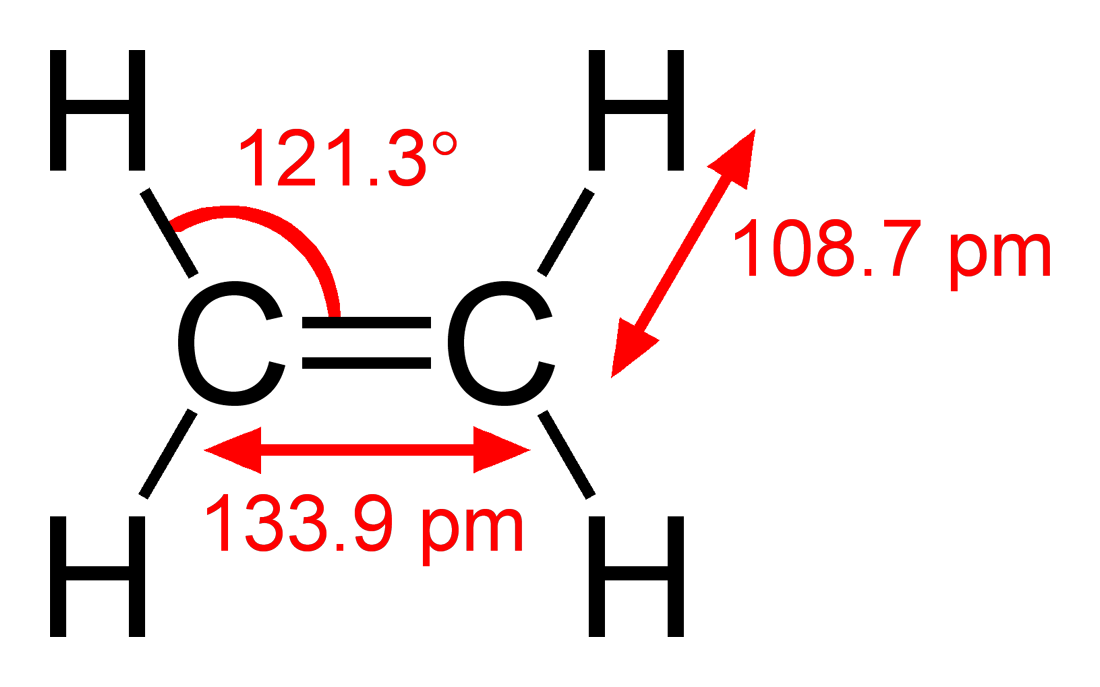
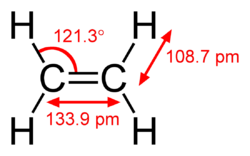
Jest to cząsteczka płaska i symetryczna, a kąty pomiędzy wiązaniami (H−C−H) wynoszą 120°. Długości wiązan wynoszą odpowiednio:
- pomiędzy atomem węgla a atomami wodoru 110 pm;
- pomiędzy atomami węgla 134 pm;
W wyniku hybrydyzacji orbitali (sp2) w obu atomach węgla, pomiędzy nimi występuje jedno wiązanie π i jedno wiązanie σ. Ulega reakcjom addycji, utlenienia i polimeryzacji.
W mieszaninie z powietrzem jest wybuchowy w granicach stężeń 2,75–28,6%, oraz podczas ogrzewania pod zwiększonym ciśnieniem.
Remove ads
Występowanie, otrzymywanie i zastosowanie
W stanie naturalnym występuje w niewielkich (zmiennych) ilościach w gazie ziemnym. Otrzymywany jest na skalę techniczną podczas termicznego rozkładu węglowodorów gazowych i ciekłych (piroliza etenowo-propenowa), z gazowych produktów procesów rafinacji ropy naftowej (kraking termiczny i katalityczny, hydrokraking, reforming) i z gazów koksowniczych.
Niewielkie ilości etenu do celów laboratoryjnych można otrzymać w wyniku odwodnienia etanolu przez wkraplanie go do gorącego kwasu siarkowego lub podczas ogrzewania etanolu z tlenkiem glinu:
- C
2H
5OH → C
2H
4↑ + H
2O
Można też otrzymać poprzez ogrzewanie folii polietylenowej (reakcja depolimeryzacji):
- −[−CH
2−CH
2−]
n → n C
2H
4↑
Eten jest jednym z podstawowych surowców przemysłu petrochemicznego. Stosowany jest do produkcji polietylenu i wielu kopolimerów, etylobenzenu (do produkcji styrenu), tlenku etylenu, chloropochodnych (chlorek winylu, dichloroetan), etanolu i wyższych alkoholi alifatycznych.
Etylen w biochemii
Podsumowanie
Perspektywa
Etylen jest hormonem roślinnym, stymulującym opadanie liści, dojrzewanie owoców, starzenie się roślin. Wydzielany jest przez praktycznie wszystkie części rośliny[4].
Biosynteza

Biosynteza etylenu przebiega w kilku etapach. Substratem jest metionina, która jest przekształcana w S-adenozylometioninę (SAM) przez enzym o nazwie syntaza SAM. Następnie SAM jest przekształcana w kwas 1-aminocyklopropano-1-karboksylowy (ACC) przez syntazę ACC (ACS), natomiast metionina jest regenerowana w cyklu Yanga (patrz schemat obok). Ostatnim etapem jest konwersja ACC do etylenu przez oksydazę ACC (ACO), gdzie ACC jest utleniany przy udziale oksydazy ACC do etylenu oraz dwutlenku węgla i cyjanowodoru[5].
Zastosowanie
W przechowalniach owoców skuteczne usuwanie etylenu wydzielanego przez owoce zapobiega ich przedwczesnemu dojrzewaniu. Natomiast przed sprzedażą owoce poddaje się działaniu etylenu w celu szybkiego doprowadzenia ich do stanu dojrzałości. Takiemu zabiegowi standardowo poddaje się banany, które zbierane są zielone, w stadium dojrzałości zbiorczej i po dotarciu na miejsce przeznaczenia dla uzyskania jednolitych jakościowo owoców poddane są zabiegowi gazowania etylenem przez okres 4-7 dni[6]. Przedwczesnemu dojrzewaniu zapobiega się, blokując działanie etylenu za pomocą 1-Metylocyklopropenu.
Potrójna odpowiedź u roślin
Etylen jest odpowiedzialny za tzw. potrójną odpowiedź u roślin. Gdy nasiono kiełkuje i napotyka przeszkodę, musi wykonać manewr, aby ją ominąć. Etylen stymuluje grubienie łodygi, zmniejszenie elongacji i wykrzywienie się rośliny, tak by ta mogła przedostać się na powierzchnię.
Mutacje
Występuje kilka rodzajów mutacji roślin związanych z etylenem:
- ein – roślina nie ma receptorów etylenu
- eto – roślina produkuje za dużo etylenu, ale reaguje na podawane przez człowieka inhibitory
- ctr – nie reagują na inhibitory (ponieważ nie występuje u nich kinaza, będąca normalnie negatywnym regulatorem ekspresji) i dlatego przeprowadzają potrójną odpowiedź, nawet w powietrzu.
Remove ads
Przypisy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads