Najlepsze pytania
Chronologia
Czat
Perspektywa
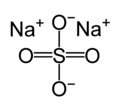
Siarczan sodu
związek chemiczny Z Wikipedii, wolnej encyklopedii
Remove ads
Siarczan sodu, Na2SO4 – nieorganiczny związek chemiczny, sól kwasu siarkowego i sodu. Występuje w postaci bezwodnej i uwodnionej – heptahydratu i dekahydratu. Forma bezwodna występuje w naturze jako rzadki minerał tenardyt, a dziesięciowodna – mirabilit (natomiast minerał glauberyt jest mieszanym siarczanem sodowo-wapniowym).
Remove ads
Historia
Siarczan sodu w formie dekahydratu, Na2SO4·10H2O, został wyizolowany w roku 1625 przez Johanna Glaubera z wody ze źródła leczniczego w pobliżu Neapolu. Ponieważ wypicie tej wody doprowadziło go do wyleczenia z ciężkiej choroby układu pokarmowego, nazwał uzyskane kryształy Sal Mirabilis („sól cudowna”). W późniejszym okresie Glauber opracował metodę otrzymywania kwasu solnego z chlorku sodu z kwasem siarkowym i jako produkt uboczny wyizolował substancję, którą zidentyfikował jako swoją Sal Mirabilis. W wyniku długoletnich badań tego związku określił 26 jego zastosowań medycznych, 12 alchemicznych i 21 w sztuce; m.in. opracował mieszaninę oziębiającą umożliwiającą wymrożenie wody z wina. W efekcie siarczan sodu został nazwany „solą glauberską”; nazwa ta bywa używana również współcześnie[5].
Remove ads
Otrzymywanie
Poza wydobyciem siarczanu sodu z jego naturalnych złóż i następnym oczyszczaniem go, może być on także otrzymywany w dwóch procesach otrzymywania chlorowodoru[2]:
- procesie Mannheima opartym na reakcji chlorku sodu z kwasem siarkowym:
- 2NaCl + H2SO4 → Na2SO4 + 2HCl↑
- procesie Hargreavesa, w którym zamiast kwasu siarkowego używa się dwutlenku siarki:
- 4NaCl + 2SO2 + O2 + 2H2O → 2Na2SO4 + 4HCl↑
Otrzymany roztwór jest następnie poddawany krystalizacji frakcyjnej[2].
Siarczan sodu jest także produktem ubocznym otrzymywania fenolu poprzez stapianie soli kwasów benzenosulfonowych z wodorotlenkiem sodu[2].
Remove ads
Właściwości

Bezwodny siarczan sodu jest białym krystalicznym proszkiem o strukturze rombowej lub heksagonalnej i twardości w skali Mohsa równej 2,8. Ma właściwości higroskopijne. Współczynnik załamania wynosi 1,468[2].
Dziesięciowodny siarczan sodu tworzy natomiast bezbarwne jednoskośne kryształy o twardości w skali Mohsa wynoszącej 1,8. Współczynnik załamania wynosi 1,394[2].
Siarczan sodu bardzo dobrze rozpuszcza się w wodzie, natomiast jest nierozpuszczalny w etanolu[1][2].
Rozpuszczanie siarczanu sodu Na2SO4 w wodzie pochłania ciepło otoczenia +78,6 kJ/mol i układ oziębia się[6].
Zastosowanie

Siarczan sodu jest wykorzystywany w procesie Krafta do otrzymywania ścieru drzewnego. Stosowany również przy produkcji szkła, barwników (m.in. ultramaryny) i detergentów. Bezwodny siarczan sodu stosuje się jako środek pochłaniający wodę. Służy również do otrzymywania innych soli[2].
W medycynie stosowany jest jako osmotycznie aktywny środek przeczyszczający. Jest on słabo absorbowany w przewodzie pokarmowym tworząc roztwór hipertoniczny, co uniemożliwia odwadnianie masy kałowej w jelitach[7].
Remove ads
Przypisy
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads