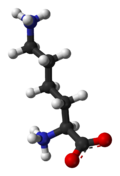
Lisina
From Wikipedia, the free encyclopedia
Remove ads
A lisina[1] (abreviada Lys ou K) é un aminoácido compoñente das proteínas sintetizadas polos seres vivos. É un dos dez aminoácidos esenciais para os seres humanos. A súa fórmula molecular é C6H14N2O2 e o seu nome IUPAC é ácido 2,6-diaminohexanoico. Está codificada polos codóns AAA e AAG. O seu punto isoeléctrico é 9,74.


Remove ads
Estrutura química
Actúa quimicamente como unha base, igual que a arxinina e a histidina, xa que a súa cadea lateral contén un grupo amino protonable que a miúdo participa na formación de pontes de hidróxeno e como base xeral nas catálises.
Este grupo amino, ademais de darlle carga positiva ás proteínas, é acetilable por encimas específicos, coñecidos como acetiltransferases. Considérase que esta acetilación é unha modificación postraducional, xa que se produce despois da tradución da proteína a partir do ARN mensaxeiro. Porén, as súas modificacións postraducionais máis comúns inclúen a metilación do grupo ε-amino, que dá como resultado a metil-, dimetil- e a trimetillisina. Isto último ocorre na proteína calmodulina.
O coláxeno contén hidroxilisina, que se deriva da lisina a través da lisil hidroxilase. A O-glicosilación dos residuos de lisina no retículo endoplasmático ou no aparato de Golgi utilízase para marcar certas proteínas para a secreción fóra da célula.
Remove ads
Biosíntese
Como aminoácido esencial, a lisina non se sintetiza no organismo dos animais e, por conseguinte, estes deben inxerilo como lisina ou como proteínas que conteñan lisina. Existen dúas rutas coñecidas para a biosíntese deste aminoácido. A primeira lévase a cabo en bacterias e plantas superiores, a través do ácido diaminopimélico, e a segunda na maior parte dos fungos superiores, por medio do ácido α-aminoadípico. Nas plantas e nos microorganismos a lisina sintetízase a partir de ácido aspártico, que se converte en primeiro lugar en β-aspartil-semialdehido. A ciclación xera dihidropicolinato, que se reduce a Δ1-piperidina-2,6-dicarboxilato. A apertura do anel deste heterociclo xera unha serie de derivados do ácido pimélico, que finalmente xeran lisina.
Algúns dos encimas que participan nesta biosíntese son os seguintes:[2]
- Aspartoquinase
- β-aspartato semialdehido deshidroxenase
- dihidropicolinato sintase
- Δ1-piperidina-2,6-dicarboxilato deshidroxenase
- N-succinil-2-amino-6-cetopimelato sintase
- Succinil diaminopimelato aminotransferase
- Succinil diaminopimelato desuccinilase
- Diaminopimelato epimerase
- Diaminopimelato descarboxilase

Remove ads
Metabolismo
A lisina metabolízase nos mamíferos para dar acetil-CoA, a través dunha transaminación inicial con α-cetoglutarato. A degradación bacteriana da lisina dá como resultado cadaverina, a través dun proceso de descarboxilación.
A allisina é un derivado da lisina, utilizado na síntese da elastina e do coláxeno. Prodúcese pola acción do encima lisil oxidase sobre a lisina na matriz extracelular e é esencial na formación dos enlaces cruzados que estabilizan o coláxeno e a elastina.
Síntese
A lisina sintética, racémica, coñécese desde hai moito tempo.[3] Unha síntese práctica iníciase a partir de caprolactama.[4]
Degradación
Na súa degradación oxidativa a lisina orixina acetoacetil-CoA, polo que é un aminoácido cetoxénico.
Fontes dietéticas
Os requirimentos nutricionais de lisina son de 1,5 g diarios. Encóntrase en cantidades mínimas en todos os cereais (gramíneas), pero é moi abundante nos legumes. Son boas fontes de lisina os alimentos ricos en proteínas: carnes (especificamente as carnes vermellas, a de porco e a de ave), queixo (en particular o parmesano), algúns peixes (bacallau e sardiñas) e ovos.
Propiedades
A L-lisina é un compoñente necesario para a síntese de todas as proteínas do organismo. Desempeña un papel central na absorción do calcio; na construción das proteínas musculares; na recuperación das intervencións cirúrxicas ou das mancaduras deportivas, e na produción de hormonas, encimas e anticorpos.
Modificación
A lisina pode modificarse de diferentes maneiras: acetilación, metilación, ubiquitinación, sumoilación (unión de proteínas SUMO), biotinilación, carboxilación etc., o cal tende a modificar a función da proteína da cal a lisina modificada forma parte.[5]
Importancia clínica
Suxeriuse que a lisina pode ser beneficiosa para as persoas que presentan infeccións de herpes simplex.[6] Porén, fan falta máis estudos para confirmar esta afirmación.
Existen conxugados de lisina que parecen ter propiedades prometedoras para o tratamento do cáncer, porque parece que provocan que as células cancerosas se autodestrúan cando o fármaco se utiliza en combinación co uso de fototerapia, sen danar ás células non cancerosas.[7]
A lisina ten unha acción ansiolítica debido aos seus efectos sobre os receptores da serotonina. Un estudo en ratas [8] demostrou que a sobreestimulación dos receptores 5-HT4 no tracto intestinal está asociada con patoloxías intestinais (diarreas) inducidas pola ansiedade. A lisina actúa como un antagonista da serotonina e reduce a sobreestimulación deses receptores, reducindo tamén os signos de ansiedade e os trastornos intestinais que esta induce. Outro estudo indica que a deficiencia de lisina leva a un incremento patolóxico da serotonina na amígdala, estrutura cerebral implicada na regulación emocional e a resposta ao estrés.[9] Estudos en humanos tamén mostraron unha correlación negativa entre a redución dos niveis de inxestión de lisina e a ansiedade.[10]
De acordo con estudos en animais a deficiencia de lisima causa immunodeficiencia.[11].
A lisina, inxerida con L-carnitina, axuda a que a carnitina diminúa notablemente os niveis de colesterol no sangue.
Papel na nutrición animal
A lisina é un aminoácido esencial limitante para moitas especies animais de importancia zootécnica. Cando se equilibran formulacións de alimentos para gando emprégase o concepto de "aminoácido limitante" para incorporar a cantidade correcta na dieta baseándose no contido de lisina dos distintos alimentos proteicos dispoñibles e o posible emprego de lisina sintética. Isto último é común e moi económico de facer na alimentación dos porcos e outras especies de interese zootécnico. O obxectivo é optimizar o crecemento do gando.
No caso da nutrición do gando leiteiro a lisina é tamén limitante xunto coa metionina, pero non se pode empregar lisina sintética directamente debido a que a fermentación microbiana no rume a destrúe en grande medida; porén, existen xa produtos comerciais cunha protección química que impide dita degradación, aínda que a rendibilidade económica deses produtos é discutible.
Remove ads
Notas
Véxase tamén
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads