Предлошка:Chembox Absorbance
| |||
| |||
| Систематско име | Етаннитрил[1] | ||
| Назнаки | |||
|---|---|---|---|
| 75-05-8 | |||
| Бајлштајн | 741857 | ||
| ChEBI | CHEBI:38472 | ||
| ChEMBL | ChEMBL45211 | ||
| ChemSpider | 6102 | ||
| EC-број | 200-835-2 | ||
Гмелин |
895 | ||
| 3Д-модел (Jmol) | Слика | ||
| MeSH | ацетонитрил | ||
| PubChem | 6342 | ||
| RTECS-бр. | AL7700000 | ||
| |||
| UNII | Z072SB282N | ||
| ОН-бр. | 1648 | ||
| Својства | |||
| Хемиска формула | |||
| Моларна маса | 0 g mol−1 | ||
| Изглед | Безбојна течност | ||
| Мирис | Слабо, изразено, овошно | ||
| Густина | 0.786 g/cm3 при 25°C | ||
| Точка на топење | |||
| Точка на вриење | |||
| Мешлив | |||
| log P | −0.334 | ||
| Парен притисок | 9.71 kPa (при 20,0 °C) | ||
Хенриева константа (kH) |
530 μmol/(Pa·kg) | ||
| Киселост (pKa) | 25 | ||
| UV-vis (λmax) | 195 nm | ||
Магнетна чувствителност (χ) |
−28,0⋅10-6 cm3/mol | ||
| Показател на прекршување (nD) | 1.344 | ||
| Термохемија | |||
| Ст. енталпија на образување ΔfH |
40.16–40.96 kJ/mol | ||
| Ст. енталпија на согорување ΔcH |
−1256.03 – −1256.63 kJ/mol | ||
| Стандардна моларна ентропија S |
149.62 J/(K·mol) | ||
| Специфичен топлински капацитет, C | 91.69 J/(K·mol) | ||
| Опасност | |||
| GHS-ознаки: | |||
Пиктограми |
  | ||
Сигнални зборови |
Опасност | ||
Изјави за опасност |
H225, H302, H312, H319, H332 | ||
Изјави за претпазливост |
P210, P280, P305+P351+P338 | ||
| NFPA 704 | |||
| Температура на запалување | 2.0 °C (35.6 °F; 275.1 K) | ||
| 523.0 °C (973.4 °F; 796.1 K) | |||
| Граници на запалливост | 4.4–16.0% | ||
| Смртоносна доза или концентрација: | |||
LD50 (средна доза) |
| ||
LC50 (средна концентрација) |
5655 ppm (морско прасе, 4 ч) 2828 ppm (зајак, 4 ч) 53,000 ppm (стаорец, 30 min) 7500 ppm (стаорец, 8 ч) 2693 ppm (глушец, 1 ч)[3] | ||
LCLo (најниска објавена) |
16,000 ppm (куче, 4 ч)[3] | ||
| NIOSH (здравствени граници во САД): | |||
PEL (дозволива) |
TWA 40 ppm (70 mg/m3)[4] | ||
REL (препорачана) |
TWA 20 ppm (34 mg/m3)[4] | ||
IDLH (непосредна опасност) |
500 ppm[4] | ||
| Дополнителни податоци | |||
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |||
| Наводи | |||
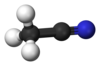
Ацетонитрил, чести скратено како MeCN (метил цијанид), е хемиско соединение со формула CH
3CN и структурна формула H
3C–C≡N. Оваа безбојна течност е наједноставниот органски нитрил (цијановодородот е поедноставен нитрил, но цијанидниот анјон не е класифициран како органски). Се произведува главно како нуспроизвод од производството на акрилонитрил. Се користи како поларен апротичен растворувач во органската синтеза и во прочистувањето на бутадиен.[5] N≡C–C скелетот е линеарен со кратко растојание C≡N од 1,16 Å.[6]
Ацетонитрил првпат бил подготвен во 1847 година од францускиот хемичар Жан-Батист Думас.[7]
Ацетонитрил се користи главно како растворувач за прочистување на бутадиен во рафинериите. Поточно, ацетонитрилот се внесува во горниот дел од колоната за дестилација исполнета со јаглеводороди, вклучително и бутадиен и како што ацетонитрилот паѓа низ колоната, го апсорбира бутадиенот кој потоа се испраќа од дното на кулата до втора разделна кула. Потоа се користи топлина во разделната кула за да се одвои бутадиенот.
Во лабораторија се користи како растворувач со среден поларитет кој се меша со вода и низа органски растворувачи, но не и со заситени јаглеводороди. Бидејќи има удобен опсег на течност и висока диелектрична константа од 38,8. Со диполен момент од 3,92 D,[8] ацетонитрил раствора широк опсег на јонски и неполарни соединенија и е корисен како мобилна фаза во HPLC и LC-MS.
Широко се користи во апликациите на батериите поради неговата релативно висока диелектрична константа и способноста да раствори електролити. Од слични причини тој е популарен растворувач во цикличната волтаметрија.
Неговиот прекин на ултравиолетова транспарентност, нискиот вискозитет и ниската хемиска реактивност го прават популарен избор за течна хроматографија со високи перформанси (HPLC).
Ацетонитрилот игра значајна улога како доминантен растворувач кој се користи во синтезата на олигонуклеотиди од нуклеозидни фосфорамидити.
Индустриски, се користи како растворувач за производство на фармацевтски производи и фотографски филм.[9]
Органски синтези
Ацетонитрилот е вообичаен двојаглероден градежен блок во органската синтеза[10] од многу корисни хемикалии, вклучувајќи ацетамидин хидрохлорид, тиамин и α-нафтален оцетна киселина.[11] Неговата реакција со цијаноген хлорид дава малонитрил.[5]
Како донатор на електронски пар
Ацетонитрилот има слободен електронски пар во азотниот атом, кој може да формира многу нитрилни комплекси со преоден метал. Бидејќи е слабо базен, тој е лесно заменлив лиганд. На пример, бис(ацетонитрил)паладиум дихлорид се подготвува со загревање на суспензија од паладиум хлорид во ацетонитрил:[12]
Сроден комплекс е тетракис (ацетонитрил) бакар(I) хексафлуорофосфат [Cu(CH
3CN)
4]+
. CH
3CN групите во овие комплекси се брзо поместени од многу други лиганди.
Исто така, формира луисови адукти со луисови киселини од групата 13 како бор трифлуорид.[13] Во суперкиселините, можно е да се протонира ацетонитрил.[14]
Ацетонитрил е нуспроизвод од производството на акрилонитрил. Повеќето се согоруваат за да се поддржи планираниот процес, но се проценува дека неколку илјади тони се задржани за горенаведените апликации.[15] Така, трендовите на производство на ацетонитрил генерално ги следат оние на акрилонитрилот. Ацетонитрил, исто така, може да се произведува со многу други методи, но тие не се од комерцијална важност од 2002 година. Илустративни начини се со дехидрација на ацетамид или со хидрогенирање на мешавини од јаглерод моноксид и амонијак.[16] Во 1992 година, во САД беа произведени 14.700 тони (32.400.000 lb) ацетонитрил.
Истражувана е и каталитичката амоксидација на етилен.[17]
Недостаток на ацетонитрил во 2008-2009 година
Почнувајќи од октомври 2008 година, светската понуда на ацетонитрил беше мала бидејќи кинеското производство беше затворено за Олимпијадата. Понатаму, една американска фабрика беше оштетена во Тексас за време на ураганот Ајк.[18] Поради глобалното економско забавување, производството на акрилонитрил што се користи во акрилни влакна и во смоли на акрилонитрил бутадиен стирен (ABS) се намали. Ацетонитрилот е нуспроизвод во производството на акрилонитрил и неговото производство исто така се намали, што дополнително го зголемува недостигот на ацетонитрил.[19] Глобалниот недостиг на ацетонитрил продолжи до почетокот на 2009 година.[потребно е ажурирање]
Токсичност
Ацетонитрил има само скромна токсичност во мали дози.[11][20] Може да се метаболизира за да произведе цијановодород, кој е извор на забележаните токсични ефекти.[9][21][22] Генерално, почетокот на токсичните ефекти е одложен, поради времето потребно за телото да го метаболизира ацетонитрилот во цијанид (обично околу 2-12 часа).[11]
Случаите на труење со ацетонитрил кај луѓето (или, поконкретно, на труење со цијанид по изложување на ацетонитрил) се ретки, но не се непознати, со вдишување, голтање и (можеби) со апсорпција на кожата.[21] Симптомите, кои обично не се појавуваат неколку часа по изложувањето, вклучуваат тешкотии со дишењето, бавен пулс, гадење и повраќање. Конвулзии и кома може да се појават во сериозни случаи, проследени со смрт од респираторна инсуфициенција. Третманот е како за труење со цијанид, со кислород, натриум нитрит и натриум тиосулфат меѓу најчесто користените итни третмани.[21]
Се користи во формулации за отстранувач на лак за нокти и покрај неговата токсичност. Најмалку два случаи се пријавени на случајно труење на мали деца со отстранувач на лак на база на ацетонитрил, од кои еден бил фатален.[23] Ацетонот и етил ацетатот често се претпочитаат како побезбедни за домашна употреба, а ацетонитрилот е забранет во козметичките производи во Европската економска област од март 2000 година.[24]
Метаболизам и екскреција
| Соединение | Цијанид, концентрација во мозокот (μg/kg) | Орално LD50 (mg/kg) |
|---|---|---|
| Калиум цијанид | 748 ± 200 | 10 |
| Пропионитрил | 508 ± 84 | 40 |
| Бутиронитрил | 437 ± 106 | 50 |
| Малононитрил | 649 ± 209 | 60 |
| Акрилонитрил | 395 ± 106 | 90 |
| Ацетонитрил | 28 ± 5 | 2460 |
| Готварска сол (NaCl) | Н/П | 3000 |
| Концентрациите на јонски цијанид измерени во мозокот на стаорци Спраг-Доли еден час по орална администрација на of an LD50 на различни нитрили.[25] | ||
Заеднички со другите нитрили, ацетонитрилот може да се метаболизира во микрозомите, особено во црниот дроб, за да произведе цијановодород, како што беше првпат прикажано од Поцани и сор. во 1959 година.[26] Првиот чекор во оваа патека е оксидација на ацетонитрил во гликолонитрил со помош на NADPH-зависна цитохром P450 монооксигеназа. Гликолонитрилот потоа се подложува на спонтано распаѓање за да добие цијановодород и формалдехид.[20][21] Формалдехид, токсин и канцероген сам по себе, дополнително се оксидира до мравја киселина, која е уште еден извор на токсичност.
Метаболизмот на ацетонитрилот е многу побавен од оној на другите нитрили, што е причина за неговата релативно ниска токсичност. Оттука, еден час по администрацијата на потенцијално смртоносна доза, концентрацијата на цијанид во мозокот на стаорецот беше 1⁄20 од онаа за доза на пропионитрил 60 пати помала (види табела).[25]
Релативно бавниот метаболизам на ацетонитрил во цијановодород овозможува поголем дел од произведениот цијанид да се детоксицира во телото до тиоцијанат (патот на родан). Исто така, овозможува поголем дел од ацетонитрилот да се излачува непроменет пред да се метаболизира. Главните патишта на екскреција се со издишување и со урина.[20][21][22]
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.