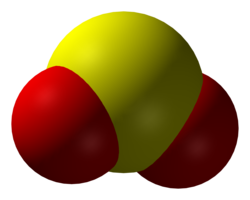
സൾഫർ ഡയോക്സൈഡ്
രാസ സംയുക്തം From Wikipedia, the free encyclopedia
Remove ads
ഒരു സൾഫർ അണുവും രണ്ടു് ഓക്സിജൻ അണുക്കളും അടങ്ങുന്ന തന്മാത്രയുള്ള ഒരു വാതകമാണു് സൾഫർ ഡയോക്സൈഡ്. ഇതിന്റെ രാസവാക്യം SO2 എന്നാണു്. രൂക്ഷമായ തുളച്ചുകയറുന്ന മണമുള്ള ഒരു വാതകമാണിത്. അഗ്നിപർവതങ്ങളിൽ നിന്നും പലതരം വ്യവസായങ്ങളിൽ നിന്നും ഈ വാതകം പുറത്തുവിടാറുണ്ട്. കൽക്കരി പെട്രോളിയം എന്നിവയിൽ സൾഫർ സംയുക്തങ്ങൾ ഉള്ളതുകാരണം ഇവ ജ്വലിക്കുമ്പോൾ സൾഫർ ഡയോക്സൈഡ് ഉണ്ടാകും. SO2, സാധാരണഗതിയിൽ NO2 പോലെയുള്ള രാസത്വരകത്തിന്റെ സാന്നിദ്ധ്യത്തിൽ ഓക്സിഡേഷനു വിധേയമാകുമ്പോൾ H2SO4 ഉണ്ടാകും. ഇത് ആസിഡ് മഴയ്ക്ക് കാരണമാകും.[9] അന്തരീക്ഷത്തിൽ തങ്ങിനിൽക്കുന്ന ധൂളികളും ഇത്തരത്തിൽ ഉണ്ടാകും. ഈ രണ്ടു വിധത്തിലാണ് സൾഫർ ഡയോക്സൈഡ് പ്രധാനമായും പരിസ്ഥിതിയെ ബാധിക്കുന്നത്.
Remove ads
ഘടനയും ബോണ്ടുകളും
SO2 ഒരു ഒടിവുള്ള തന്മാത്രയാണ്.

ഉത്പാദനം
ജ്വലനത്തിലൂടെ
സൾഫറോ സൾഫർ അടങ്ങിയിട്ടുള്ള വസ്തുക്കളോ കത്തിക്കുമ്പോൾ സൾഫർ ഡയോക്സൈഡ് ഉണ്ടാകും:
- S8 + 8 O2 → 8 SO2
കമ്പിളി, മുടി, റബ്ബർ എന്നിവയൊക്കെ കത്തിക്കുമ്പോൾ സൾഫർ ഉണ്ടാകും. ഇരുമ്പുമായി ചേർന്ന് (വീടിനു തീ പിടിക്കുമ്പോഴും മറ്റും) ഇത് ഫെറസ് സൾഫൈഡ് ഉണ്ടാക്കും. ഇതിനെ വീണ്ടും ഓക്സിജന്റെ സാന്നിദ്ധ്യത്തിൽ ചൂടാക്കിയാൽ സൾഫർ ഡയോക്സൈഡ് വീണ്ടും സ്വതന്ത്രമാകും:
4 FeS2 + 11 O2 → 2 Fe2O3 + 8 SO2
ഹൈഡ്രജൻ സൾഫൈഡ് ജ്വലിച്ചാലും രാസപ്രവർത്തനം ഇതുപോലെ തന്നെയാണ് നടക്കുന്നത്.
- 2 H2S + 3 O2 → 2 H2O + 2 SO2
പൈറൈറ്റ്, സ്ഫാലെറൈറ്റ്, സിന്നബാർ തുടങ്ങിയ അയിരുകൾ വ്യാവസായികമായി റോസ്റ്റ് ചെയ്യുമ്പോഴും സൾഫർ ഡയോക്സൈഡ് ഉത്പാദിപ്പിക്കപ്പെടും:[10]
- 4 FeS2 + 11 O2 → 2 Fe2O3 + 8 SO2
- 2 ZnS + 3 O2 → 2 ZnO + 2 SO2
- HgS + O2 → Hg + SO2
- 4 FeS + 7O2 → 2 Fe2O3 + 4 SO2
ഈ രീതികളെല്ലാം ചേർന്നാണ് അഗ്നിപർവതങ്ങളിൽ നിന്ന് ദശലക്ഷക്കണക്കിന് ടൺ സൾഫർ ഡയോക്സൈഡ് പുറത്തുവരുന്നത്.
Remove ads
പ്രതിപ്രവർത്തനങ്ങൾ
വ്യാവസായികം
ക്ഷാരഗുണമുള്ള ലായനികൾ സൾഫൈറ്റ് ലവണങ്ങളുമായി പ്രതിപ്രവർത്തിക്കുമ്പോൾ:
- SO2 + 2 NaOH → Na2SO3 + H2O
ക്ലൗസ് പ്രക്രീയയിൽ സൾഫർ ഡയോക്സൈഡ് ഒക്സിഡൈസിംഗ് രാസവസ്തുവായാണ് പ്രവർത്തിക്കുന്നത്. റിഫൈനറികളിൽ ഈ രാസപ്രവർത്തനം വൻ തോതിൽ ഉപയോഗിക്കാറുണ്ട്:
- SO2 + 2 H2S → 3 S + 2 H2O
സൾഫ്യൂറിക് ആസിഡിന്റെ നിർമ്മാണം.
- 2 SO2 + 2 H2O + O2 → 2 H2SO4
ഉപയോഗങ്ങൾ
സൾഫ്യൂറിക് ആസിഡിന്റെ നിർമ്മാണത്തിലെ ഉപയോഗം
ഭക്ഷ്യവസ്തുക്കൾ സൂക്ഷിച്ചുവയ്ക്കാൻ
ഉണക്കിയ ആപ്രിക്കോട്ട്, ഫിഗ് തുടങ്ങിയ പഴങ്ങൾ സൂക്ഷിച്ചുവയ്ക്കാൻ സൾഫർ ഡയോക്സൈഡിന്റെ രോഗാണുക്കളെ നശിപ്പിക്കാനുള്ള ശേഷി ഉപയോഗപ്പെടുത്താറുണ്ട്. ചീയൽ തടയുകയും നിറം സംരക്ഷിക്കുകയും ചെയ്യും എന്ന ഗുണവുമുണ്ട്. മൊളാസസ്സിലും ചിലപ്പോൾ ഇത് ചേർക്കാറുണ്ട്.
വൈൻ നിർമ്മാണം
വൈനുത്പാദനത്തിൽ സൾഫർ ഡയോക്സൈഡ് ഉപയോഗിക്കാറുണ്ട്.[11] എല്ലാത്തരം വൈനുകളിലും സൾഫർ ഉണ്ടാകും.[12] രോഗാണു നാശിനിയായും ഓക്സിഡേഷൻ തടയുന്ന രാസവസ്തുവായുമാണ് ഇത് പ്രവർത്തിക്കുന്നത്.
SO2 വൈൻ നിർമ്മാണശാലകൾ വൃത്തിയാക്കാനും ഉപയോഗിക്കപ്പെടുന്നുണ്ട്.
റെഡ്യൂസിംഗ് രാസവസ്തുവായുള്ള ഉപയോഗം
പേപ്പറിനെ ബ്ലീച്ച് ചെയ്യാൻ ഇതുപയോഗിക്കാറുണ്ട്. ക്ലോറിനേറ്റ് ചെയ്ത ജലത്തെ ഉപയോഗശേഷം ഒഴുക്കിക്കളയുന്നതിനു മുൻപ് സൾഫർ ഡയോക്സൈഡ് ഉപയോഗിച്ച് റെഡ്യൂസ് ചെയ്യാറുണ്ട്. ഇത് ക്ലോറിനെ സ്വതന്ത്രമാക്കും. [13]
ഇത് ജലത്തിൽ ലയിക്കും.
ബയോകെമിസ്ട്രിയിലും വൈദ്യത്തിലുമുള്ള ഉപയോഗം
വലിയ അളവിൽ സൾഫർ ഡയോക്സൈഡ് മാരകമാണ്. ബാക്ടീരിയകളും മറ്റും ഇത് ഉത്പാദിപ്പിക്കാറുണ്ട്. സസ്തനികളുടെ ശരീരപ്രവർത്തനത്തിൽ സൾഫർ ഡയോക്സൈഡിന്റെ പ്രഭാവം ഇതുവരെ പൂർണമായി മനസ്സിലാക്കാൻ സാധിച്ചിട്ടില്ല. [14] ഹെറിംഗ്-ബ്രൂവർ റിഫ്ലക്സ്, പൾമണറി സ്ട്രെച്ച് റിഫ്ലക്സ് എന്നിവയെ സൾഫർ ഡയോക്സൈഡ് തടയും.
തണുപ്പിക്കാനുള്ള ഉപയോഗം
ഫ്രിയോണുകൾ കണ്ടുപിടിക്കുന്നതിനു മുൻപ് സൾഫർ ഡയോക്സൈഡ് റഫ്രിജിറേറ്ററുകളിൽ ഉപയോഗിച്ചിരുന്നു.
ലബോറട്ടറിയിൽ ലായകമായും മറ്റുമുള്ള ഉപയോഗം
ഓക്സിഡൈസിംഗ് ലവണങ്ങളെ ലയിപ്പിക്കാനുള്ള ലായകമായി സൾഫർ ഡയോക്സൈഡ് ഉപയോഗിക്കാറുണ്ട്. സൾഫൊണൈൽ ഗ്രൂപ്പിന്റെ ഉത്പാദനത്തിനും ഇതുപയോഗിക്കും:[15]
Remove ads
അന്തരീക്ഷത്തിലെ മാലിന്യം

അഗ്നിപർവ്വതസ്ഫോടനങ്ങളിൽ നിന്ന് പുറത്തുവരുന്നതിനാലും മറ്റും അന്തരീക്ഷത്തിൽ സൾഫർ ഡയോക്സൈഡിന്റെ സാന്നിദ്ധ്യമുണ്ട്. [16] അമേരിക്കൻ ഐക്യനാടുകളിലെ പരിസ്ഥിതി സംരക്ഷണ ഏജൻസിയുടെ കണക്കനുസരിച്ച് [17]), താഴെപ്പറയുന്ന അളവ് സൾഫർ ഡയോക്സൈഡ് അമേരിക്കൻ ഐക്യനാടുകളിൽ പ്രതിവർഷം ബഹിർഗമിക്കുന്നുണ്ട്:
മലിനീകാരി എന്ന നിലയിൽ മനുഷ്യാരോഗ്യത്തിൽ സൾഫർ ഡയോക്സൈഡ് വലിയ സ്വാധീനം ചെലുത്തുന്നുണ്ട്. [18] മൃഗങ്ങളെയും സസ്യങ്ങളെയും ഇത് ബാധിക്കും. [19]
കൽക്കരിയിൽ നിന്ന് സൾഫർ ഡയോക്സൈഡ് ഫ്ലൂയിഡൈസ്ഡ് ബെഡ് കംബഷൻ എന്ന പ്രക്രീയ ഉപയോഗിച്ച് നീക്കം ചെയ്യാൻ സാധിക്കും. [20] കത്തിക്കുന്നതിനു മുൻപ് ഇന്ധനങ്ങളിൽ നിന്ന് സൾഫർ നീക്കം ചെയതാൽ SO2 ഉണ്ടാകുന്നത് തടയാൻ സാധിക്കും. [21][22]
കാൽസ്യം, മഗ്നീഷ്യം ഓക്സൈഡ് എന്നിവ പെട്രോൾ, ഡീസൽ എഞ്ചിനുകളിൽ നിന്ന് സൾഫർ ഡയോക്സൈഡ് ഗാസ് ബഹിർഗമിക്കുന്നതു തടയാൻ കൂട്ടിച്ചേർക്കലിന് ഉപയോഗിക്കാറുണ്ട്. [23]
2006-ൽ ലോകത്തിൽ ഏറ്റവും കൂടുതൽ സൾഫർ ഡയോക്സൈഡ് പുറന്തള്ളുന്ന രാജ്യം ചൈനയായിരുന്നു[24]
Remove ads
സുരക്ഷ
ശ്വസനം
ഈ വാതകം ശ്വസിച്ചാൽ ശ്വാസകോശസംബന്ധമായ അസുഖലക്ഷണങ്ങൾ കാണപ്പെടും (ശ്വാസമെടുക്കാനുള്ള ബുദ്ധിമുട്ട് തുടങ്ങി മരണം വരെ സംഭവിക്കാം). [25] ശരാശരി 5 ppm (13 mg/m3) സുരക്ഷിതമായ അളവ്. [26]
സൾഫർ ഡയോക്സൈഡ് ശ്വസനവും വളർച്ചയെത്താതെ കുട്ടികൾ ജനിക്കുന്നതും തമ്മിൽ ബന്ധമുണ്ട്. [27]
ഉള്ളിലെത്തൽ
അമേരിക്കൻ ഐക്യനാടുകളിൽ ഭക്ഷ്യസാധനങ്ങൾ സൂക്ഷിക്കാൻ സൾഫർ ഡയോക്സൈഡും സോഡിയം ബൈസൾഫൈറ്റും ഉപയോഗിക്കാനുള്ള അനുമതിയുണ്ട്. [28]
Remove ads
ഇവയും കാണുക
- സൾഫർ ട്രൈ ഓക്സൈഡ്
- സൾഫർ-അയഡിൻ സൈക്കിൾ
അവലംബം
പുറത്തേയ്ക്കുള്ള കണ്ണികൾ
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads