From Wikipedia, the free encyclopedia
Un receptor de Fc ou receptor Fc (abreviado FcR) é unha proteína que se encontra na superficie de certas células incluíndo entre outros os linfocitos B, células dendríticas foliculares, células asasinas naturais, macrófagos, neutrófilos, eosinófilos, basófilos, plaquetas humanas, e mastocitos, que contribúen ás funcións protectoras do sistema inmunitario. O seu nome deriva da súa especificidade de unión por unha parte dos anticorpos chamada rexión do fragmento cristalizable (Fc), situado no pé da molécula con forma de Y do anticorpo. Os receptores de Fc únense aos anticorpos que están adheridos a células infectadas ou a patóxenos invasores. A súa actividade estimula as células fagocíticas ou citotóxicas para que destrúan os microbios ou células infectadas por medio de fagocitose mediada por anticorpos ou citotoxicidade mediada por células dependente de anticorpo. Algúns virus como os flavivirus utilizan os receptores de Fc para axudarse na infección das células, por un mecanismo infectivo chamado potenciación dependente de anticorpo.[1]

Hai varios tipos de receptores Fc (ou FcR), que se clasifican baseándose no tipo de anticorpo que recoñecen. A letra latina utilizada para identificar un tipo de anticorpo é convertida na correspondente letra grega, situada despois de 'Fc'. Por exemplo, aqueles que se unen á clase máis común de anticorpo, a IgG, denomínanse receptores de Fc-gamma (FcγR), os que se unen á IgA chámanse recepotores Fc-alfa (FcαR) etc. As clases de FcR tamén se distinguen polas células que os expresan (macrófagos, granulocitos, células asasinas naturais, células T e B) e as propiedades de sinalización de cada receptor.[2]
Todos os receptores de Fcγ (FcγR) pertencen á superfamilia das inmunoglobulinas e son os receptores de Fc máis importantes para inducir a fagocitose de microbios opsonizados (marcados ou cubertos de anticorpos).[3] Esta familia inclúe varios membros, como FcγRI (CD64), FcγRIIA (CD32), FcγRIIB (CD32), FcγRIIIA (CD16a), FcγRIIIB (CD16b), que difiren nas súas afinidades polo anticorpo debido ás súas distintas estruturas moleculares.[4] Por exemplo, o FcγRI únese a unha IgG máis fortemente que o FcγRII ou o FcγRIII. O FcγRI tamén ten unha porción extracelular composta por tres dominios similares a inmunoglobulinas, o que supón un dominio máis do que teñen o FcγRII ou o FcγRIII. Esta propiedade permite que o FcγRI se una a unha soa molécula de IgG (ou monómero), pero todos os receptores Fcγ deben unirse a múltiples moléculas de IgG dentro dun inmunocomplexo para seren activadas.[5]
Os receptores Fc-gamma difiren na súa afinidade polas IgG e igualmente as diferentes subclases de IgG teñen afinidades únicas para cada un dos receptores Fc-gamma.[6] Estas interaccións son máis afinadas polo glicano (oligosacárido) en posición CH2-84.4 da IgG.[6] Por exemplo, ao crear impedimentos estéricos, os glicanos CH2-84.4 que conteñen fucosa reducen a afinidade da IgG polo FcγRIIIA.[6] En contraste, os glicanos G0, que carecen de galactosa e no seu lugar terminan en residuos de GlcNAc, teñen unha afinidade incrementada polo FcγRIIIA.[6]
Outro FcR, chamado FcRn, exprésase en múltiples tipos de células e é similar en estrutura ao MHC de clase I. Este receptor tamén se une a IgG e está implicado na preservación deste anticorpo.[7] Porén, como este receptor Fc está tamén implicado en transferir as Ig da nai por vía placentaria ao feto, ou a través do leite a un meniño lactante, denomínase receptor Fc neonatal (FcRn).[8][9] Recentemente, certas investigacións suxeriron que este receptor xoga un papel na homeostase dos niveis de Ig séricos.
Só hai un receptor de Fc que pertenza ao subgrupo FcαR, que se denomina FcαRI (ou CD89).[10] FcαRI encóntrase na superficie de neutrófilos, eosinófilos, monocitos, algúns macrófagos (incluíndo as células de Kupffer), e algunhas células dendríticas.[10] Está composto por dous dominios similares a Ig extracelulares, e é membro tanto da superfamilia das inmunoglobulinas coma da familia do receptor de recoñecemento inmune multicadea (MIRR).[3] Envía sinais ao asociarse con dúas cadeas de sinalización FcRγ.[10] Outro receptor pode tamén unirse a IgA, aínda que ten maior afinidade polo anticorpo IgM.[11] Este receptor denomínase receptor Fc-alfa/mu (Fcα/μR) e é unha proteína transmembrana de tipo I. Cun dominio similar a Ig na súa porción extracelular, este receptor Fc é tamén un membro da superfamilia das inmunoglobulinas.[12]
Coñécense dous tipos de FcεR:[3]
| Nome do receptor | Principal ligando anticorpo | Afinidade polo ligando | Disribución celular | Efecto despois de unirse ao anticorpo |
| FcγRI (CD64) | IgG1 e IgG3 | Alta (Kd ~ 10−9 M) | Macrófagos Neutrófilos Eosinófilos Células dendríticas |
Fagocitose Activación celular Activación da explosión respiratoria Indución da matanza de microbios |
| FcγRIIA (CD32) | IgG | Baixa (Kd > 10−7 M) | Macrófagos Neutrófilos Eosinófilos Plaquetas Células de Langerhans |
Fagocitose Desgranulación (eosinófilos) |
| FcγRIIB1 (CD32) | IgG | Baixa (Kd > 10−7 M) | Células B Mastocitos |
Non hai fagocitose Inhibición da actividade celular |
| FcγRIIB2 (CD32) | IgG | Baixa (Kd > 10−7 M) | Macrófagos Neutrófilos Eosinófilos |
Fagocitose Inhibición da actividade celular |
| FcγRIIIA (CD16a) | IgG | Baixa (Kd > 10−6 M) | Células NK Macrófagos (en certos tecidos) |
Indución da citotoxicidade mediada por células dependente de anticorpos (ADCC) Indución da liberación de citocinas polos macrófagos |
| FcγRIIIB (CD16b) | IgG | Baixa (Kd > 10−6 M) | Eosinófilos Macrófagos Neutrófilos Mastocitos Células dendríticas foliculares |
Indución da matanza de microbios |
| FcεRI | IgE | Alta (Kd ~ 10−10 M) | Mastocitos Eosinófilos Basófilos Células de Langerhans Monocitos |
Desgranulación Fagocitose |
| FcεRII (CD23) | IgE | Baixa (Kd > 10−7 M) | Células B Eosinófilos Células de Langerhans |
Posible molécula de adhesión Transporte de IgE a través do epitelio intestinal humano Mecanismo de retroalimentación positiva para potenciar a sensibilización alérxica (células B) |
| FcαRI (CD89) | IgA | Baixa (Kd > 10−6 M) | Monocitos Macrófagos Neutrófilos Eosinófilos |
Fagocitose Indución da matanza de microbios |
| Fcα/μR | IgA e IgM | Alta para IgM, media para IgA | Células B Células mesanxiais Macrófagos |
Endocitose Indución da matanza de microbios |
| FcRn | IgG | Monocitos Macrófagos Células dendríticas Células epiteliais Células endoteliaiss Hepatocitos |
Transfire IgG desde a nai ao feto a través da placenta Transfire IgG da nai ao meniño lactante a través do leite Protexe a IgG da degradación |

Os receptores de Fc encóntranse en varias células do sistema inmunitario incluíndo fagocitos como os macrófagos e monocitos, granulocitos como os neutrófilos e eosinófilos, e linfocitos do sistema inmunitario innato (células asasinas naturais) ou do sistema inmunitario adaptativo (por exemplo, células B).[17][18][19] Permiten que estas células se unan a anticorpos que están adheridos á superficie de células infectadas por microbios, axudando a estas células inmunes a identificar e eliminar os patóxenos microbianos. Os receptores de Fc únense aos anticorpos pola súa rexión Fc (ou cola), e esta interacción activa a célula que posúe o receptor de Fc.[20] A activación dos fagocitos é a función máis común atribuída aos receptores de Fc. Por exemplo, os macrófagos empezan a inxerir e matar un patóxeno cuberto de IgG por fagocitose despois da unión dos seus receptores Fcγ.[21] Outro proceso que implica os receptores Fc denomínase citotoxicidade mediada por células dependente de anticorpos (ADCC). Durante a ADCC, os receptores FcγRIII na superficie das células NK estimula as células NK para liberar moléculas citotóxicas dos seus gránulos para matar células cubertas de anticorpos.[22] O FcεRI ten unha función diferente. O FcεRI é o receptor de Fc dos granulocitos, e está implicado nas reaccións alérxicas e na defensa contra infeccións parasíticas. Cando está presente un antíxeno alérxico apropiado ou parasito, os enlaces cruzados de polo menos dúas moléculas de IgE e os seus receptores de Fc da superficie dun granulocito desencadean que a célula libere rapidamente os mediadores preformados almacenados nos seus gránulos.[3]
Os receptores Fc-gamma xeran sinais dentro das células por medio dun importante motivo de activación chamado motivo de activación baseado na tirosina inmunorreceptor (ITAM, do inglés Immunoreceptor Tyrosine-based Activation Motif ).[23] Un ITAM é unha secuencia específica de aminoácidos (YXXL) que aparece dúas veces en estreita sucesión na cola intracelular dun receptor. Cando se engaden grupos fosfato a un residuo de tirosina (Y) do ITAM por encimas chamados tirosina quinases, xérase unha fervenza de sinalización dentro da célula. Esta reacción de fosforilación normalmente ocorre a continuación de que un receptor de Fc se una ao seu ligando. Un ITAM está presente na cola intracelular do FcγRIIA e a súa fosforilación induce a fagocitose nos macrófagos. O FcγRI e o FcγRIIIA non teñen un ITAM pero poden transmitir un sinal activador aos seus fagocitos interaccionando con outra proteína que si o ten. Esta proteína adaptadora chámase subunidade Fcγ e, como o FcγRIIA, contén as dúas secuencias YXXL que son características dun ITAM.
A presenza dun só un motivo YXXL non é dabondo para activar as células, e representa un motivo (I/VXXYXXL) chamado motivo inhibidor baseado na tirosina inmunorreceptor (ITIM, do inglés Immunoreceptor Tyrosine-based Inhibitory Motif). O FcγRIIB1 e o FcγRIIB2 teñen unha secuencia ITIM e son receptores de Fc inhibidores; non inducen a fagocitose. As accións inhibidoras destes receptores están controladas por encimas que eliminan os grupos fosfato dos residuos de tirosina; as fosfatases SHP-1 e SHIP-1 inhiben a sinalización por receptores Fcγ.[24] A unión do ligando ao FcγRIIB leva á fosforilación da tirosina do motivo ITAM. Esta modificación xera o sitio de unión para a fosfatase, un dominio de recoñecemento SH2. A abolición da sinalización de activación de ITAM está causada pola inhibición da proteína tirosina quinases da familia Src, e pola hidrolización da PIP3 da membrana, interrompendo a posterior sinalización augas abaixo polos receptores activadores, como os FcγRs activadores, TCR, BCR e receptores de citocinas (por exemplo, c-Kit).[25]
A sinalización negativa por FcγRIIB é importante principalmente para a regulación de células B activadas. A sinalización de células B positiva é iniciada pola unión de antíxenos alleos ás inmunogloblinas de superficie. O mesmo anticorpo específico de antíxeno é segregado e pode suprimir por retroalimentación, ou promover unha sinalización negativa. Esta sinalización negativa proporciónaa o FcγRIIB.:[26] Os experimentos usando mutantes de deleción de células B e encimas negativos dominantes estableceron firmemente o importante papel exercido pola inositol 5-fosfatase que contén o dominio SH2 (chamada SHIP) na sinalización negativa. A sinalización negativa a través de SHIP parece inhibir a vía Ras por competición do dominio SH2 con Grb2 e Shc e pode implicar o consumo de mediadores lipídicos intracelulares que actúan como activadores de encimas alostéricos ou que promoven a entrada de Ca2+ extracelular.[27]
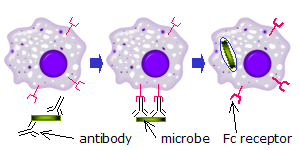
Cando as IgG, específicas para un determinado antíxeno ou compoñente da superficie, se unen ao patóxeno pola súa rexión Fab (fragmento de unión ao antíxeno), as súas rexións Fc quedan orientadas cara a fóra, ao alcance directo dos fagocitos. Os fagocitos únense ás rexións Fc polos seus receptores de Fc.[21] Establécense moitas interaccións de baixa afinidade entre o receptor e o anticorpo que en conxunto menteñen unido firmemente o microbio cuberto de anticorpos. Esta afinidade individual baixa impide que os receptores de Fc se unan a anticorpos en ausencia do antíxeno, e, por tanto, reduce a oportunidade de activación das células inmunes en ausencia de infección. Isto tamén impide a aglutinación de fagocitos polo anticorpo cando non hai antíxeno. Unha vez que se uniu o patóxeno, as interaccións entre a rexión Fc do anticorpo e os receptores de Fc do fagocito teñen como resultado o inicio da fagocitose. O patóxeno é fagocitado polo fagocito por medio dun proceso activo que implica a unión e liberación do complexo rexión Fc/receptor de Fc, ata que a membrana plasmática do fagocito rodea completamente o patóxeno.[28]

O receptor de Fc das células NK recoñece as IgG que están unidas á superficie dunha célula diana infectada por un patóxeno e denomínase CD16 ou FcγRIII.[29] A activación de FcγRIII pola IgG causa a liberación de citocinas como o IFN-γ, que envía sinais a outras céllas inmunitarias, e mediadores citotóxicos como a perforina e grancima, que entran na célula diana e promoven a morte celular ao desencadear a apoptose. Este proceso denomínase citotoxicidade mediada por células dependente de anticorpo (ADCC). O FcγRIII das células NK pode tamén asociarse con IgG monoméricas (é dicir, a IgG que non está unida a antíxenos). Cando isto ocorre, o receptor de Fc inhibe a actividade da célula NK.[30]
Os anticorpos IgE únense aos antíxenos dos alérxenos. Estas moléculas de IgE unidas a alérxenos interaccioan con receptores Fcε na superfice de mastocitos. A activación dos mastocitos despois da unión ao FcεRI ten como resultado un proceso chamado desgranulación, no que os mastocitos liberan moléculas preformadas dos seus gránulos citoplásmicos onde estaban almacenados; estes son unha mestura de compostos como a histamina, proteoglicanos e serina proteases.[31] Os mastocitos activados tamén sintetizan e segregan mediadores derivados de lípidos (como as prostaglandinas, leucotrienos e factor activador de plaquetas) e citocinas (como interleucina 1, interleucina 3, interleucina 4, interleucina 5, interleucina 6, interleucina 13, factor de necose tumoral-alfa, GM-CSF, e varias quimiocinas).[32][33] Estes mediadores contribúen á inflamación ao atraer outros leucocito.
Os parasitos grandes como os vermes Schistosoma mansoni son demasiado grandes como para ser inxeridos polos fagocitos. Ademais, teñen unha estrutura externa chamada tegumento que é resistente ao ataque por substancias liberadas por macrófagos e mastocitos. Porén, estes parasitos poden quedar cubertos con IgE e son recoñecidos polo FcεRI na superficie dos eosinófilos. Os eosinófilos activados liberan mediadores preformados como a proteína básica maior e encimas como a peroxidase, contra os cales os vermes non son resistentes.[34][35] A interacción do receptor FcεRI coa porción Fc das IgE unidas ao verme causa que o eosinófilo libere estas moléculas por un mecanismo similar ao da célla NK durante a ADCC.[36]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.